CopyRight 2009-2020 © All Rights Reserved.版权所有: 中国海关未经授权禁止复制或建立镜像
猕猴桃腐烂病菌鉴定及室内杀菌剂筛选
作者:邵宝林1 杨益芬1 鲁 昕1 刘露希1 宿白玉1 张 莹2 廖 芳2
邵宝林1 杨益芬1 鲁 昕1 刘露希1 宿白玉1 张 莹2 廖 芳2
摘 要 猕猴桃腐烂病菌是引起猕猴桃果实采后腐烂变质的一类重要病原,在储藏、运输及销售环节均可能导致严重的经济损失,制约着猕猴桃产业的健康发展。本文针对猕猴桃腐烂病开展了病原鉴定及室内杀菌剂筛选,研究结果表明,引起猕猴桃腐烂的病菌主要为葡萄座腔菌(Botryosphaeria dothidea)、间座壳菌(Diaporthe spp.,无性态为拟茎点霉菌Phomopsis spp.)和灰葡萄孢(Botrytis cinerea)。供试杀菌剂中,戊唑·咪鲜胺对分离获得的腐烂病菌生长均能起到明显的抑制作用,EC50(μg/mL)分别为0.0443、0.0093和0.1383。效果次之的是10%苯醚甲环唑,EC50(μg/mL)分别为0.0489、0.1060和1.2130。本研究结果可为猕猴桃腐烂病的有效防控提供理论依据。
关键词 猕猴桃;病菌真菌;鉴定;杀菌剂毒力
Isolation and Identification of Pathogenic Fungi Causing Post-harvest Fruit Rot of Kiwifruit and Indoor Screening of Fungicides
SHAO Bao-Lin1 YANG Yi-Fen1 LU Xin1 LIU Lu-Xi1
SU Bai-Yu1 ZHANG Ying2 LIAO Fang2
Abstract The pathogenic fungi causing post-harvest fruit rots of kiwifruit are important pathogens that cause serious economic losses during storage, transportation and sales. In this research, the pathogenic fungi of kiwifruit were isolated, cultured and identified. It was discovered that the pathogens causing kiwifruit rot were mainly Botryosphaeria dothidea, Phomopsis/Diaporthe sp. and Botrytis cinerea, of which Botrytis cinerea has the strongest pathogenicity. The results of indoor screening of fungicides showed that the tebuconazole·prochloraz among the tested fungicides could inhibit the growth of Botryosphaeria dothidea, Phomopsis/Diaporthe sp. and Botrytis cinerea, and it was the best fungicide with EC50 (μg/mL) values of 0.0443, 0.0093 and 0.1383 respectively, followed by the difenoconazole with EC50 (μg/mL) values of 0.0489, 0.1060 and 1.2130 respectively. The research results can provide theoretical basis for guiding the prevention and control of post-harvest fruit rots of kiwifruit.
Keywords kiwifruit; pathogenic fungi; identification; toxicity of fungicides
基金项目:四川省科技计划项目(2018JY0288)
第一作者:邵宝林(1980&—),男,汉族,山东东营人,博士,高级农艺师,主要从事进出境植物检疫及植物病害生物防治研究工作,E-mail: sbl0218@126.com
1.成都海关技术中心 成都 610041
2.天津海关动植物与食品检测中心 天津 300461
1.Technical Center of Chengdu Customs, Chengdu 610041
2. AnimalPlant and Food Inspection Center of Tianjin Customs, Tianjin 300461
猕猴桃质地柔软,味道酸甜,富含糖类、维生素C和多种氨基酸,营养价值高,深受消费者青睐。同时,猕猴桃的经济价值也很高。据《中国猕猴桃产业发展报告2017》统计数据[1],全球猕猴桃产量前三名为中国、意大利及新西兰。2016年我国猕猴桃产量达到237万吨,主要集中在陕西、河南和四川等地,此三省产量占我国猕猴桃总产量的85.2%。目前,我国猕猴桃种植面积跃居世界第一,超过其他各国种植面积总和。2018年,我国猕猴桃种植面积达17.6万公顷。其中,红心猕猴桃种植面积较大,并以其独特的风味迅速走红,畅销欧美、日本及我国香港地区,出口呈逐年增长趋势,产业发展迅速,市场前景广阔。但猕猴桃采后容易发生腐烂,尤其是病原微生物引发的腐烂发展速度快,在储藏、运输及销售环节均能导致严重的经济损失,制约着猕猴桃产业的健康发展。
猕猴桃腐烂病菌主要为害近成熟期和贮藏期的果实,对果实的侵害始于花期和幼果期,在果肉内长期潜伏,采摘时通常果实外表无症状,直到果实处于后熟过程中才发病。在猕猴桃腐烂病防控方面,因生物防治和植物源农药在国内尚未大面积推广,化学防治仍是首选的防控措施。因此,为指导科学合理施药,防止滥用药的情况出现,针对猕猴桃腐烂病开展病原鉴定及室内杀菌剂筛选十分必要。尽管毒力测定应使用原药才能反映杀菌剂有效成分的真实毒力作用,但为客观评价杀菌剂对致病菌的抑制作用,本研究以田间实际所用商品化制剂为研究对象,通过毒力测定筛选最佳杀菌剂,研究结果可为猕猴桃腐烂病的有效防控提供参考依据。
1 材料与方法
1.1 材料
本研究收集了四川猕猴桃生产基地及网络电商销售的果实,从中挑选具有腐烂症状的猕猴桃病果作为实验样本。结合田间实际用药选择以下杀菌剂:10%苯醚甲环唑水分散粒剂(上海禾本药业股份有限公司);25%吡唑嘧菌酯悬浮剂(山东胜邦绿野化学有限公司);戊唑·咪鲜胺水乳剂(总有效成分含量45%,戊唑醇含量15%,咪鲜胺含量30%,海南正业中农高科股份有限公司);2%春雷霉素水剂(湖南博士威农用化学有限公司);40%喹啉铜悬浮剂(上海泰丰化工有限公司);波尔·锰锌可湿性粉剂(总有效成分含量78%,波尔多液含量48%,代森锰锌含量30%,美国仙农有限公司);氢氧化铜水分散粒剂(有效成分含量46%,美国杜邦公司)。
1.2 方法
1.2.1 病原真菌的分离培养及形态学观察
挑选腐烂病果作为病菌分离培养的实验材料,用70%乙醇对病果表面消毒,取病健交界处果肉组织转移至含氯霉素的PDA平板上,置于25℃恒温培养箱中进行培养。将培养物分离纯化后,定期观察菌落生长情况,并记录菌落培养性状,包括菌落颜色、形状等,同时在显微镜下测量记录分生孢子形状及大小等。
1.2.2 分子生物学鉴定
1.2.2.1 病菌液体培养
从分离纯化好的菌落平板上挑取适量菌丝,转移至PDB培养基。
培养条件:28℃,130 r/min,培养2 d~3 d,若菌丝量少,可延长培养时间。
1.2.2.2 DNA提取
收集菌丝,晾干或用灭菌滤纸吸干水分,液氮研磨待用。DNA提取采用CTAB提取法,或者采用商品化的基因组提取试剂盒。具体操作中,通过超微量核酸蛋白测定和琼脂糖凝胶电泳来检测DNA提取质量。
1.2.2.3 PCR反应
采用引物对ITS4/ITS5扩增,引物序列为ITS4:5'-TCCTCCGCTTATTGATATGC-3';ITS5:5'-GGAAGTAAAAGTCGTAACAAGG-3'。
反应体系为30 μL:10×PCR buffer(含Mg2+)3 μL,dNTPs(2.5 mmol/L)2 μL,上下游引物(10 μmol/L)各1.0 μL,Taq DNA聚合酶0.4 μL,DNA模板1.0 μL(30 ng/μL),ddH2O 21.6 μL。
PCR反应程序:94℃预变性3 min;94℃变性30 s,55℃复性30 s,72℃延伸1 min,35个循环;72℃延伸7 min,保存于4℃。
1.2.2.4 电泳及测序
PCR产物用1.5%琼脂糖凝胶进行电泳,EB染色后凝胶成像观察,如有目标片段大小(500 bp~600 bp)的条带出现,PCR产物送基因公司进行序列测定。
1.2.2.5 rDNA-ITS序列分析
将测序获得的序列与NCBI网站GenBank中相关序列进行同源性比对分析,在NCBI数据库中进行相似性检索,采用ClustalW进行对齐,用邻接法(Neighbor-joining, N-J)构建系统发育进化树,并用自举法对其进行检验,重复1000次,进而分析分类地位。
1.2.3 致病性测定
选用健康的猕猴桃果实接种,用70%乙醇对果实表面擦拭消毒。采用创伤法接种菌丝块,设置无菌水空白对照。实验设置3次重复,每个重复设3个处理,20℃~22℃保湿2 d,室温下继续培养观察;出现症状后,取发病部位的病健交界组织进行真菌再分离,完成柯赫氏法则验证,确认分离获得的真菌是否为致病菌。
1.2.4 室内药效测定
将不同浓度的药液加入PDA培养基中制成含药平板,以无菌水作对照。用打孔器在病菌菌落边缘处打孔,将菌饼转接至含药平板中央,设3个重复,放置25℃培养箱中,5 d后观察菌落生长情况,十字交叉法进行测量。抑菌率计算公式如下:

杀菌剂有效成分的浓度转换成对数,抑菌率转换成机率值,以浓度对数值为自变量,抑菌机率值为因变量,求出毒力回归方程,以EC50衡量杀菌剂毒力大小。
2 结果分析与讨论
2.1 猕猴桃腐烂病菌的分离与鉴定
从猕猴桃腐烂病果上分离纯化共获得45个真菌菌株,通过培养性状、形态特征观察及致病性测定,引起猕猴桃腐烂病菌共3株,在PDA平板上的菌落特征见图1。采用ITS4/ITS5引物进行PCR扩增,产物送基因公司测序,随后将测序获得的序列与NCBI网站GenBank中相关序列进行同源性比对分析(见表1),鉴定出以下真菌:菌株B为葡萄座腔菌(Botryosphaeria dothidea),菌株G为间座壳菌(Diaporthe sp.,无性态为拟茎点霉菌Phomopsis sp.),菌株O为灰葡萄孢(Botrytis cinerea),选取与分离菌株序列相似性较高的菌株作为参比菌株构建系统发育树(见图2)。
2.2 室内杀菌剂的筛选
以葡萄座腔菌(菌株B)、拟茎点霉菌(菌株G)、灰葡萄孢菌(菌株O)为对象,结合田间实际用药情况,对7种常用的杀菌剂进行室内筛选。结果表明,不同杀菌剂对猕猴桃腐烂病菌的抑菌效果存在较大差异,其中,戊唑·咪鲜胺水乳剂对供试病菌均起到抑菌作用,且效果最好;苯醚甲环唑次之。从不同杀菌剂对菌株B、G、O的毒力看(见表2~4),供试杀菌剂中45%戊唑·咪鲜胺是最佳防治药剂,EC50分别为0.0093 μg/mL、0.1383 μg/mL和0.0443 μg/mL,95%置信区分别为0.0054~0.0159、0.1167~0.1640、0.0170~0.1155;10%苯醚甲环唑效果次之,EC50分别为0.1060 μg/mL、1.2130 μg/mL和0.0489 μg/mL,95%置信区分别为0.0888~0.1266、0.8569~1.7171、0.0081~0.2957;吡唑嘧菌酯对菌株B、G的毒力比对菌株O的毒力强。在铜制剂中,40%喹啉铜优于46%氢氧化铜,其中46%氢氧化铜对菌株O无抑菌效果。

图1 3株猕猴桃腐烂病菌在PDA平板上的菌落特征
Fig.1 Colony morphology of 3 fungal isolates on PDA medium
表1 3株猕猴桃腐烂病菌同源性比对分析
Table 1 The analysis results of 3 fungal isolates by NCBI BLAST
菌株编号 | 目标片段大小/bp | 同源性比对 | 同源性/% | |
最同源的种 | GenBank序列号 | |||
B | 505 | 葡萄座腔菌(Botryosphaeria dothidea) | KF778787.1 | 100.00 |
G | 576 | 间座壳菌(拟茎点霉菌的有性态)(Diaporthe hongkongensis) | NR_111848.1 | 97.74 |
O | 515 | 灰葡萄孢(Botrytis cinerea) | KC172064.1 | 100.00 |
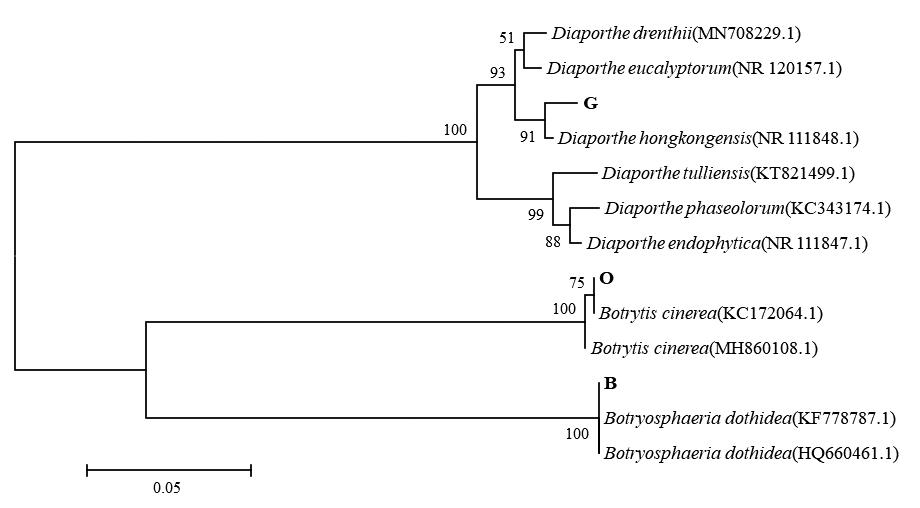
图2 基于ITS基因序列构建的猕猴桃腐烂病菌系统发育树(N-J)
Fig.2 Neighbor-joining tree based on rDNA-ITS sequences of 3 fungal isolates and related fungal species
2.3 讨论
猕猴桃是一种呼吸跃变型水果,采后极易成熟软化,引起腐烂的生理性病害与病理性病害在无病征的情况下很难区分,尤其是储藏条件不佳、机械创伤等引起的腐烂,后期着生腐生菌,从而导致不能准确判断腐烂病原。猕猴桃腐烂病害多是采前携带潜伏的病原菌或采后病原菌侵染所致,因采收时间不当,果实进入呼吸跃变高峰期更易软化腐烂。因此,采前的病害防控和采后储藏管理尤为重要,采收入库操作应避免划伤、挤压等,入库后应注意储藏温度和湿度,避免出现货物混放、堆放过密、不通风等情况。
表2 不同杀菌剂对菌株B的毒力
Table 2 The toxicity of fungicides against isolate B
杀菌剂 | 毒力回归方程 | 相关系数r | EC50/(μg/mL) |
45%戊唑·咪鲜胺 | Y=5.8888+0.6566x | 0.9762 | 0.0443 |
2%春雷霉素 | Y=4.4335+0.2924x | 0.9885 | 86.5677 |
40%喹啉铜 | Y=5.4376+0.6265x | 1.0000 | 0.2003 |
10%苯醚甲环唑 | Y=5.3528+0.2691x | 0.9470 | 0.0489 |
25%吡唑醚菌酯 | Y=5.2228+0.2995x | 0.9947 | 0.1804 |
78%波尔·锰锌 | Y=4.6404+0.3213x | 1.0000 | 13.1650 |
46%氢氧化铜 | Y=4.2453+0.9124x | 0.9432 | 6.7170 |
表3 不同杀菌剂对菌株G的毒力
Table3 The toxicity of fungicides against isolate G
杀菌剂 | 毒力回归方程 | 相关系数r | EC50/(μg/mL) |
45%戊唑·咪鲜胺 | Y=6.2016+0.5911x | 0.9903 | 0.0093 |
2%春雷霉素 | Y=1.5594+3.0228x | 0.9513 | 13.7471 |
40%喹啉铜 | Y=6.7942+3.0704x | 0.9635 | 0.2604 |
10%苯醚甲环唑 | Y=5.8063+0.8272x | 0.9994 | 0.1060 |
25%吡唑醚菌酯 | Y=5.4496+0.4772x | 0.9957 | 0.1142 |
78%波尔·锰锌 | Y=3.6444+0.8888x | 0.9979 | 33.5128 |
46%氢氧化铜 | Y=4.2740+0.6023x | 0.9954 | 16.0513 |
表4 不同杀菌剂对菌株O的毒力
Table4 The toxicity of fungicides against isolate O
杀菌剂 | 毒力回归方程 | 相关系数r | EC50/(μg/mL) |
45%戊唑·咪鲜胺 | Y=5.9633+1.1213x | 0.9990 | 0.1383 |
2%春雷霉素 | Y=4.5632+0.6206x | 0.9901 | 5.0568 |
40%喹啉铜 | Y=3.4901+0.7764x | 0.9839 | 88.0611 |
10%苯醚甲环唑 | Y=4.9782+0.2604x | 0.9993 | 1.2130 |
25%吡唑醚菌酯 | Y=4.5882+0.4402x | 0.9978 | 8.6183 |
78%波尔·锰锌 | Y=4.6639+0.1593x | 1.0000 | 128.7479 |
46%氢氧化铜 | - | - | - |
国内关于猕猴桃腐烂病病原鉴定及药剂筛选方面的研究较多。姜景魁等[2]认为引起猕猴桃果实腐烂的黃腐病病原为拟茎点霉(Phomopsis sp.),对病原菌的种还需进一步鉴定。王小洁等[3]认为引起猕猴桃软腐病的病原为葡萄座腔菌(Botryosphaeria dothidea),50%多菌灵可湿性粉剂1000倍液的抑菌效果最好,抑制率高达91.97%,95%三唑醇1600倍液次之,抑制率为81.72%。段爱莉等[4]认为引起陕西省周至县“华优”“海沃德”“秦美”猕猴桃贮藏期果实霉烂优势病原菌为青霉菌(Penicillium spp.)。李诚等[5]确定江西奉新猕猴桃灰霉病的病原菌为Botrytis cinerea(有性态Botryotinia fuckeliana),认为肟菌·戊唑醇、氟硅唑和异菌脲的抑菌效果很好,EC50分别为0.1180 g/mL、0.2886 g/mL和0.3552 g/mL。王井田等[6]认为己唑醇微乳剂、咪酰胺锰盐可湿性粉剂对猕猴桃果实腐烂病病菌拟茎点霉(Phomopsis sp.)具有较高的抑制活性,其EC50分别为0.068 μg/mL、0.105 μg/mL。黎晓茜等[7]从采集烂果分离到致病能力较强的盘多毛孢菌Pestalotiopsis gracilis,筛选到抑制效果较好的42.4%唑醚·氟酰胺悬浮剂、复配剂(80%甲基硫菌灵可湿性粉剂与40%嘧菌酯悬浮剂按1∶1混合)、40%氟硅唑乳油等3种杀菌剂,EC50分别为0.068 mg/L、0.220 mg/L和2.187 mg/L。李黎等[8]用28种真菌杀菌剂对Botryosphaeria dothidea, Diaporthe actinidiae, Pestalotiopsis microspora, Alternaria alternata等4种猕猴桃果实腐烂病菌进行了室内药剂防治测定,认为45%代森铵150倍液及30%琥胶肥酸铜300倍液对4种病原菌菌丝生长的抑制效果最好,抑制率高达88.19%。本文作者认为,引起猕猴桃腐烂的病菌主要为葡萄座腔菌(Botryosphaeria dothidea)、间座壳菌(Diaporthe sp.,无性态为拟茎点霉菌Phomopsis sp.)、灰葡萄孢(Botrytis cinerea),其中,灰葡萄孢(Botrytis cinerea)在低温储藏条件下也可生长[9],且在为害猕猴桃时产生乙烯,加速果实软化,缩短贮藏期[10],应引起高度重视。另外,试验中发现红阳猕猴桃极不耐存储,致病性测定也显示最易感病。室内杀菌剂筛选试验结果表明,不同杀菌剂对拟茎点霉菌、灰葡萄孢菌、葡萄座腔菌的毒力表现出较大差异,供试杀菌剂中戊唑·咪鲜胺水乳剂是最佳防治药剂,EC95分别为5.6222 μg/mL、4.0531 μg/mL和14.1757 μg/mL,95%置信区分别为1.7586~17.9743、2.7785~5.9125和3.2674~61.5007,但在实际生产中是否最优还有待进一步验证,施用浓度还需结合生产实际进一步优化。
3 结论
通过对猕猴桃腐烂病果的病原分离与鉴定,发现引起猕猴桃腐烂的病菌主要为葡萄座腔菌(Botryosphaeria dothidea)、间座壳菌(Diaporthe sp.,无性态为拟茎点霉菌Phomopsis sp.)和灰葡萄孢(Botrytis cinerea);通过室内杀菌剂筛选,供试7种杀菌剂中45%戊唑·咪鲜胺水乳剂为最佳杀菌剂,其次是10%苯醚甲环唑水分散粒剂。本研究结果可为后续猕猴桃采后病害发生规律研究以及制定有效防控措施提供参考依据。
【该文经CNKI学术不端文献检测系统检测,总文字复制比为9%。】
参考文献
[ 1] 上官王强. 中国猕猴桃产业发展报告2017[M]. 北京: 中国农业出版社, 2017: 3, 6.
[2] 姜景魁, 张绍升, 廖廷武, 等. 猕猴桃黄腐病的研究[J]. 中国果树, 2007(6): 14 - 16.
[3] 王小洁, 李士谣, 李亚巍, 等. 猕猴桃软腐病病原菌的分离鉴定及其防治药剂筛选[J]. 植物保护学报, 2017, 44(5): 826 - 832.
[4] 段爱莉, 雷玉山, 孙翔宇, 等. 猕猴桃果实贮藏期主要真菌病害的rDNA-ITS鉴定及序列分析[J]. 中国农业科学, 2013, 46(4): 810 - 818.
[5] 李诚, 蒋军喜, 赵尚高, 等. 猕猴桃灰霉病病原菌鉴定及室内药剂筛选[J]. 植物保护, 2014, 40(3): 48 - 52.
[6] 王井田, 刘达富, 刘允义, 等. 猕猴桃果实腐烂病的发病规律及药剂筛选试验[J]. 浙江林业科技, 2013, 33(3): 55 - 57.
[7] 黎晓茜, 曾彬, 尹显慧, 等. 修文县猕猴桃腐烂病病原鉴定及防治药剂筛选[J].中国南方果树, 2016, 45(5): 101 - 104.
[8] 李黎, 潘慧, 邓蕾, 等. 猕猴桃果实腐烂病最佳防治药剂的室内筛选[J]. 中国南方果树, 2019, 48(4): 83 - 86.
[9] 高磊, 罗轩, 张蕾, 等. 猕猴桃采后真菌腐烂病害发生与防治技术研究进展[J].中国果树, 2018, (3): 72 - 76.
[10] Qadir A. Ethylene production by Botrytis cinerea and infected kiwifruit[D]. New Zealand: Massey Univer sity,1994.
(文章类别:CPST-B)







