CopyRight 2009-2020 © All Rights Reserved.版权所有: 中国海关未经授权禁止复制或建立镜像
高效液相色谱(HPLC)法测定化妆品中对甲苯磺酸异丙酯含量
作者:杨永超1 杜 宇1 何 成1 于艳军1 韩 伟1 李宁涛1 熊中强1 王利兵1*
杨永超1 杜 宇1 何 成1 于艳军1 韩 伟1 李宁涛1 熊中强1 王利兵1*
摘 要 建立了测定化妆品中对甲苯磺酸异丙酯(IPTS)含量的高效液相—二极管阵列检测器(HPLC-DAD)方法。方法采用C18(250 mm×4.6 mm,5μm)反相柱;流动相为乙腈—20 mM乙酸铵水溶液(pH=3),等度洗脱,流速1.0 mL/min;柱温为35℃;采集波长为227 nm。结果表明在0.5~50μg/mL浓度范围内,IPTS的浓度与峰面积呈现良好的线性关系,线性相关系数r=0.9996,检测限(LOD)和定量限(LOQ)分别为2.5μg/mg、5.0μg/mg。方法在低、中、高三浓度水平的添加回收率为95.8%~108.1%,RSD在0.72%~2.27%范围内。方法用于市售化妆品中IPTS的检测,1个样品检出为阳性,并用紫外吸收光谱和气质联用仪(GC-MS)进行确证,结果为假阳性。试验证明该方法简便准确,检测限较低,满足实际检测需要,可用于化妆品中IPTS的检测。
关键词 化妆品;对甲苯磺酸异丙酯;高效液相色谱;GC-MS确证
Determination of Isopropyl P-toluenesulfonate in Cosmetics by High-performance Liquid Chromatography
YANG Yong-Chao1 DU Yu1 HE Cheng1 YU Yan-Jun1
HAN Wei1 LI Ning-Tao1 XIONG Zhong-Qiang1 WANG Li-Bing1*
Abstract A sensitive and rapid method was developed for the determination of isopropyl p-toluenesulfonate (IPTS) in cosmetics by high-performance liquid chromatography with a diode array detector (HPLC-DAD). The method uses a C18 (250 mm×4.6 mm, 5μm) reversed phase column; the mobile phase was acetonitrile-20 mM ammonium acetate aqueous solution (pH=3), isocratic elution, flow rate 1.0 mL/min; column temperature was 35℃; The collection wavelength is 227 nm. The results show that in the concentration range of 0.5-50μg/mL, the concentration of IPTS has a good linear relationship with the peak area; the linear correlation coefficient r=0.999 6, the limit of detection and quantification (LOD and LOQ) were 2.5μg/mg and 5.0μg/mg, respectively. The recovery rate at low, medium and high levels is 95.8% -108.1% with relative standard deviations from 0.72% to 2.27%. Then the simple protocol was applied to the determination of IPTS in cosmetics. One positive sample was detected and confirmed by UV absorption spectrum and gas chromatography-mass spectrometry (GC-MS), indicating a false positive result. Results showed that the method could serve for cosmetics supervision in determination of the toxic IPTS.
Keywords cosmetics; isopropyl p-toluenesulfonate; high-performance liquid chromatography; confirmed by GC-MS
棕榈酸异丙酯(IPP)和肉豆蔻酸异丙酯(IPM)是一种低黏度亲油类的非离子型表面活性剂,具有良好的铺展性、润滑性、滋润度、保湿性、透气性以及极佳的皮肤相容性,对皮肤和黏膜的刺激性很低,可使皮肤光滑、柔润、富有弹性。因而广泛应用于化妆品中,如护肤霜、发油、毛发调理剂等,特别是婴幼儿产品和高档化妆品中[1-3]. 目前两种重要化合物的合成途径主要是相应的棕榈酸、肉豆蔻酸分别与异丙酯在催化剂——对甲苯磺酸作用下酯化得到,在特定情况下,对甲苯磺酸与异丙酯也会发生酯化反应,从而生成副产物对甲苯磺酸异丙酯(isopropyl p-toluenesulphonic acid ester,IPTS)[4]。
研究表明,对苯磺酸酯类是一种潜在的毒性物质[5-7],这些物质可与DNA发生烷基化反应[8-9]从而诱发癌症。截至目前,IPTS在世界范围内尚未列入化妆品的“禁限用”组分中。但是,欧洲药品管理局(EMA)和美国食药局对这类毒性物质已经起草了相应的指南,其毒理学关注阈值为1.5μg/人/天[10-11]。因此,不久的将来,IPTS极有可能被列入化妆品有毒有害物质的监管目录中。
随着化妆品产业的发展,人们接触化妆品的概率和频率都在急速上涨。IPP和IPM的存在,加快、加深了皮肤对IPTS的吸收,进一步加大了消费者使用化妆品时的安全风险。因此,对化妆品中该毒性物质浓度水平的控制至关重要。
目前,对于这类物质的检测,主要有气质联用(GC-MS)技术[12]、高效液相色谱[13]和液相色谱串联质谱技术[14]。现有的报道几乎都是对药物中IPTS的测定,而对于化妆品则鲜有报道。因此,本文建立一种高效液相色谱(HPLC)方法,联合GC-MS确证,试验结果表明该方法可以简便快速测定化妆品中IPTS的含量。
1 试验部分
1.1 仪器和试剂
高效液相色谱仪(美国ThermoFisher,型号: Ultimate 3000SD),配置二极管阵列检测器(DAD);气相色谱—质谱联用仪(美国布鲁克,型号:SCION-TQ);紫外可见分光光度计(美国Agilent,型号:G9822A cary300)。
对甲苯磺酸异丙酯标准品(上海安谱实验科技有限公司,货号:CDDM-I873800-1 g,纯度:97.0%);乙腈(色谱纯);乙酸铵(优级纯);超纯水。
1.2 标准储备液配制
精密称取对甲苯磺酸异丙酯标准品约10.0 mg(精确至0.1 mg),置10.0 mL量瓶中,加乙腈溶解并稀释至刻度,摇匀,作为标准储备液(现配现用)。
1.3 样品制备
称取0.1 g(精确至0.001 g)化妆品样品置于10 mL带盖带刻度样品管中,加入5 mL乙腈,超声提取10 min,10000 r/min离心2 min,取上层清液经0.45μm滤膜过滤后上机测试。
1.4 色谱条件
色谱柱为ThermoFisher AcclaimTM 120-C18 (250 mm×4.6 mm, 5μm)。流动相为乙腈-20 mmol/L乙酸铵水溶液(50:50,乙酸铵水溶液提前用乙酸调至pH=3),流速为1.0 mL/min,检测波长为227 nm,进样量5μL。
1.5 GC-MS确证条件
色谱条件:色谱柱为毛细管柱(HP-5 30 m × 0.25 mm ×0.25μm)。氦气(纯度99.99%)为载气,流速1.0 mL/min。程序升温:起始温度为100℃,维持1 min,然后升至250℃,保持10 min,升温速率为10℃/min。进样口温度250℃,分流比10:1,进样体积1.0μL,溶剂延迟4 min。
质谱条件:EI源(电子轰击电离源),电子能量为80 eV,离子源温度为250℃。扫描方式为选择离子扫描(SIM),选择离子(m/z:91、172、214)。
2 结果与讨论
2.1 波长选择
对IPTS溶液进行全波长(190-800nm)扫描。对甲苯磺酸异丙酯的紫外吸收图谱在227 nm处有最大吸收,因此,本实验选择227 nm作为检测波长。
2.2 稳定性试验
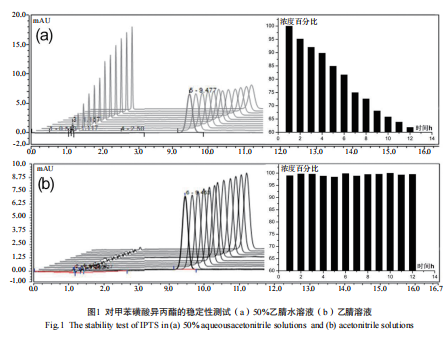
试验考察了IPTS在不同溶液A和B中的稳定性。A为50%乙腈/水,B标准溶液的溶剂为乙腈,分别于室温放置12 h,期间每小时测量A和B标准溶液的浓度,以研究标准溶液的稳定性,测试结果如图1所示。图(a),A标准溶液,随着时间的推移IPTS的峰面积(Rt=9.48)在逐渐减小,从其柱形图中看出,12 h后,IPTS浓度仅剩60%左右;而图(b),B标准溶液,12小时内,IPTS的浓度基本无变化,表明IPTS在乙腈中的稳定性良好,试验说明,水相增加,IPTS稳定性降低,因此标准溶液配制选择乙腈做溶剂,最好现用现配。
2.3 色谱柱的选择
试验考察了Acclaim 120-C18和ZORBAX Eclipse XDB-CN(规格都为250 mm×4.6 mm,5μm)反相柱分离效果。结果表明,二者都能很好的分离出IPTS,都可满足分析需求。但是后者出峰时间比前者更早一些,易被杂质峰干扰,若通过改变流动相比例,调整合适的出峰时间,需要加入更多的水相,会降低IPTS的稳定性。故选用Acclaim 120-C18(250 mm×4.6 mm,5μm)为本试验的色谱柱。
2.4 流动相的选择
试验考察了90:10(V/V),70:30(V/V)和50:50(V/V)水-乙腈流动相对分离效果的影响。结果表明,流动相为50:50(V/V)水-乙腈时,IPTS峰形尖锐且对称,并且出峰时间大于9 min,可有效避免极性较大的杂质峰的干扰(一般出峰时间小于5 min)。然而50:50(V/V)水-乙腈流动相,并不适用于所有类型的化妆品,对于部分乳液,精华乳等,会出现干扰峰。因此,水相中加入20 mmol/L的乙酸铵(乙酸铵水溶液提前用乙酸调至pH=3),干扰峰消失,这可能是由于乙酸铵与样品中的杂质相互作用,起到了消除基质干扰的效果[15-17]。故选用20 mmol 乙酸铵(pH值=3)水溶液-乙腈(V/V =50:50)为本实验的流动相。
2.5 提取剂的选择
试验考察了乙腈、乙酸乙酯、甲醇、正己烷对化妆品中IPTS的提取效果,见图2(a)。结果表明,正己烷效率最低,乙腈,甲醇和乙酸乙酯的提取效率相差不大,乙腈略高,且杂质干扰最少,故选用乙腈为萃取溶剂。
2.6 提取时间的优化
以乙腈作为萃取剂,考察了超声提取时间(5 min-20 min)对提取效果的影响,结果如图2(b)所示。提取时间为10 min时,提取几近完全,10 min后提取效率基本保持一致,方法最终选择超声提取时间为10 min。
3 方法学验证
3.1 线性范围
精密量取1.2标准储备液0.5 mL、0.25 mL、0.1 mL、0.05 mL、0.01 mL,分别置10 mL 量瓶中,加乙腈溶剂稀释至刻度,摇匀,得浓度为50.0μg/mL、25.0μg/mL、10.0μg/mL、5.0μg/mL、1.0μg/mL溶液,然后用1.0μg/mL标准溶液稀释得到0.5μg/mL溶液,最终得到线性系列溶液50.0μg/mL、25.0μg/mL、10.0μg/mL、5.0μg/mL、1.0μg/mL、0.5μg/mL(共计6个浓度点)。上机测试,记录对甲苯磺酸异丙酯峰面积。以浓度(μg/mL)为横坐标x,主峰面积为纵坐标y,进行线性回归。回归曲线为: y = 0.0547x-0.016,r= 0.9996。表明,IPTS在0.5~50 μg/mL范围内线性良好。
3.2 精密度试验
以浓度为20μg/mL的标准溶液为测试点,连续进样6次,记录对甲苯磺酸异丙酯峰面积,计算相应的相对标准偏差。结果显示RSD为1.96%,表明仪器精密度良好。
3.3 检测限、定量限和检出浓度、最低定量浓度
采用逐级稀释标准溶液方法进样,信噪比(S/N)为3时的样品浓度即为检测限浓度;S/N为10时的样品浓度即为定量限浓度。按此方法,进样量为5μL时,得出的检测限为(LOD)0.05μg/mL,定量限(LOQ)为0.1μg/mL。当取样量为0.1 g,5 mL乙腈提取时,相应的检出浓度为2.5μg/g,最低定量浓度为5.0μg/g。另外,方法通过增大样品的进样量,可降低检测限和定量限。
3.4 回收率
取3种空白化妆品,润肤水,乳状、膏状,每种化妆品分别添加5μg、10μg、50μg标准品,每个浓度平行6份,然后按照“1.3”项下的方法制备样品上机测试,计算回收率,结果见表1。3种化妆品的三水平添加回收率在95.8%~108.1%之间,表明各种化妆品样品的加标回收试验结果良好。相应的测定结果RSD均小于5%,该方法准确度和精密度良好。
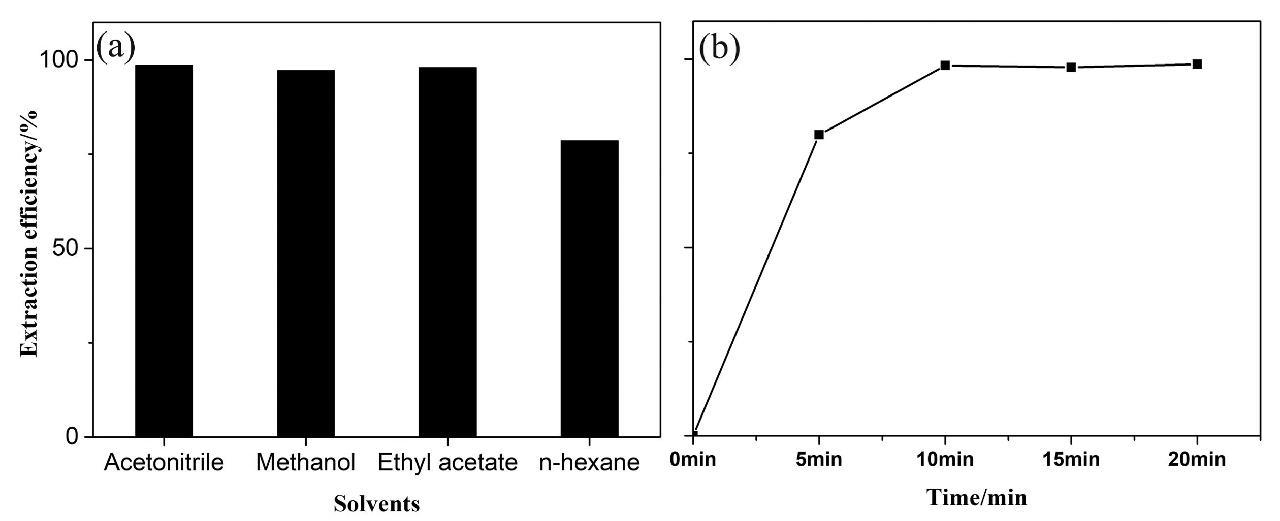
图 2 (a)溶剂和(b)提取时间对提取效率的影响
Fig.2 The effect of (a) solvents and (b) extraction time on extraction efficiencies
表1 三种化妆品回收率实验结果
Table 1 Recovery rate test results of 3 kinds of cosmetics
化妆品 | (μg·mL-1) | μg | (μg·mL-1) | % | % |
润肤水 | 未检出 | 5.0 | 1.076 | 107.6 | 0.93 |
10.0 | 2.071 | 103.6 | 0.70 | ||
50.0 | 9.722 | 97.2 | 0.88 | ||
乳液 | 未检出 | 5.0 | 1.031 | 103.1 | 1.96 |
10.0 | 1.915 | 95.8 | 1.76 | ||
50.0 | 9.652 | 96.2 | 2.27 | ||
膏状 | 未检出 | 5.0 | 1.081 | 108.1 | 0.96 |
10.0 | 2.053 | 102.6 | 1.61 | ||
50.0 | 9.660 | 96.6 | 0.72 |
3.5 GC-MS确证
试验过程中,由于化妆品成分复杂,对HPLC检测结果容易造成基质干扰,出现假阳性的现象。除了进行后台目标物和检出物的UV-vis光谱对照方法外,本文采用GC-MS方法进行进一步确证,以保证结果的准确性。按照上文确证条件,对加标的阴性化妆品样品进行GC-MS确证,图谱见图3。
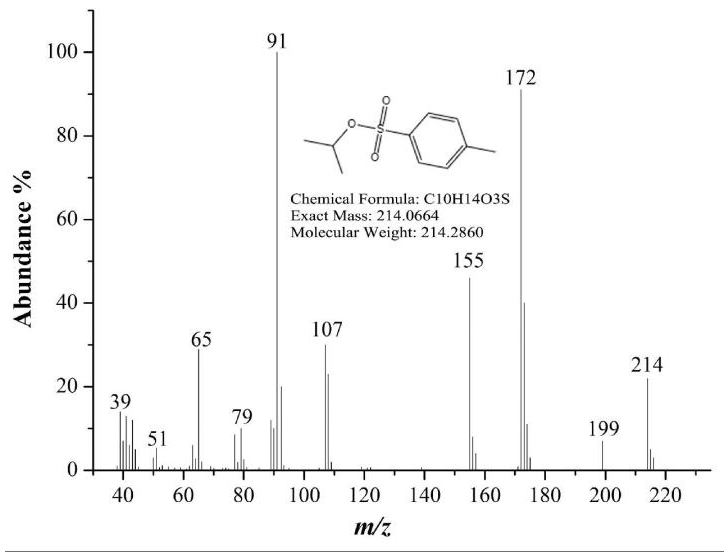
图3 GC-MS确证
Fig.3 Confirmation by GC-MS
3.6 样品检测
3.6.1 实际样品测试
取市售8种化妆品,按文中方法制备样品,上机测试,计算化妆品中对IPTS的含量。详细结果见表2。结果显示,4#样品检出IPTS,浓度为42μg/g,其他均未检出。
表2 实际样品检测结果
Table 2 Test results of samples on sale
No. | 检测结果/(μg/mL) | 换算浓度/(μg/g) |
1# | 未检出 | 未检出 |
2# | 未检出 | 未检出 |
3# | 未检出 | 未检出 |
4# | 0.84 | 42 |
5# | 未检出 | 未检出 |
6# | 未检出 | 未检出 |
7# | 未检出 | 未检出 |
8# | 未检出 | 未检出 |
3.6.2 阳性样品确证
HPLC后台提取4#样品和浓度相似的标准品(1μg/mL)的紫外吸收图谱。通过比对可知,二者的紫外图谱并不一样,证明4#样品为假阳性。
同时对4#样品提取液进行GC-MS确证,结果进一步表明,4#样品确实为假阳性。后续工作将会对该检出物质进行分析。
4 讨论
本文建立了高效液相色谱法测定化妆品中的毒性物质—对甲苯磺酸异丙酯(IPTS)的方法。该方法线性与精密度良好,方法准确、可靠、操作便捷。方法用于市售化妆品中IPTS的检测,检测结果表明:8个样品中仅一个检出目标物,通过UV-Vis图谱比对及GC-MS确证,表明样品为假阳性。方法的建立健全了化妆品检测技术库,可为化妆品安全监管提供技术支持。
【该文经 CNKI 学术不端文献检测系统检测,总文字复制比为 4.7%。】
参考文献
[1]卜文娟,耿全华,阮复昌.棕榈酸异丙酯的合成研究进展[J].香料香精化妆品,2010, 48(6): 49-52.
[2] 兰宾. 化妆品工艺学[M ]. 北京: 轻工业出版社, 1987.
[3] 吴志平,张治柳,黄克瀛. 肉豆蔻酸异丙酯的合成工艺研究[J].中南林学院学报,2000, 20(4): 72-75.
[4] Tay, B. Y. P. Analysis of isopropyl para-toluenesulfonate in palm-based esters by gas chromatography with flame ionization detection and confirmed with mass spectrometry. Int. J. Cosmet. Sci. 35, 57-63 (3).
[5] 阮晓玲, 郑项元, 徐洁,等. 药物中基因毒性杂质分析方法的研究进展[J]. 中国药科大学学报,2016,47(3): 267-274.
[6] 王萍,徐彩虹,陈仙,等. 原料药中基因毒性杂质控制的研究进展[J]. 中国现代应用药学, 2015,32(1): 119-126.
[7] Glowienke, S, Frieauff, W, Allmendinger, T, Martus, H, Suter, W and Mueller, L. Structure-activity considerations and in vitro approaches to assess the genotoxicity of 19 methane-, benzene- and toluene sulfonic acid esters. Mutat Res, 2005, 581: 23-24.
[8] Stopper H, Lutz W K. Induction of micronuclei in human cell lines and primary cells by combination treatment with Î3-radiation and ethyl methanesulfonate. Mutagenesis, 2002, 17: 177-181.
[9] Garcíaa A, Rupéreza F J, Ceppa F, et al. Development of chromatographic methods for the determination of genotoxic impurities in cloperastine fendizoate. J Pharm Biomed Anal, 2012, 61: 230-236.
[10] Committee for Medicinal Products for Human Use Guidelines on the limits of genotoxic impurities, European Medicines Agency (EMEA). Available at: http://www.ema.europa. eu/WC500002903.pdf, accessed 12 September 2015.
[11] Guidance for industry genotoxic and carcinogenic impurities in drug substances and products: Recommended Approaches, U.S. Food and Drug Administration. Available at: http:// www.fda.gov/ohrms/dockets/98fr/fda-2008-d-0629-gdl.pdf, accessed 2 September 2015.
[12] 霍立,刘艳妮. 气质联用技术检测对甲苯磺酸酯类杂质[J]. 中国新技术新产, 2016, 1: 55.
[13] 孙朴. HPLC法测定氢溴酸西酞普兰中的基因毒性杂质对甲苯磺酸乙酯[J]. 药学研究, 2015, 34(11): 637-639.
[14] 梁键谋,傅聪,陈悦. LC-MS/MS测定草酸右旋西酞普兰中对甲苯磺酸酯类基因毒性杂质的含量[J]. 中国现代应用药学, 2016, 33(11): 1436-1440.
[15] Taylor G E, Gosling M, Pearce A. Low level determination of p-toluenesulfonate and benzenesulfonate esters in drug substance by high performance liquid chromatography/mass spectrometry[J]. J. Chromatogr. A, 2006, 1119: 231-237.
[16] Tay B Y P, Yung S C, Teoh T Y. Determination and confirmation of isopropyl p-toluenesulfonate in cosmetics by HPLC-diode array detector method and GC-MS[J]. International Journal of Cosmetic Science, 2016, 1-7
[17] Yadav R R, Rokade M D, Gangrade D M, et al. Determination of potentially genotoxic impurities in Sorafenib Tosylate by UPLC method[J]. International Journal of Theoretical & Applied Sciences, 2012, 4(2): 145-156.
(文章类别:CPST-C)







