CopyRight 2009-2020 © All Rights Reserved.版权所有: 中国海关未经授权禁止复制或建立镜像
离子色谱法同时测定化妆品中亚硝酸盐、苯甲酸和山梨酸的含量
作者:何 成1* 张丽娟2 张 颖1 于艳军1 熊中强1 杨永超1
何 成1* 张丽娟2 张 颖1 于艳军1 熊中强1 杨永超1
近年来,随着人们生活水平的不断提高,化妆品的使用越来越多,逐渐成为人们生活中的必需品,但生产商为了达到特定效果,往往会在化妆品中增添各种添加剂,尤其是在廉价的产品中添加剂非常常见,超标的添加剂会对皮肤带来损害,因此化妆品的安全性不容忽视。防腐剂是指可以抑制微生物生长,防止物质变质的一类添加剂。为了使化妆品能够长久保持,就必须阻止微生物的繁殖,而使用防腐剂是最经济便捷的方式之一。但是一定浓度的防腐剂积累在皮肤上会对皮肤造成伤害,如皮肤角质层损害、细胞老化加剧、皮肤过敏反应等。苯甲酸和山梨酸作为防腐剂被添加到化妆品中,起到杀菌防腐的作用。在特定条件下,亚硝酸盐可以转化为强致癌物亚硝酸铵,对人体有致癌、致畸形等严重危害。亚硝酸钠在《化妆品卫生规范》(2015版)为限用物质,在化妆品中限量为0.2%。苯甲酸和山梨酸过量接触会刺激皮肤,损害肝脏器官。在《化妆品卫生规范》(2015版)中,苯甲酸、山梨酸也同样为限用物质,苯甲酸在淋洗类化妆品中限量为2.5%;在驻留类产品和淋洗类肤用化妆品中限量为2%,且不得用于3岁以下孩子使用的产品中;山梨酸的限量值为0.6%[1]。
国内外对亚硝酸钠、苯甲酸和山梨酸的测定已有多种检测方法,主要有气相色谱法[2-4]、高效液相色谱法[5-7]和离子色谱法[8-11]等。《化妆品卫生规范》(2015版)中提供了苯甲酸、山梨酸相应的参考检验方法为高效液相色谱法和气相色谱法,但未提供亚硝酸钠的检测方法。用离子色谱法同时测定化妆品中亚硝酸钠、苯甲酸和山梨酸的含量在文献中鲜有报道。
本文建立了同时测定化妆品中亚硝酸钠、苯甲酸和山梨酸的离子色谱法,其中,亚硝酸钠、苯甲酸和山梨酸检测结果和保留时间重现性好,分离度好和回收率高,适宜日常检测。
1 试验部分
1.1 仪器与试剂
ICS1600型离子色谱仪,配ED20 电化学检测器和AS-DV自动进样装置 美国Dionex 公司;KQ800-KDE超声波清洗器 昆山市超声仪器有限公司; PL403天平 德国Sartiorias公司;旋涡振荡器 天津市泰斯特仪器有限公司;Sigma 2-16pk台式冷冻离心机 德国Sigma公司;Milli-Q Integral 10纯水机 法国密理博公司。
亚硝酸钠(色谱纯);苯甲酸:标准品级,纯度≥98%;山梨酸:标准品级,纯度≥98%;50%氢氧化钠(超纯);实验用水为超纯水,电阻率为18.5 MΩ·cm。
1.2 标准溶液的配制
淋洗液的配制:称取2.4 g质量分数为50%氢氧化钠溶液,加入烧杯中加水稀释,转移至1 L容量瓶中,定刻度,过滤后经超声脱气,作为淋洗液备用。
标准储备溶液配制(200 mg/L):亚硝酸钠标准储备溶液(200 mg/L):称取0.1 g亚硝酸钠,用超纯水溶解并定容于500 mL容量瓶中;苯甲酸标准储备溶液(200 mg/L):称取0.1 g苯甲酸,用超纯水溶解并定容于500 mL容量瓶中;山梨酸标准储备溶液(200 mg/L):称取0.1 g山梨酸,用超纯水溶解并定容于500 mL容量瓶中;将储备液置于冰箱中冷藏,使用加水前稀释至所需浓度。
1.3 仪器条件
Ion Pac AS11 阴离子交换色谱柱(250 mm×4 mm),配Ion Pac AG11 保护柱(50 mm×4 mm);洗脱条件:30 mmol/L氢氧化钠溶液为流动相;流速:1.0 mL/min;进样量:25 mL;检测器为电导检测器;柱温:30℃;抑制电流为59 mA。
1.4 样品前处理
称取质量约0.2 g样品于50 mL具塞比色管中,加水定容到刻度,加1 mL乙腈和1 mL二氯甲烷,用涡旋振荡器分散,在离心机于10000 r/min离心10 min,取上清液经0.45 μm滤膜过滤,经RP柱后,滤液供离子色谱测定用。
2 结果与讨论
2.1 提取溶剂和分散剂的选择
化妆品成分非常复杂,含有油脂、粉质等各种基质,因此提取溶剂的选择显得尤为重要;本实验比较了水、乙醇和水/乙腈作为提取剂,发现当乙醇作为提取剂时,3种待测物回收率都是最低的;当水/乙腈和水作为提取剂时,3种待测物都具有比较高的回收率,其中水/乙腈作为提取剂时,亚硝酸钠回收率最高。因此选择水/乙腈作为提取溶剂。
为了更好地分散乳状和霜状化妆品,需加入低极性有机溶剂作为分散剂。本实验考察了正己烷和二氯甲烷作为分散剂,对样品回收率进行研究,结果表明二氯甲烷作为分散剂时,待测物回收率最高,因此选择二氯甲烷作为分散剂。
2.2 超声萃取的选择
将已知的阳性样品分别超声提取0 min、10 min、20 min、30 min,测定提取液中3种待测防腐剂的含量。结果显示,超声提取时间为0~30 min内,亚硝酸盐、苯甲酸和山梨酸提取效率差异不大;而经超声提取后,样品中杂质峰干扰苯甲酸和山梨酸的分离,因此样品前处理选择不使用超声萃取。
2.3 淋洗条件的优化
在流速1.0 mL/min条件下,考察了20 mmol/L、30 mmol/L和40 mmol/L三个浓度水平的NaOH洗脱液的洗脱效果。结果显示,当洗脱液中NaOH浓度为20 mmol/L时,出峰时间较慢,检测时间过长;当洗脱液中NaOH浓度为40 mmol/L时,目标物不能很好地分离,因此选用30 mmol/L的NaOH溶液作为淋洗液。
在30 mmol/L的NaOH溶液作为淋洗液条件下,考察流速分别为0.8 mL/min、1.0 mL/min、1.2 mL/min 和1.5 mL/min时的分离效果,流速过小,分析时间过长;流速过大,虽然出峰时间快,但峰的分离度不够好。综合考虑最终选择流速1.0 mL/min,确保分离度的同时,也能实现15 min内快速出峰。
综上得到最佳的色谱条件:淋洗液NaOH的浓度为30 mmol/L,流速 1.0 mL/min。此时化妆品中亚硝酸盐、苯甲酸和山梨酸能完全分离,见图1。
2.4 方法的线性范围
将标准储备溶液用水进行稀释,配置成质量分数为1 mg/L、2 mg/L、5 mg/L、10 mg/L的标准混合工作溶液,在设定的色谱条件下,外标法定量,绘制标准工作曲线,结果见表1。由表1数据看出,本方法线性关系较好。
2.5 检出限和定量限
在优化的色谱条件下,以信号噪声的S/N=3计算,测得亚硝酸钠、苯甲酸钠和山梨酸钾检出限分别为0.25 mg/kg、50 mg/kg和70 mg/kg;以信号噪声的S/N=10相应的浓度确定定量限,3种物质定量限分别为0.50 mg/kg、120 mg/kg和150 mg/kg。
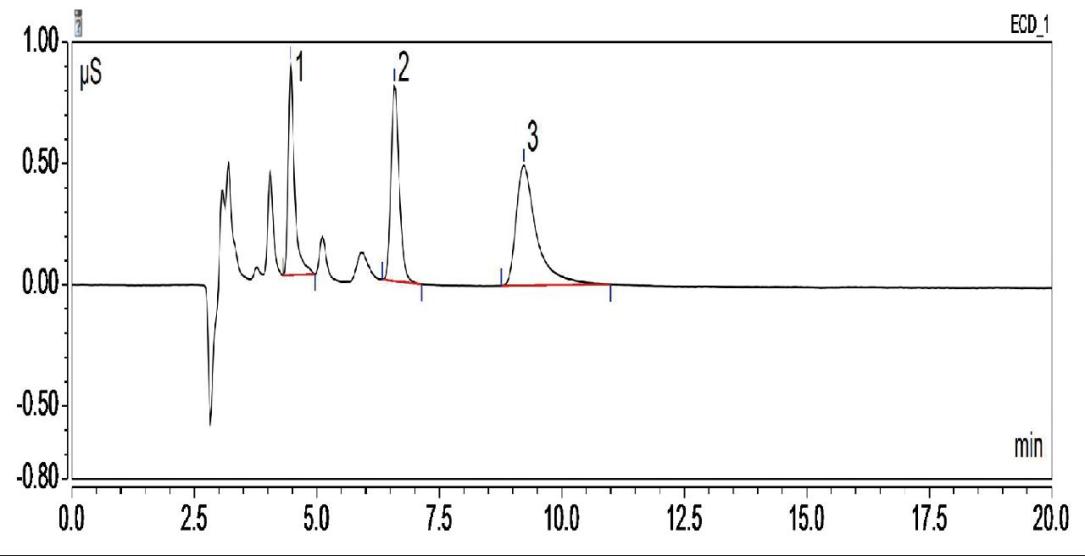
1-NO2-;2-苯甲酸;3-山梨酸
1-NO2-; 2-benzoic acid; 3-sorbic acid
图1 标准溶液的色谱分离图
Fig.1 Chromatogram of standard solution
表1 亚硝酸钠、苯甲酸钠和山梨酸钾的线性关系
Table 1 Linear relationship of sodium nitrite, sodium benzoate and potassium sorbate
Linear relationship | Correlation coefficient / r2 | Linear range (mg/L) | |
亚硝酸钠 | y = 0.1248x+0.014 | 0.9999 | 1~10 |
苯甲酸钠 | y = 0.0269x+0.0008 | 0.9995 | 1~10 |
山梨酸钾 | y = 0.052x-0.0001 | 0.9998 | 1~10 |
2.6 样品测定及加标回收试验
在优化的色谱条件下,测定某稀释后的化妆品样品,并按80%、100%和120% 3个水平进行加标回收试验,结果见表2。
表2 实际样品中亚硝酸钠、苯甲酸钠和山梨酸钾的含量及其添加回收率(n=6)
Table 2 The content and recovery rate of sodium nitrite, sodium benzoate and potassium sorbate
in actual samples(n=6)
(mg/L) | (mg/L) | (mg/L) | (mg/L) | (%) |
亚硝酸钠 | 4.5 | 3.6 | 7.88 | 97.28 |
4.5 | 4.5 | 8.54 | 94.89 | |
4.5 | 5.4 | 9.36 | 94.55 | |
苯甲酸钠 | 4.15 | 3.32 | 7.28 | 97.46 |
4.15 | 4.15 | 8.89 | 107.11 | |
4.15 | 4.98 | 9.21 | 100.88 | |
| 8.7 | 6.96 | 15.12 | 96.55 |
8.7 | 8.7 | 18.33 | 105.34 | |
8.7 | 10.44 | 18.39 | 96.08 |
2.7 精密度实验
称取6份化妆品样品,按照本方法设定的条件进行样品前处理和色谱分析,峰面积和保留时间的相对标准偏差(RSD)结果见表3。由表3数据看出,本方法精密度较好。
表3 精密度实验结果(n=6)
Table 3 Precision test(n=6)
Peak Area (RSD%) | Retention Time (RSD%) | |
亚硝酸钠 | 2.31 | 0.21 |
苯甲酸钠 | 3.02 | 0.23 |
山梨酸钾 | 4.10 | 0.29 |
3 结论
本实验建立了离子色谱法同时测定化妆品中亚硝酸钠、苯甲酸和山梨酸的分析方法。结果表明,该方法样品前处理简单,快速、准确,可用于化妆品中亚硝酸钠、苯甲酸和山梨酸的含量检测。
【该文经 CNKI 学术不端文献检测系统检测,总文字复制比为3.8%。】
参考文献
[1]《化妆品安全技术规范》(2015 年版)[S]. 国家食品药品监督管理总局, 2015.
[2] Michiko Kakemoto. Simultaneous determination of sorbic acid, dehydroacetic acid and benzoic acid by gas chromatography-mass spectrometry[J]. Journal of Chromatography A, 1992(594): 253-257.
[3] Nuttanee Tungkijanansin, Waleed Alahmad, Thumnoon Nhujak,et al.Simultaneous determination of benzoic acid,sorbic acid, and propionic acid in fermented food by headspace solid-phase microextraction followed by GC-FID[J]. Food Chemistry, 2020(329): 127161.
[4] Chunzhou Dong, Yong Mei, Lin Chena. Simultaneous determination of sorbic and benzoic acids in food dressing by headspace solid-phase microextraction and gas chromatography[J]. Journal of Chromatography A, 2006(1117): 109-114.
[5] Mingzhen Ding, Jing Peng, Shaoling Ma, et al.An environment-friendly procedure for the high performance liquid chromatography determination of benzoic acid and sorbic acid in soy sauce[J]. Food Chemistry, 2015(183): 26-29.
[6] Ittipon Techakriengkrai, Ranee Surakarnkul. Analysis of benzoic acid and sorbic acid in Thai rice wines and distillates by solid-phase sorbent extraction and high-performance liquid chromatography[J]. Journal of Food Composition and Analysis, 2007(20): 220-225.
[7] Irina Timofeeva, Daria Kanashina, Kira Stepanova, et al. A simple and highly-available microextraction of benzoic and sorbic acids in beverages and soy sauce samples for high performance liquid chromatography with ultraviolet etection[J]. Journal of Chromatography A, 2019(1588): 1-7.
[8] TeresaD’Amore, Aurelia Di Taranto, Giovanna Berardi, et al. Going green in food analysis: A rapid and accurate method for the determination of sorbic acid and benzoic acid in foods by capillary ion chromatography with conductivity detection[J]. LWT, 2021(141): 110841.
[9] Jingli Hu, Terri Christison, Jeffrey Rohrer. Determination of dimethylamine and nitrite in pharmaceuticals by ion chromatography to assess the likelihood of nitrosamine formation[J]. Heliyon, 2021(7): e06179.
[10] Eoin Murray, Patrick Roche, Matthieu Briet, et al.Fully automated, low-cost ion chromatography system for in-situ analysis of nitrite and nitrate in natural waters[J]. Talanta, 2020(216): 120955.
[11] Eoin Murray, Patrick Roche, Kevin Harrington, et al. Low cost 235 nm ultra-violet light-emitting diode-based absorbance detector for application in a portable ion chromatography system for nitrite and nitrate monitoring[J]. Journal of Chromatography A, 2019(1603): 8-14.
(文章类别:CPST-C)







