CopyRight 2009-2020 © All Rights Reserved.版权所有: 中国海关未经授权禁止复制或建立镜像
食品中大肠菌群、大肠埃希氏菌 测量不确定度评定
作者:游元丁 赵阳 徐孟怀 冉茂乾 李跃红 朱明 焦彦朝 李勤刚
游元丁 赵阳 徐孟怀 冉茂乾 李跃红 朱明 焦彦朝 李勤刚
Abstract This study is intended to establish a method for evaluating the uncertainty of coliforms and E. coli in food, and provide a uncertainty measurement approach case for the other food microbiological examination. According to the second method based on GB 4789.3-2016 National Food Safety Standard Food Microbiological Examination: Enumeration of Coliforms and GB 4789.38-2012 National Food Safety Standard Food Microbiological Examination: Escherichia coli Count and JJF 1059.1-2012 Evaluation and Representation of Uncertainty Measurement, this study took the added stains as known proficiency testing sample, analyzed the uncertainty introduced by sample preparation, dilution process, sample adding process and repeated measurement process. A mathematical model was established to analyze the uncertainty. The result shows that the coliforms expanded uncertainty (Uc) for the sample was 0.115 (p=95%, k=2.26) and the E. coli expanded uncertainty (UE.coli) was 0.115 too. The uncertainty in the process was mainly composed of the uncertainty introduced by sample single test process and the uncertainty of repeated measurement process. The uncertainty of repeating measurement process was the most contribution to the uncertainty, both of which were 97%.
Keywords coliforms; E. coli; measurement uncertainty; microorganisms
大肠菌群是在一定条件下能发酵乳糖、产酸产气的革兰氏阴性无芽孢杆菌,是国内外通用的食品污染常用指示菌之一,是评价食品卫生状况的重要指标,食品中大肠菌群含量表明食品被粪便污染的程度[1-2]。大肠菌群包括埃希氏菌属、克雷伯氏菌属、肠杆菌属和柠檬酸杆菌属等的细菌。大肠埃希氏菌、革兰氏阴性短杆菌是人和动物肠道正常寄居菌,环境适应能力很强,作为条件致病菌,大肠杆菌含有很多致病因子,包括菌毛、脂多糖复合物、夹馍和内毒素等[3-4]。与大肠菌群一样,大肠埃希氏菌菌群数量也是评估食品安全的重要指标之一。大肠菌群或大肠埃希氏菌超标的原因可能是由于产品受到了来自原料、包装材料、人员、设备等方面的污染,或者由于产品储运条件不当造成。
测量不确定度是与测量结果相关联的参数,用于表征合理赋予测量值的分散性,是衡量实验室检测能力的重要指标[5-6]。实验室通过测量不确定度的评估来度量检测结果的准确度和可信度,因此有效评价测量不确定度,科学给出检测结果对于食品安全尤为重要。
本研究根据JJF 1059.1-2012《测量不确定度评定与表示》[5]、GB 4789.3-2016《食品安全国家标准 食品微生物学检验 大肠菌群计数》[7]、GB 4789.38-2012《食品安全国家标准 食品微生物学检验 大肠埃希氏菌计数》[8],以大肠菌群和大肠埃希氏菌检测为例,通过分析检测全过程中不确定度来源,构建数据模型,探讨了食品微生物定量检测的测量不确定度评定方法,为大肠菌群、大肠埃希氏菌的日常检测工作提供测量不确定度评定依据,为食品微生物定量检测出具检测结果提供理论指导。
1 材料与方法
1.1 材料
样品:能力验证样品,按1.2.1所述进行样品制备后为液体样品。该样品来自中国检验检疫科学研究院测试评价中心组织的微生物技能考核能力验证样品,由该能力验证的技术报告可知样品添加菌株信息,见表1。
表1 样品添加菌株信息
Table 1 Strain information in samples
菌株名称 | 来源编号 | |
大肠埃希氏菌 | E. coli | ATCC 8739 |
肺炎克雷伯氏菌 | Klebsiella pneumoniae | ATCC 13883 |
金黄色葡萄球菌 | Staphylococcus aureus | ATCC 25923 |
蜡样芽孢杆菌 | Bacillus cereus | DM 423 |
试剂:氯化钠(NaCl)购自国药集团化学试剂有限公司,分析纯;结晶紫中性红胆盐琼脂(VRBA)、结晶紫中性红胆盐MUG琼脂(VRBA-MUG)等培养基购自北京陆桥技术有限责任公司。所有培养基和试剂均验证合格且在有效期内。
1.2 方法
1.2.1 样品制备
按照参试指导书,用60 mL无菌生理盐水再水化样品制备成60 mL食品样品,因样品数量原因,本试验取25 mL水化好的样品置于225 mL无菌生理盐水中,制备成1:10的样品均液作为评定试验的样品。
1.2.2 样品测定
移取25 mL样品于225 mL生理盐水中,制成1:10的样品均液,进行10倍系列稀释,选择2~3个连续的适宜稀释度的样品均液,每个稀释度接种2个平皿,每皿1 mL样品均液,每皿倾倒15~20 mL VRBA培养基,旋转平皿使培养基与样品充分混匀。大肠菌群检测在培养基凝固后再加入3~4 mL VRBA覆盖平板表层;大肠埃希氏菌检测在培养基凝固后再加入3~4 mL VRBA-MUG覆盖平板表层;平板均置于(36±1)℃恒温培养箱中倒置培养24 h,由同组人员进行10次重复测定。同时用生理盐水作空白对照。
1.2.3 结果计数
大肠菌群计数选取菌落数在15~150 CFU之间的平板进行典型菌落和可疑菌落计数,最低稀释度平板低于15 CFU的记录具体菌落数。大肠埃希氏菌选取菌落数在10~100 CFU之间的平板,暗室中360~366 nm波长紫外灯照射下计数发浅蓝色荧光的菌落。
2 结果与分析
2.1 不确定度的主要来源分析
除了确认试验不一样以外,大肠菌群与大肠埃希氏菌检测过程基本一致,分析大肠菌群和大肠埃希氏菌的不确定度来源主要有单次样品检测产生的不确定度和重复检测过程中产生的不确定度,单次检测产生的不确定度由稀释引入的测量不确定度u(d)、加样至平板引入的测量不确定度u(J)组成。其他诸如样本储存条件、培养基配置时间、灭菌条件及用量等因素由于无法估量且贡献较小,在此忽略不计[9-10]。不确定度来源分析如图1所示。
2.2 数据模型
依据GB 4789.3-2016中第二法,单次检测大肠菌群Y值,计算为式(1)。
 (1)
(1)
式(1)中,Y为样品中大肠菌群菌落数; 为某一稀释度典型菌落和可疑菌落总数;A为某一稀释度鉴定为阳性的菌落数;B为某一稀释度用于鉴定试验的菌落数;D为稀释倍数。
为某一稀释度典型菌落和可疑菌落总数;A为某一稀释度鉴定为阳性的菌落数;B为某一稀释度用于鉴定试验的菌落数;D为稀释倍数。
本评定试验中样品菌株添加信息已知,所有VRBA上的菌落形态均为典型,且均为大肠菌群,因此不做确认试验,并可简化该模型为
 (2)
(2)
式(2)中,Y为菌落总数; 为某一稀释度检测结果的平均数;D为稀释倍数。
为某一稀释度检测结果的平均数;D为稀释倍数。
依据GB 4789.38-2012中第二法,大肠埃希氏菌单次检测结果也为式(2)。大肠菌群和大肠埃希氏菌检测过程引入的不确定度由样品单次检测过程引入的不确定度u(Y)和重复检测过程引入的不确定度u(R)组成。
2.3 不确定度评定
2.3.1 样品稀释中引入的不确定度评定
样品稀释中产生的不确定度主要由样品稀释引入,为B类不确定度。移取25 mL样品添加至225 mL生理盐水中制成1:10的样品均液;后续制备1:100、1:1000的样品均液时,移取1 mL样品至9 mL生理盐水管中制成。
(1)用移液管量取25 mL样品引入的不确定度。为方便进行灭菌和包装,本实验室采用了同一根10 mL A级分度移液管进行3次移液,分别移取2次10 mL和1次5 mL样品置于225 mL的无菌 生理盐水瓶中。移取10 mL引入的不确定度 u(V1)主要包括移液管容量允许误差引入的体积不确定度u(V1-MPE)、量具校准时与使用时温度差异引入的体积不确定度u(V1-t)。
①根据JJG 196-2006《常用玻璃量器》[11]的要求,10 mL A级分度移液管容量允许误差是±0.05 mL,取均匀分布,故u(V1-MPE)=0.05 mL / ≈0.0289 mL。
≈0.0289 mL。
②温度差异为5℃;水溶液的膨胀系数约为2.1×10-4℃-1,u(V1-t)=10 mL×5℃×2.1×10-4℃-1=0.0105 mL。
③合成u(V1),u(V1)= ≈0.0307 mL,实际量取10 mL,urel(V1)=u(V1)/10 mL=0.00307 mL。
≈0.0307 mL,实际量取10 mL,urel(V1)=u(V1)/10 mL=0.00307 mL。
移取5 mL样品引入的不确定度 u(V2)主要包括移液管容量允许误差引入的体积不确定度u(V2-MPE)、量具校准时与使用时温度差异引入的体积不确定度u(V2-t),u(V2-MPE)=u(V1-MPE)=0.0289 mL,u(V2-t)=5 mL×5℃×2.1×10-4℃-1=0.00525 mL,合成u(V2)=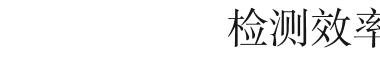 ≈0.0294 mL,实际取用量5 mL,urel(V2)=u(V2)/5 mL=0.00587。
≈0.0294 mL,实际取用量5 mL,urel(V2)=u(V2)/5 mL=0.00587。
(2)用量筒量取225 mL生理盐水引入的不确定度u(V3)。用分度值为5 mL的量筒量取225 mL生理盐水,引入的不确定度主要由量筒容量允许误差引入的不确定度和量具校准时与使用时温度差异引入的体积不确定度组成,250 mL量筒容量允许误差为±1.0 mL,温差为5℃,取均匀分布,计算方法同2.3.1中(1)所述,结果见表2。
(3)制备1:100、1:1000的样品均液引入的不确定度。制备1:100、1:1000的样品均液时,均用1 mL A级移液管移取1 mL加入9 mL的生理盐水管中,9 mL的生理盐水管用10 mL的A级移液管移取9 mL生理盐水完成。移液管移取1 mL和用10 mL分装9 mL的生理盐水管引入的不确定度均由移液管容量允许误差引入的体积不确定度、量具校准时与使用时温度差异引入的体积不确定度组成。1 mL的A级移液管容量允许误差为±0.008 mL,10 mL A级分度移液管的容量允许误差为±0.05 mL,取均匀分布,计算方法同2.3.1中(1)所述,结果见表2。
表2 逐级稀释过程中引入的测量不确定度
Table 2 The measurement uncertainty in the process of step dilution
稀释比例 | 使用玻璃器具 | 移取体积 (mL) | 不确定度 |
1:10 | 250 mL的量筒 | 225 | u rel ( V 3 ) = 0.00277 |
1:100 | 10 mL A级移液管 | 9 | u rel ( V 5 ) = 0.00338 |
1:1000 | 10 mL A级移液管 | 9 | u rel ( V 5 ) = 0.00338 |
大肠菌群和大肠埃希氏菌稀释步骤相同,且检测结果均在稀释比例为1:100上,在稀释过程中主要由制备1:10及制备1:100的样品均液稀释过程中引入不确定度组成,则稀释过程中相对标准不确定度
urel(d)=
≈0.00974
2.3.2 样品加样引入的不确定度评定
一般情况下,肉眼观察结果在选择性分离平板上的菌落清晰可见,平皿上菌落数的不确定度可忽略不计。样品加样过程中分别以1 mL的加样体积接种2块选择性分离平板,引入的不确定度u rel(J)主要包括由2次移取1 mL引入的不确定度组成。移取1 mL稀释液使用1 mL的A级移液管,移取体积为1 mL,引入的不确定度u rel(J1)=u rel(V4)=0.00474,则u rel(J)= ≈0.00670。
≈0.00670。
2.3.3 标准不确定度的合成
单次检测过程中,大肠菌群和大肠埃希氏菌操作一致,稀释过程一致,引入的标准不确定度u rel(Y)相等,由稀释过程引入的相对标准不确定度u rel(d)和样品加样时引入的相对标准不确定度u rel(J)组成,u rel(Y) = ≈0.0118。
≈0.0118。
2.3.4 样品重复测量的不确定度u(R)
实验人员在一定时间内进行10次重复检测操作,评定其标准差和标准不确定度,做A类测量不确定度的预评定,大肠菌群检测结果见表3,大肠埃希氏菌检测结果见表4。由于检测结果的发散性较大,因此,以菌落数的对数值计算测量不确定度。
大肠菌群检测中,选择菌落数在15~150 CFU之间的稀释度平板进行计数,该试验选择稀释度为10-2的平板进行结果报告,若同一稀释度2个平板计数结果均在要求范围内,则有2个结果参与单次检测结果计算(见表3中序号1、2、3、5、7、9、10),若同一稀释度只有1个平板计数结果在要求范围内,则取该结果进行计算(见表中序号8),若所有稀释度结果都不在范围内,则取最接近于15 CFU或150 CFU的平均菌落数乘以稀释倍数计算(见表3中序号4、6)。同一样品制备10份稀释液,重复检测10次,由表3数据,根据贝塞尔公式计算大肠菌群合成标准不确定度u(Rc),见式(3),自由度v = (10-1) =9。
u(Rc) = ≈0.0495 (3)
≈0.0495 (3)
大肠埃希氏菌检测中,选择菌落数在10~100 CFU之间的稀释度平板进行计数,该试验选择稀释度为10-2的平板进行结果报告,序号为1的2个结果均不在范围内,选择最接近范围的10-2稀释度平板上的数据报告结果,序号为3、5、10中2个平板上有1个平板上的结果不在范围内,选择在范围内的结果进行计算。同一样品制备10份稀释液,重复检测10次,由表4数据,根据贝塞尔公式计算合成标准不确定度u(RE.coli),见式(4),自由度v = (10-1) =9。
u(RE.coli) = ≈0.0496 (4)
≈0.0496 (4)
2.3.5 合成标准不确定度
测定过程中的标准不确定度uc(YR)主要由单次检测引入的测量不确定度urel(Y)和重复测量引入的测量不确定度urel(R)组成,则大肠菌群检测过程中的标准不确定度uc(YR-c)计算,见式(5)。
uc(YR-c) =
= ≈0.0509 (5)
≈0.0509 (5)
同理,大肠埃希氏菌检测过程中的标准不确定度uc(YR-E.coli)计算,见式(6)。
uc(YR-E. coli) =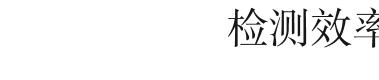
= ≈0.0510 (6)
≈0.0510 (6)
2.3.6 结果报告
根据JJF 1059.1-2012,取置信概率p =95%,自由度v =10-1时,由t分布表得k =2.26,则该样品大肠菌群检测的扩展不确定度Uc = uc(YR-c)∙k =0.0509×2.26 ≈0.115。同理,置信概率p =95%,自由度v =10-1,k =2.26时,该样品大肠埃希氏菌检测的扩展不确定度为UE.coli =uc(YR-E.coli)∙ k =0.0510×2.26 ≈0.115。
以序号为1的检测结果为例,大肠菌群检测结果Yc =3300 CFU/mL,取对数lgYc =3.519,考虑不确定度应为3.519±0.115,取反对数,检测结果报告YR-C的取值范围为2500~4300 CFU/mL;大肠埃希氏菌检测结果YE.coli =900 CFU/mL,取对数lgYE.coli =2.954,考虑不确定度应为2.954±0.115,取反对数,检测结果报告YR-E.coli的取值范围为690~1200 CFU/mL。
3 结论与讨论
3.1 评定食品微生物测量不确定度的重要性
食品中微生物指标是影响食品安全的重要指标,同时《食品安全国家标准 散装即食食品中致病菌限量》(GB 31607-2021)[12]、《食品安全国家标准 预包装食品中致病菌限量》(GB 29921-2021)[13]中规定了散装即食及预包装食品中致病菌指标及其限量要求,覆盖了大多数食品。大肠菌群、大肠埃希氏菌作为判断食品是否受到粪便等污染的重要卫生指标,很多产品标准均对其限量要求进行了规定,且当检测结果在标准限量附近时,需要借助不确定度来进行检测结果的符合性判定。本研究探讨了GB 4789.3-2016、GB 4789.38-2012中第二法检测大肠菌群、大肠埃希氏菌检测过程中引入的不确定度来源,可以有效掌握食品微生物检验方法不确定度的评定,严格控制食品微生物检测过程中各不确定度贡献分量,有效降低不确定度,以此得到客观数据,确保检测方法的准确性,提高检测数据的有效性、可靠性、科学性、公正性[14-17]。
3.2 不确定度来源分析
本研究以大肠菌群、大肠埃希氏菌为例,探讨分析食品微生物检测引入的不确定度来源,主要由样品制备、样品稀释、样品加样及重复性试验引入的测量不确定度组成,重复性试验引入的不确定度涵盖了测试环境、培养温度、培养时间、样本均匀性、结果计数等。除了文中列出的不确定度分量以外,样品的储存、样品的均质、培养基配制时间、培养基灭菌条件、培养基用量等分量不便于计算,且对不确定度贡献较小,忽略不计。但是作为不确定度的来源,应严格按照标准进行实验操作,可将相关分量条件制定为作业指导书,最大程度减小此类分量带来的不确定度。就本实验来说,使用的培养基均按照作业指导书进行验收,按照说明进行配置和灭菌;高压灭菌锅定期由有资质的服务商进行校准,每次灭菌用化学指示卡进行监控,每季度用生物指示剂进行灭菌效果监测;培养箱定期进行校准和清洁消毒,并有效利用温度校准偏差因子,每日监控温度。对于此类无法估量且贡献较小的分量,实验室应进行有效控制,尽可能地降低不确定度的引入[16-19]。
本研究中大肠菌群检测及大肠埃希氏菌检测由重复性引入的不确定度占比u(R):uc(YR)均约为97%,检测过程中不确定度主要贡献来源于重复性检测引入的不确定度,由单次检测过程中的样本取样、稀释过程及加样过程引入的不确定度较小,考虑到食品微生物检测全过程,更全面分析不确定度来源,还研究分析了单次检测引入的测量不确定度。
3.3 固体样本制备过程中引入的测量不确定度分析
本研究以能力验证样品(液体)开展不确定度来源分析,样本制备引入的不确定度计算包含于稀释过程中。食品微生物检测过程中很多样品为固体样品,在样品制备时,由电子天平称量25 g样品引入的不确定度定度u(M)主要来自天平的最大允许误差MPE。一般实验室采用Ⅱ级电子天平进行称量,实际分度值d=0.01 g,检定分度值e=10 d=0.1 g,根据《电子天平》(JJG 1036-2008)[20],准确级为Ⅱ级的电子天平的最大允许误差MPE=±0.5e=±0.05 g,根据JJF 1059.1-2012,最大允许误差导致的不确定度取均匀分布,因此u(M)=0.05 g/ ≈0.0289g,urel(M)=u(M)/25g≈0.00116。用量筒量取225 mL的生理盐水引入的测量不确定度计算同2.3.1中(2)所述。
≈0.0289g,urel(M)=u(M)/25g≈0.00116。用量筒量取225 mL的生理盐水引入的测量不确定度计算同2.3.1中(2)所述。
3.4 不确定度模型的建立
本研究测量不确定度来源从单次检测及重复试验过程进行分析,建立数学模型 ,考虑了稀释、加样等过程对不确定度的贡献,该模型适用于食品微生物定量检测过程中测量不确定度的分析。由于食品微生物检测过程中,微生物是活的物质,不同的菌落之间有互生和拮抗作用,且不同的微生物有不同特性,在不同样品、不同部位中均匀度存在差异,检测结果数据发散性较大,样品中目标菌含量数量级越高,发散性越大,因而微生物污染的样品分析结果以宏量为主,直接按照贝塞尔公式计算标准差不太合理,因此本研究取检测结果的对数计算合并样本标准差[21-23]。
,考虑了稀释、加样等过程对不确定度的贡献,该模型适用于食品微生物定量检测过程中测量不确定度的分析。由于食品微生物检测过程中,微生物是活的物质,不同的菌落之间有互生和拮抗作用,且不同的微生物有不同特性,在不同样品、不同部位中均匀度存在差异,检测结果数据发散性较大,样品中目标菌含量数量级越高,发散性越大,因而微生物污染的样品分析结果以宏量为主,直接按照贝塞尔公式计算标准差不太合理,因此本研究取检测结果的对数计算合并样本标准差[21-23]。
参考文献
[1]许晓琳, 汪红梅, 何芙蓉, 等. 食品和水中大肠埃希氏菌验证方法的比较[J]. 食品安全质量检测学报, 2020, 11(8): 2617-2620.
[2]冯立玲, 罗军昆, 吴艳, 等. 食品中大肠菌群检测人员差异性分析与讨论[J]. 轻工科技, 2020, 36(9): 35-36.
[3]马雪婷, 冯雨欣, 耿冰雨, 等. 食源性大肠杆菌危害及其检测技术研究进展[J]. 广东化工, 2021, 48(22): 191-193.
[4]邵志勇, 陈夏冰, 何斌, 等. 大肠杆菌病的研究进展[J]. 养殖与饲料, 2021, 20(8): 5-7.
[5] JJF 1059.1-2012测量不确定度评定与表示[S]. 北京: 中国标准出版社, 2013.
[6] RB/T 151-2016食品微生物定量检测的测量不确定度评估指南[S]. 北京: 中国标准出版社, 2016.
[7] GB 4789.3-2016食品安全国家标准 食品微生物学检验 大肠菌群计数[S]. 北京: 中国标准出版社, 2017.
[8] GB 4789.38-2012食品安全国家标准 食品微生物学检验 大肠埃希氏菌计数[S]. 北京: 中国标准出版社, 2012.
[9]郭丽艳. 能力验证样品中霉菌和酵母检测结果的不确定度评定[J]. 食品安全质量检测学报, 2019, 10(18): 6088-6092
[10]杨燕, 李琼琼, 宋光艳, 等. 能力验证乳粉中乳酸菌计数不确定度的评定[J]. 食品安全质量检测学报, 2016, 7(7): 2747-2750.
[11] JJG 196-2006 常用玻璃量器[S]. 北京: 中国计量出版社, 2007.
[12] GB 31607-2021食品安全国家标准 散装即食食品中致病菌限量[S]. 北京: 中国标准出版社, 2022.
[13] GB 29921-2021 食品安全国家标准 预包装食品中致病菌限量[S]. 北京: 中国标准出版社, 2021.
[14] 翟洪稳, 范素芳, 王娟, 等. 测量不确定度在食品检验中的应用及进展[J]. 食品科学, 2021, 42(5): 314-320.
[15] 胡婕, 毛林夏, 李昱贤, 等. 面包中霉菌检测结果的测量不确定度评定[J]. 中国口岸科学技术, 2021, 3(7): 95-99.
[16] 吴卫玲, 胡同静, 钟君杰, 等. 食品中蜡样芽孢杆菌平板计数的不确定度评定[J]. 中国调味品, 2016, 41(12): 118-121.
[17] 游元丁, 赵阳,林雪丹, 等. 食品中金黄色葡萄球菌测量不确定度评定[J]. 食品安全质量检测学报, 2021, 12(6): 2468-2473.
[18] 赵琪, 甄珍. 单核细胞增生李斯特氏菌MPN法结果测量不确定度评定[J]. 中国口岸科学技术, 2022, 4(5): 77-81.
[19] 岳苑, 马桂娟. 全脂乳粉中菌落总数的测量不确定度评定[J]. 食品与发酵科技, 2018, 54(3): 124-126.
[20] JJG 1036-2008电子天平[S]. 北京: 中国计量出版社, 2008.
[21] 杨燕, 李琼琼, 宋光艳, 等. 能力验证乳粉中乳酸菌计数不确定度的评定[J]. 食品安全质量检测学报, 2016, 7(7): 2747-2750.
[22] 高阳, 刘丹.干枸杞浆果菌落总数测定结果的测量不确定度评价[J]. 工业微生物, 2020, 50(6): 30-32.
[23] 徐丽萍, 商晓春, 舒青青. 质控金黄色葡萄球菌计数结果不确定度评定[J]. 中国卫生检验杂志, 2011, 21(3): 654-656.







