CopyRight 2009-2020 © All Rights Reserved.版权所有: 中国海关未经授权禁止复制或建立镜像
多环芳烃毒理学及累积暴露风险评估研究进展
作者:王璐 董洁 李菊 侯颖烨 曾广丰 陈文锐 蔡翠玲 谢建军
王璐 董洁 李菊 侯颖烨 曾广丰 陈文锐 蔡翠玲 谢建军
多环芳烃(polycyclic aromatic hydrocarbons,PAHs),由两个或两个以上苯环以稠环和非稠环方式连接而成的持久性有机污染物,分布广泛,能够通过呼吸、皮肤、吞食等途径进入人体,具有致畸、致癌、致突变等毒性效应[1]。美国环保署(US EPA)优先控制的PAHs有16种,其中7种被我国国家环境保护部列入“中国环境优先控制污染物”的黑名单[2],见表1。国际癌症研究机构将BaP归为Ⅰ类致癌物,BaA、Chr、BbF归为2B类致癌物。我国《化妆品安全技术规范》(2015)规定,NaP、Chr等10种PAHs不得在化妆品中检出。GB 2762-2017《食品污染物限量》要求,谷物及其制品,熏、烧、烤肉类,熏、烤水产品中BaP的最大残留限量为5.0 μg/kg,油脂及其制品为10 μg/kg。欧盟标准则更为严格,增加了婴幼儿食品的最大残留限量,并对BaP、BaA、BbF和Chr 4种PAHs的总含量限量作了要求,如传统烟熏肉和烟熏肉制品中4种PAHs含量的最大限量为50 μg/kg。
人类接触PAHs的途径主要包括:(1)接触被污染的环境,如汽车尾气、吸烟和燃料(如木材、煤炭和石油产品)不完全燃烧等造成的大气污染;(2)接触含有煤烟、焦油或原油产品的土壤、水体等[3];(3)食用高温烹饪的食物[4];(4)接触不合格的玩具等消费品、职业暴露等。PAHs各同系物结构相似,以混合物形式存在,若同时暴露,可能表现出协同或拮抗的作用[5],探讨研究PAHs累积风险评估,对指导人们避免过多暴露于PAHs环境下具有实际意义。目前,国内外对于PAHs的累积风险评估多集中在环境和食品领域,PAHs累积毒性效应的问题得到初探。本文将对PAHs的毒理学及各领域累积风险评估情况进行综述,总结归纳了评估模型使用中的难点和问题,并提出建议,期望为其后续开展相关研究提供参考。
1 多环芳烃的物理化学特性
PAHs 极难溶于水,易溶于有机溶剂,化学性质非常稳定,分为增环结构和周环合并结构两大类。一般来说,随着环数或角度的增加,疏水性相应增大,在环境中的持久性更强,比如具有角度结构的Phe比直线型的An在环境中更加稳定[6]。
2 多环芳烃毒物代谢动力学特征
2.1 吸收
2.1.1 经口吸收
大鼠口服一定剂量PAHs后,BaP、Dba和Pyr的吸收率可达到30%~90%,并且吸收率高度依赖于PAHs在动物或人体内的溶解度,摄入的食物若油脂度较高则能促进吸收,若为水或固体食物则会抑制吸收[3]。此外,有研究表明,Flu、Pyr和BaA在胃肠道吸收速度最快,1~2 h后血液中的浓度就可以达到峰值[7]。Foth等[8]提出BaP的口服生物利用度为40%。
2.1.2 经皮肤吸收
通过体内、体外实验研究发现,BaP溶解在丙酮中时,皮肤吸收率达到50%。结合BaP皮肤吸收的动物试验数据库,大多数研究使用20%的估计值,原因是与丙酮为载体时相比,皮肤从汗液中吸收的BaP可能更低[9]。
2.1.3 呼吸吸入
随呼吸吸入PAHs是导致肺癌多有发生的主要原因之一。有研究称,空气中94%的PAHs会吸附在粒径小于2.99 μm的大气颗粒上,BaP的浓度每100 m3增加0.1 μg,肺癌死亡率增加5%[10],焦化厂附近人群因吸入PAHs所致肺癌的总体归因分数超过了44% [11]。
2.2 分布
PAHs脂溶性强,进入生物体内后会迅速溶于脂肪,不易被分解排出。将贻贝置于Phe水溶液(250 μg/L、500 μg/L和1000 μg/L)中暴露11 d后(吸收实验),再转入清水中清除11 d(清除实验),测得Phe的吸收速率显著高于消除速率,实验说明Phe在贻贝体组织中具有生物累积效应[12]。
2.3 生物转化
PAHs生物转化包括阶段Ⅰ(氧化反应)、阶段Ⅱ(结合反应)和阶段Ⅲ(转运反应)。以BaP为例,进入生物体内的BaP,一部分经过几种细胞色素P450(CYPs)中的亚型代谢活化,生成具有强致癌活性的亲电子环氧化物;另一部分代谢产物与谷胱甘肽(GSH)、葡萄糖醛酸(UDPGA)等结合形成无毒的水溶性物质,经ABC蛋白转运排出体外,达到解毒的作用,如图1所示。
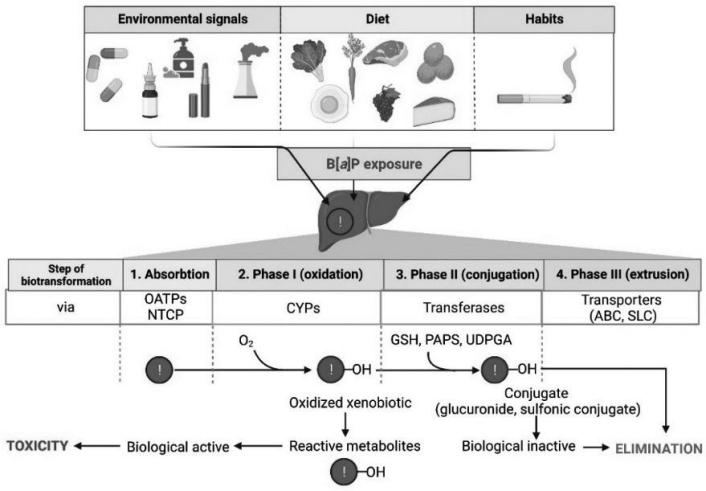
图1 BaP的生物转化途径[13]
Fig.1 Steps in the biotransformation of BaP[13]
3 多环芳烃的毒性
3.1 致癌性
收集涉及PAHs的文献发现,若PAHs暴露在人群中,则会增加患肺、胃、喉、肾、前列腺、乳腺和结肠癌的风险[14-15]。吸入的PAHs会沉淀在肺泡上,残留肺部数年,导致肺癌[16]。皮肤暴露,可诱发不同品系小鼠的良性和恶性皮肤肿瘤,职业暴露会导致肺癌、皮肤癌或膀胱癌[17]。Kroese等[18]研究口服BaP与肿瘤发生率的关系,雄性和雌性Wistar大鼠(n=52/组)每周5 d,每天喂服 0 mg/(kg·bw)、3 mg/(kg·bw)、10 mg/(kg·bw)或30 mg/(kg·bw)BaP,连续104周后,发现大鼠肝脏、前胃、耳道、口腔、皮肤、肠道(仅雄性)、肾脏和雌性乳腺、食管的肿瘤发生率呈剂量依赖性增加。Cioroiu等[19]评估了罗马尼亚31例肺癌患者肺部的PAHs,检测到15种PAHs,其中BaA、An、Flu、BaP、BbF、BkF是主要致癌成分,首次证明肺癌患者肺部存在高浓度的致癌物质。
3.2 致畸性
流行病学研究表明,增加PAHs暴露会对生殖过程造成干扰,如抑制胎儿生长,影响胎儿的牙齿发育甚至神经发育等[20-21]。群体分析也表明,暴露于BaP的小鼠显示胎儿体重、长度和头围减少,出生缺陷[22]。Ye等[23]研究了BaP对人滋养层细胞和小鼠流产的影响,发现BaP剂量从0.1 mg/kg开始,异常小鼠胎儿的发生率呈剂量依赖性,当剂量达2 mg/kg时,胎儿停止发育。
3.3 致突变性
PAHs的二氢二醇衍生物是终致癌物,具有亲电性,可与DNA等细胞内大分子共价结合,DNA加合物的形成是癌变早期的一个指标,可能导致基因突变、DNA链断裂或染色体畸变等[24]。Kroese等[18]研究大鼠中口服0.1 mg/kg BaP,用32P标记DNA加合物,发现DNA加合物存在于肿瘤发生的组织(前胃和肝脏)。Hakura A等[25]用突变试验lacZ转基因小鼠检测连续5 d口服125 mg/(kg·bw)的BaP,体内突变分析表明,所有器官的突变频率都明显高于自发频率,突变频率最高的是结肠,其次是前胃>脾脏>腺胃、肝和肺。
3.4 其他毒性
人若增加与PAHs的接触,还可导致生育能力下降,后代生殖障碍、卵巢功能衰竭、基因毒性、胎儿免疫功能损害、动脉硬化等[26-29]。在一项接触BaP的儿童患病调查中还发现15%的儿童在肘部长过湿疹,10%的儿童患过风疹,20%的儿童经常打喷嚏、流鼻涕或鼻塞,15%的儿童流过鼻血,25%的儿童感觉呼吸困难,42%的儿童经常干咳,60%的儿童经常患感冒[30]。
综上所述,大量的体内和体外实验证实增加接触PAHs会导致致癌、致畸、致突变及其他毒性。但PAHs的不同暴露量对人体造成健康危害的程度和机理尚未明确,所以对PAHs的健康风险评估的研究具有十分重要的意义,能够指导人类避免过多暴露在含有PAHs的环境中。
4 累积暴露风险评估方法
累积暴露风险评估方法主要有危害指数法(HI)、累积风险指数法(CRI)、相对效能因子法(RPF)、毒性分离点指数法(PODI) 、联合暴露阈值法(MOE)和毒性当量因子法(TEF)等。HI法是各组分危害系数(HQ)的总和,适用于毒性相似且具备明确剂量-反应关系的化学物[31],此法也是US EPA研究开发的方法。CRI值与HI值互为倒数,CRI法与不确定系数(UF)紧密相关。RPF法是要求各组分毒性作用靶点、暴露途径和持续时间具有相似性,所有组分剂量相加后,每种组分的效能比不变[32]。PODI法是将每个组分的暴露量(EXP)与其POD的比值相加。MOE则是PODI值的倒数,主要适用于遗传毒性致癌物的风险评估[33]。BaP当量因子法是假定BaP的TEF为1,通过其他PAHs对人体的危害性与BaP比较得到各组分TEF值,各组分浓度和其TEF值相乘,再累乘,得到毒性等效剂量(TEQ)[34],该法便于比较不同PAHs风险大小。以上6种累积风险评估方法信息见表2。
终生致癌风险法(ILCR)是健康风险评价的一种方法,在累积风险评价过程中,通常与上述6种方法联合使用,表示在一定时间内(终生)暴露于一定剂量的致癌污染物而产生的超过正常水平的癌症发病率。当ILCR<10-6时,认为是可接受,当ILCR值>10-4时,表示存在严重危险,当10-6<ILCR<10-4时,则存在潜在致癌风险[35]。
5 多环芳烃累积风险评估的研究现状
PAHs复杂多样且相互之间可能存在拮抗和协同作用,累积暴露对人体带来的健康风险受到国内外学者的广泛关注。PAHs风险评估方面的研究主要涉及环境、食品、玩具、职业暴露等领域。
5.1 环境
5.1.1 大气
PAHs是大气中常见的污染物,其浓度受森林火灾、有机物不完全燃烧等方面的影响。吴明红等[36]使用TEF法联合ILCR法研究上海近郊PM10和PM2.5中16种PAHs的致癌风险,其TEQ总量分别为5.4和4.1 ng/m3,致癌风险按年龄段为成人>儿童>青年,按性别为女性>男性,所有年龄段的终生致癌风险均高于10-6,存在一定的健康风险,提出需从源头对可吸入颗粒物的排放浓度进行有效控制的建议。Mohammad H等[37]评估德黑兰大气PM10颗粒结合PAHs的浓度、分布和来源,风险分析表明,吸入途径平均和最大ILCR值分别为7.85 × 10-6和16.78 × 10-6,存在潜在致癌风险。李文静等[38]利用HI结合ILCR模型评估北京市朝阳区居民经吸入接触PM2.5中16种PAHs的暴露风险,发现PM2.5中的PAHs以4~6环为主,BaP的年平均浓度为0.90 ng/m3,总致癌性风险为1.2×10-6,具有潜在致癌性。
5.1.2 土壤
原珑苗[39]比较了不同接触方式接触河西走廊土壤,18种PAHs的致癌风险,发现经口摄入>呼吸吸入>皮肤接触,人群中儿童致癌风险最高,其次是成年人。Che K等[40]比较了TEF和HI模型对衡水地区9座变电站土壤中16种PAHs暴露健康风险评估结果,发现TEF评估会导致风险熵偏小,不适用于非致癌物质的风险评价。从环境风险控制角度考虑,HI模型更适用于污染土壤的健康风险评价。Luo Q等[41]基于蒙特卡罗模拟的概率风险评价模型定量评估了沈阳地区表层土壤16种PAHs的健康风险,发现BaP是致癌风险的最主要贡献物质,Pyr、Flu和Phe是非致癌风险的最主要贡献物质。
5.1.3 水
评估水体中PAHs的健康风险,多采用HI和ILCR模型联用法。刘阿静等[42]对兰州市3个区的饮用水源中16种PAHs进行分析测定,采用HI和ILCR模型进行人体健康风险评价,结果发现水体中非致癌风险HI值(直接摄入途径)为0.47×10-8~6.00×10-7,HI值(皮肤接触途径)为2.10×10-8~2.71×10-6,致癌风险ILCR值(直接摄入途径)为0.18×10-9~1.05×10-9,ILCR值(皮肤接触途径)为0.24×10-9~1.40×10-9,均低于US EPA推荐的阈值,表明兰州市3个区饮用水中PAHs潜在的健康风险极低。李海燕等[43]同样采用此法对珠江口表层水中15种PAHs进行健康风险评估,结果发现BaP导致的饮水途径健康风险最高,存在潜在的健康风险,需要重点控制和管理。
5.2 食品
通过膳食暴露,接触PAHs占总暴露的50%~70%[44]。分析原因为烟熏、烧烤、油炸等加工肉制品在高温加热时,脂肪组织发生热解,或接触不完全燃烧物,从而产生PAHs。因此,食品中PAHs的风险评估多以油炸、油脂类为主。Cheng L等[45]采用MOE法对120份油炸食品中15种PAHs带来的健康风险进行初步评估,发现人群经油炸食品摄入PAHs在设定暴露情况下的健康风险较低。杨晓倩等[46]采用点评估法联合MOE法对济南市居民膳食油脂中 PAHs 暴露风险开展定量评估,结论是成人、青少年、儿童在平均暴露水平以及成人和青少年高暴露水平时,健康风险较低,儿童在高暴露水平时,存在一定的致癌风险。Asamoah等[47]对来自阿克拉受污染地区的加纳妇女母乳中7种PAHs的致癌和诱变风险的评估,采用的是TEF法。
此外,环境中的PAHs也可能会通过富集转移进入蔬菜水果、水产品和饮用水中。张会敏等[48]通过TEF联合ILCR模型对南宁市不同人群食用瓜类蔬菜引起的健康风险进行评估,结果显示食用整果引起的ILCR值在1.48×10-6~7.87×10-5范围内,存在潜在致癌风险。Seyedeh 等[49]测定了1800份伊朗橄榄样品(6个不同种植区的20个品种)中16种PAHs的含量,研究结果显示,PAHs的ILCR和MOE值存在二级风险。
5.3 玩具
府雨月等[50]对苏州地区流通市场销售的儿童玩具和用品进行了18种PAHs含量的检测,采用MOE法得到最大暴露量为0.116 μg/kg·d,低于参考剂量0.49 μg/kg·d,说明发生伤害的概率较低。
5.4 职业暴露
职业暴露PAHs多发生在铝生产、煤液化、煤焦油蒸馏、木材浸渍、烟囱和发电厂。卢城德等[51]采用TEF、ILCR和预期寿命损失法评估煤焦油沥青职业接触导致的PAHs 职业健康风险,发现该场所2/3的工人存在较高致癌风险,工人PAHs暴露导致的预期寿命损失是同一地区正常成人的37.5~1459倍。 Petit等[52]使用大气BaP水平作为替代值,评估了不同行业与PAHs暴露相关的肺癌风险发生率,共分析了93个暴露组,9个行业分支,30%的暴露组高于10-4。Saleh等[53]评估了在麦加居住的职业暴露组和未暴露组吸入的空气样本中PAHs的差异,有职业暴露的工人(如巴士和卡车司机、警察等)检测到BaP的平均浓度为(0.082±0.032)ng/m3 ,而未暴露组的平均浓度为(0.044±0.006)ng/m3 ,还发现BaP暴露的增加与血清p51和p21蛋白水平呈正相关,而这些蛋白水平被认为与肿瘤的进展、侵袭和转移有关。
6 结语
综上所述,我国对PAHs累积风险评估多采用MOE、TEF、HI联合ILCR模型,CRI、PODI和RPF模型应用较少,并且风险评估技术都还处于发展阶段,评估过程中参数的不确定性对评估结果存在制约。现阶段存在问题有以下几方面:(1)PAHs各同系物的毒理学参数与各组分之间的相互作用在选择风险评估模型中起着至关重要的作用,但目前,部分PAHs的毒理学参数缺失,各组分之间相互作用的研究较少,造成选择风险评估模型难度大;(2)PAHs的累积风险评估缺乏全面性,目前研究主要集中在环境和食品领域;(3)某些累积风险评估技术缺乏国际统一的风险评判标准,这一现象使其应用受限。
基于以上研究提出如下建议:(1)发展针对PAHs的毒理学及各同系物间相互作用的研究,以完善PAHs风险数据库,有利于PAHs的累积风险模型的构建;(2)继续加大环境、食品领域及食品接触材料、化妆品、消费品或其他领域接触的PAHs研究,使其更具全面性;(3)尽快统一国内乃至国际风险评判标准,建立更加精准的评估模型和方法,以期让PAHs的累积风险评估工作更具科学性与规范性。以上建议期望为后续开展PAHs风险评估研究提供参考,为国家制定PAHs风险管控措施提供更科学、准确的PAHs分析评估数据和结论,从而保障人民群众身体健康和环境的友好和谐。
参考文献
[1] Jegannathan P, Termeh Y A, Karim M S A, et al. Enhancement of graphene quantum dots based applications via optimum physical chemistry: A review[J]. Biocybern Biomed Eng, 2018, 38(3): 481-497.
[2] Gao P, da Silva E, Hou L, et al. Human exposure to polycyclic aromatic hydrocarbons: Metabolomics perspective[J]. Environ Int, 2018, 119: 466-477.
[3] West J E, Carey A J, Ylitalo G M, et al. Polycyclic aromatic hydrocarbons in Pacific herring embryos exposed to creosotetreated pilings during a piling removal project in a nearshore marine habitat of Puget Sound[J]. Mar Pollut Bull, 2019, 142: 253-262.
[4] Chung S Y, Yettella R R, Kim J S, et al. Effects of grilling and roasting on the levels of polycyclic aromatic hydrocarbons in beef and pork[J]. Food Chem, 2011, 129(4): 1420-1426.
[5] Tarantini A, Maitre A, Lefebvre E, et al. Polycyclic aromatic hydrocarbons in binary mixtures modulate the effificiency of benzo[a]pyrene to form DNA adducts in human cells[J]. Toxicology, 2011, 279(1-3): 36-44.
[6]王震. 辽宁地区土壤中多环芳烃的污染特征、来源及致癌风险[D]. 大连:大连理工大学, 2007.
[7] World Health Organization. Polynuclear aromatic hydrocarbons in Drinking-water[R/OL]. 2003. http://www.doc88. com/p-804578068829.html.
[8] Foth H, Kahl R, and Kahl G F. Pharmacokinetics of low doses of benzo[a]pyrene in the rat[J]. Food Chem Toxicol ,1998, 26(1): 45-51.
[9] Ng K M, Chu I, Bronaugh R L, et al. Percutaneous absorption and metabolism of pyrene, benzo[a]pyrene, and di(2-ethylhexyl) phthalate: comparison of in vitro and in vivo results in the hairless guinea pig[J]. Toxicol Appl Pharm, 1992, 115(2): 216-223.
[10] Velali E, Papachristou E, Pantazaki A, et al. In vitro cellular toxicity induced by extractable organic fractions of particles exhausted from urban combustion sources Role of PAHs[J]. Environ Pollut, 2018, 243: 1166-1176.
[11] Zhang Y X, Tao S, Shen H Z, et al. Inhalation exposure to ambient polycyclic aromatic hydrocarhons and lung cancer risk of Chinese population [J]. PNAS, 2009, 106(50): 21063-21067.
[12] Yakan S D, Henkelmann B, Sch, et al. Bioaccumulation Depuration kinetics and effects of phenanthrene on Mediterranean mussel (Mytilus gallo- provincialis)[J]. J Environ Sci Heal A , 2013, 48(9) : 1037-1046.
[13] Bukowska B, Mokra K, Michałowicz J. Benzo[a]pyrene-Environmental Occurrence, Human Exposure, and Mechanisms of Toxicity[J]. Int J Mol Sci, 2022, 23, 6348.
[14] Amadou A, Praud D, Coudon T D, et al. Risk of Breast Cancer Associated with Long-Term Exposure to Benzo [a]Pyrene (BaP) Air Pollution: Evidence from the French E3N Cohort Study[J]. Environ Int, 2021, 149, 106399.
[15] Korsh J, Shen A, Aliano K, et al. Polycyclic Aromatic Hydrocarbons and Breast Cancer: A Review of the Literature[J]. Breast Care, 2015, 10, 316-318.
[16] Sulong N A, Latif M T, Sahani M, et al. Distribution, sources and potential health risks of polycyclic aromatic hydrocarbons (PAHs) in PM2.5 collected during different monsoon seasons and haze episode in Kuala Lumpur[J]. Chemosphere, 2019, 219: 1-14.
[17] Bosetti C, Boffetta P, and La Vecchia C. Occupational exposures to polycyclic aromatic hydrocarbons, and respiratory and urinary tract cancers:a quantitative review to 2005[J]. Ann Oncol, 2007, 18(3): 431-446.
[18] Kroese E D, Muller J J A, Mohn G R, et al. Tumorigenic effects in Wistar rats orally administered benzo[a]pyrene for two years (gavage studies). Implications for human cancer risks associated with oral exposure to polycyclic aromatic hydrocarbons[J]. Report No. RIVM 658603 010, 2001: 1-138.
[19] Cioroiu B I, Tarcau D, Cucu-Man S, et al. Polycyclic aromatic hydrocarbons in lung tissue of patients with pulmonary cancer from Romania[J]. Chemosphere, 2013, 92: 504-511.
[20] Perera F P, Tang D, Rauh V, et al. Relationships among Polycyclic Aromatic Hydrocarbon–DNA Adducts, Proximity to the World Trade Center and Effects on Fetal Growth[J]. Environ Health Persp, 2005, 113, 1062-1067.
[21] CHio H, Jedrychowski W, Spengler J, et al. International studies of prenatal exposure to polycylic aromatic hydrocarbons and fetal growth[J]. Environ Health Persp, 2006, 114(11): 1744-1750.
[22] Legraverend C, Guenthner T M, Nebert D W. Importance of the Route of Administration for Genetic Differences in Benzo[a]Pyrene-Induced in Utero Toxicity and Teratogenicity[J]. Teratology, 1984, 29, 35-47.
[23] Ye Y, Jiang S, Zhang C, et al. Environmental Pollutant Benzo[a]Pyrene Induces Recurrent Pregnancy Loss through Promoting Apoptosis and Suppressing Migration of Extravillous trophoblast[J]. BioMed Res Int, 2020, 2020, 1-10.
[24] Nishikawa T, Haresaku M, Fukushima A, et al. Further evaluation of an in vivo micronucleus test on rat and mouse skin: results with five skin carcinogens[J]. Mutat Res-Gen Tox En, 2002, 513(1-2): 93-102.
[25] Hakura A, Tsutsui Y, Sonoda J, et al. Multiple organ mutation in the lacZ transgenic mouse (Muta TM Mouse) 6 months after oral treatment (5days) with benzo[a]pyrene[J]. Mutat Res-Fund Mol M, 1999, 426(1): 71-77.
[26] Reddy K P, Girish B P, Reddy P S. Reproductive and Paternal Mediated Developmental Toxicity of Benzo(a)Pyrene in Adult Male Wistar Rats[J]. Toxicol Res-Ger, 2015, 4, 223-232.
[27] Jorge B C, Reis A C C, Stein J, et al. Parental Exposure to Benzo(a)Pyrene in the Peripubertal Period Impacts Reproductive Aspects of the F1 Generation in Rats[J]. Reprod Toxicol, 2021, 100, 126-136.
[28] Fanali L Z, De Oliveira C, Sturve J. Enzymatic, Morphological, and Genotoxic Effects of Benzo[a]Pyrene in Rainbow Trout (Oncorhynchus mykiss)[J]. Environ Sci Pollut R, 2021, 28, 53926-53935.
[29] Heudorf U, Schumann M, Angerer J, e1 a1. Dennal and bronchial symptoms in children: are they caused by PAH containing parquet glue or by passive smoking[J]. Int Arch Occ Env Hea, 2005, 78(8): 655-662.
[30] Wieslaw J, Aleksander G, Agnieszka P, et a1. Prenatal ambient air exposure to polycyclic aromatic hydrocarbons and the occurrence of respiratory symptoms over the first year of life European[J]. Joumal Epidemiol, 2005, 20: 775-782.
[31] Yang G L, Chen C, Wang Q, et al. Construction of risk assessment procedure for combined pesticide residue exposure [J]. Quality and Safety of Agro-products, 2018(3): 12-20.
[32] Reffstruptk. Risk assessment of mixtures of pesticides[J]. Toxicol Lett, 2012, 211: S26.
[33] US EPA. Developing relative potency factors for pesticide mixtures: biostatistical analyses of joint dose response [EB/OL]. [2003-09]. https://nepis.epa.gov/Exe/ZyPURL.cgi?Dockey=2000GU4J.txt.
[34] Nisbeti C T, Lagoy P K. Toxic equivalency factors (TEFs) for polycyclic aromatic hydrocarbons (PAHs)[J]. Regul Toxicol Pharm, 1992, 16(3): 290-300.
[35] Wang W, Huang M J, Kang Y, et al. Polycyclic aromatic hydrocarbons (PAHs) in urban surface dust of Guangzhou, China: status, sources and human health risk assessment[J]. Sci Total Environ, 2011, 409(21): 4519-4527.
[36]吴明红, 陈锣璐, 陈祖怡, 等. 多环芳烃在上海近郊大气颗粒物(PM2.5和PM10) 中的污染特征、来源及其健康风险评估[J]. 上海大学学报(自然科学版), 2014, 20(4): 521-530.
[37] Mohammad H, Masud Y, Ramin N, et al. Characterization and risk assessment of polycyclic aromatic hydrocarbons (PAHs) in urban atmospheric Particulate of Tehran, Iran[J]. Environ Sci Pollut Res, 2016(23): 1820-1832.
[38]李文静, 张美云, 万博宇, 等. 北京市朝阳区大气 PM2.5 中多环芳烃的污染特征及健康风险评估[J]. 职业与卫生, 2021, 37(16): 2235-2242.
[39]原珑苗. 河西走廊土壤中典型持久性有机污染物的污染特征、来源解析及风险评估[D]. 兰州交通大学, 2020.
[40] Che K, Yu J X, Liu K C, et al. Comparative Study of Different Toxicity Evaluation Models on Health Risks assessment of PAHs in soil of typical substation sites[J]. Environl Eng, 2022, 40(1): 128-134.
[41] Luo Q, Gu L Y, Shan Y, et al. Health risk Assessment of polycyclic aromatic hydrocarbons ib urban top soil of shenyang based on monte carlo method[J]. Environ Eng, 2020, 38(5): 196-222.
[42]刘阿静, 王波, 薛鑫, 等. 饮用水中 16 种多环芳烃的分布特征及人体健康风险评估[C]. 中国环境科学学会2019年科学技术年会, 2019.
[43]李海燕, 赖子尼, 曾艳艺, 等. 珠江口表层水中多环芳烃的分布特征及健康风险评估[J].中国环境监测, 2018, 34(2): 64-72.
[44] Sa E. Scientific opinion of the panel on contaminants in the food chain on a request from the European Commission on polycyclic aromativ hydrocarbons in food[J]. EFSA J, 2008, 724: 1-114.
[45] Cheng L, Gan Y, Tang X Q, et al. Pollution analysis and health risk assessment of polycyclic aromatic hydrocarbons in fried food[J]. Chinese J Heal Labor Technol, 2021, 31(15): 1909-1913.
[46]杨晓倩, 于志刚, 刘仲,等.济南市居民膳食油脂多环芳烃暴露定量风险评估[J]. 现代预防医学, 2018, 45(17): 3114-3117.
[47] Asamoah A, Mahdi N F, David K E, et al. PAHs contamination levels in the breast milk of Ghanaian women from an e-waste recycling site and a residential area[J]. Sci Total Environ, 2019, (666): 347-354.
[48]张会敏, 龙明华, 乔双雨, 等. 瓜类蔬菜体内多环芳烃的分布特征及健康风险评估[J]. 华南农业大学学报, 2019, 40(2): 83-93.
[49] Seyedeh F T , Majid A R, Ramin R, et al. Polycyclic aromatic hydrocarbons, pesticides, and metals in olive: analysis and probabilistic risk assessment[J]. Environ Sci Pollut R, 2021, (28): 39723-39741.
[50] 府雨月, 丁洪流, 金琦, 等. 儿童玩具和用品中18种多环芳烃含量检测与风险分析[J]. 中国塑料, 2018, 32(12): 126-131.
[51]卢城德. 煤焦油沥青职业接触人群多环芳烃暴露特征及健康风险研究[D]. 济南:济南大学, 2018.
[52] Petit P, Maître A, Persoons R, et al. Lung Cancer Risk Assessment for Workers Exposed to Polycyclic Aromatic Hydrocarbons in Various Industries[J]. Environ Int, 2019, 124: 109-120.
[53] Saleh S A.K, Adly H M, Aljahdali I A, et al. Correlation of Occupational Exposure to Carcinogenic Polycyclic Aromatic Hydrocarbons (CPAHs) and Blood Levels of P53 and P21 Proteins[J]. Biomolecules, 2022, 12: 260.
表1 US EPA 16种优先控制的PAHs的物理化学性质
Table 1 Physicochemical properties of 16 PAHs classified by US EPA as priority pollutants
序号 | 中文名称 | 英文简写 | 分子式 | 分子量 | CAS编号 | 致癌性b | 沸点 (℃) | 熔点 (℃) | 水溶解度 (mg/L, 25℃) |
1 | 萘a | Nap | C10H8 | 128 | 91-20-3 | 209 | 80 | 33.8 | |
2 | 苊烯 | Ace | C12H8 | 152 | 208-96-8 | 290 | 124 | 6.7 | |
3 | 苊 | Acp | C12H10 | 154 | 83-32-9 | 3 | 252 | 108 | 3.0 |
4 | 芴 | Fl | C13H10 | 166 | 86-73-7 | 3 | 276 | 119 | 1.7 |
5 | 菲 | Phe | C14H10 | 178 | 85-01-8 | 3 | 326 | 136 | 0.6 |
6 | 蒽 | An | C14H10 | 178 | 120-12-7 | 3 | 326 | 136 | 0.6 |
7 | 荧蒽a | Flu | C16H10 | 202 | 206-44-0 | 3 | 369 | 166 | 0.1 |
8 | 芘 | Pyr | C16H10 | 202 | 129-00-0 | 3 | 369 | 166 | 0.1 |
9 | 苯并[α]蒽 | BaA | C18H12 | 228 | 56-55-3 | 2A | 400 | 177 | 0.02 |
10 | 䓛 | Chr | C18H12 | 228 | 218-01-9 | 3 | 400 | 177 | 0.06 |
11 | 苯并[b]荧蒽a | BbF | C20H12 | 252 | 205-99-2 | 2B | 461 | 209 | 0.02 |
12 | 苯并[k]荧蒽a | BkF | C20H12 | 252 | 207-08-9 | 2B | 430 | 194 | 0.002 |
13 | 苯并[α]芘a | BaP | C20H12 | 252 | 50-32-8 | 2A | 461 | 209 | 0.002 |
14 | 茚-[1,2,3-cd]芘a | Inp | C22H12 | 276 | 193-39-5 | 2A | 498 | 233 | 0.000 |
15 | 二苯并[a,h]蒽 | Dba | C22H14 | 278 | 53-70-3 | 2A | 487 | 218 | 0.004 |
16 | 苯并[g,h,i]苝a | BghiP | C22H12 | 276 | 191-24-2 | 467 | 218 | 0.006 |
注: a表示被列入“中国环境优先控制污染物”的黑名单; b表示具有致癌性, A的致癌性比B高, 3的致癌性比2低。
表2 6种累积风险评估方法信息表
Table 2 Six cumulative risk assessment methods
序号 | 方法 | 公式 | 判断风险依据 | 优点 | 缺点 |
1 | (HI) | EXP: 暴露量;RfD: 健康值导值 | 当 HI≥1 时,存在健康风险;当HI<1时,相对安全 | 简单易懂,便于计算 | 不适用存在相互作用关系的混合物,结果易受UF的影响 |
2 | (CRI) |
| 当CRI<1,认为风险不可接受 | / | 理解和推算过程较为复杂,结果易受UF的影响 |
3 | (RPF) |
| 当EXPm≤指示化学物 | 理论上较为完备的方法 | 仅适用于具有剂量叠加性化学物,结果与指示化学物的选择相关,并需要足够的毒理学数据 |
4 | (POD) |
| / | 计算过程不引入UF,最后再引入,结果受其影响更小 | 目前,国际上无统一的风险评判依据 |
5 | (MOE) |
| 当 MOET>100时,累积暴露风险可以接受 | 结果与实际暴露量相关,不易受到政策管理的影响 | 目前,国际上尚无确定的判断风险依据,主要以单一化学物的MOE为参考 |
6 | (TEF) | C: 浓度 | / | 结果与实际暴露量相关,不易受到政策管理的影响 | 结果需要大量毒理学数据支持 |












