CopyRight 2009-2020 © All Rights Reserved.版权所有: 中国海关未经授权禁止复制或建立镜像
大豆新发病害Diaporthe novem干热处理研究初报
作者:张淼 张莹 王娓辰 刘勇 王伟 廖芳 康芬芬
张淼 张莹 王娓辰 刘勇 王伟 廖芳 康芬芬
大豆作为主要粮食作物和重要经济作物,国内有着巨大需求。国产大豆因蛋白质含量丰富,主要用于豆腐、豆浆、腐竹等豆制品制作;进口大豆因脂肪含量高,主要满足加工食用油和养殖用豆粕需求[1]。受环境因素、技术水平、生产成本等限制,我国每年需进口大量大豆以满足国内需求[2]。2020年我国进口大豆量高达10033亿t。受疫情影响,2021年大豆进口量虽较上年稍有下降,但仍达到9653.28 t[3]。由于大豆进口量持续处于高位,其携带外来有害生物入境的风险也备受重视。
2019年8月,天津海关动植物与食品检测中心植物检疫实验室从进境美国大豆中截获Diaporthe novem[4]。该病菌由Jorge Manuel Santos等[5]于2011年正式命名,无性阶段为Phomopsis sp. 9 [6]。它与《中华人民共和国进境植物检疫性有害生物名录》中大豆北方茎溃疡病菌D. caulivora及大豆南方茎溃疡病菌D. aspalathi互为近似种,为害大豆[5, 7]、向日葵[8-9]、猕猴桃[10-11]、葡萄[12]、金橘和青柠[13]等重要经济作物,引起茎秆溃疡[14]、种子和果实腐烂,造成严重经济损失。目前该病菌在智利[10]、克罗地亚[5]、澳大利亚[8-9]、葡萄牙[15]、南非[6, 12]和意大利[8, 13, 16]等地区有分布,我国无分布。2018年,Kristina Petrović等[14]从塞尔维亚大豆种子中检出该病菌,并作为一种塞尔维亚大豆上的新发病害报道。
目前,针对携带D. novem大豆的检疫处理方法尚处于空白状态。干热处理作为一种较为常用的物理处理方法,在种子检疫处理中应用广泛[17]。2008年,王良华等[18]采用干热处理的方法对大豆疫霉卵孢子的致死条件进行了筛选。本文设置不同温度梯度和处理时间组合,研究干热处理对D. novem检疫处理效果和大豆品质的影响,为口岸进境大豆中D. novem及间座壳属真菌的检疫处理工作提供依据和参考。
1 材料与方法
1.1 材料
供试菌株分离于进境美国大豆。
1.2 仪器设备
天津泰斯特仪器有限公司生产的WGL-230B型电热鼓风干燥箱(控温范围:10~300℃,控温精度:±1.0℃);日本三洋公司生产的MIR-554型低温恒温培养箱(控温范围:-10~60℃,控温精度:±0.5℃);丹麦FOSS分析仪器公司生产的 NIRS DS2500F 多功能近红外光谱分析仪(光谱范围:400~2500 nm)。
1.3 D. novem菌丝体离体干热处理
对培养7 d的供试菌株进行干热处理。设置45℃、50℃、55℃ 3个温度梯度,每个温度梯度下分别设10 min、20 min、30 min 3个处理时间,每个处理重复3次。对照25℃培养,不进行干热处理。干热处理时,先将烘箱温度调节至设定温度,待内部实测温度稳定于设定温度的±0.5℃时,放入培养物,关闭仓门,当烘箱实测温度恢复至设定温度的±0.5℃时,开始计时。
无菌条件下,使用0.7 cm 打孔器,将干热处理后的菌丝块置于PDA培养基中于25℃进行再培养。每天用十字交叉法测量菌落直径,菌落直径增长值为7.8 cm时视为长满培养皿,持续观察4周。
1.4 干热处理后大豆品质分析
选用健康非转基因大豆籽粒进行干热处理,处理条件及方法同“1.3”所述。用FOSS多功能近红外光谱分析仪对大豆籽粒的水分、蛋白质含量、含油量等指标进行测定。
1.5 数据处理
使用Microsoft Excel 2010 和IBM SPSS Statistics v21 软件进行数据整理和单因素方差分析,测定数据用进行差异显著性比较。
2 结果与分析
2.1 D. novem菌丝体干热处理效果
D. novem菌丝体干热处理效果如图1所示。由图1可以看出,与对照菌落直径相比,当处理温度在45℃和50℃,处理时间为 10 min和20 min时,干热处理对D. novem菌丝生长的抑制效果不大,5~7 d 菌丝即可长满培养皿;当50℃处理30 min 和 55℃处理10 min开始,干热处理对D. novem的菌丝有明显抑制作用,菌落不再增长,说明50℃干热处理30 min,或55℃处理10 min开始能有效杀灭离体条件下的D. novem。
2.2 干热处理对大豆籽粒主要品质的影响
大豆籽粒经不同干热处理,其水分、蛋白质、蛋白质(干基)和含油见表1。由表1可以看出,干热处理后的大豆水分在12.77%~13.80%之间,与对照13.93%相比,水分均有所减少,但仅50℃处理20 min和55℃处理20 min与对照相比差异显著,水分减少1.09%~1.16%。蛋白质、蛋白质(干基)及含油所有处理与对照相比差异不显著。试验结果表明,45~55℃干热处理10~30 min会使大豆籽粒含水量减少,减少量在1%左右,影响较小;此条件对蛋白质、蛋白质(干基)及含油等品质指标无显著影响。
3 讨论
国内尚未有对D. novem生物学特性的相关研究,其近似种大豆茎溃疡病菌的生长温度范围较广,最适生长温度为25℃,最高可生长温度方面,大豆北方茎溃疡病菌为30℃;大豆南方茎溃疡病菌为40℃[19]。本文通过试验证明,干热处理可以抑制D. novem生长。当50℃干热处理30 min,或55℃处理时间≥10 min时,可有效杀灭D. novem,且除水分略有降低外,该处理条件不会对大豆籽粒的蛋白质、蛋白质(干基)、含油等品质指标产生影响。该研究结果可为口岸进境大豆中携带间座壳属真菌的检疫处理工作提供理论依据和技术参考。
美国、巴西等国家常采用熏蒸方法处理大豆,在熏蒸时将磷化铝直接撒在大豆表面,造成铝残留,处理较为困难[20]。辐照处理也是常用的大豆检疫处理手段,能彻底消灭微生物并保证长时间不会生虫霉变,但因其价格高、消费者回避等问题在实际使用中受到限制。热处理技术是利用高温使病原菌蛋白质(酶)、核酸和脂类等重要生物高分子发生降解或改变其空间结构,使其变性或破坏,新陈代谢无法正常进行,最终导致病原菌死亡,因其具有效果好、无残留、环境友好等优势而被广泛应用[21]。目前,常见的热处理方法包括热水处理、蒸热处理、干热处理、低温热处理、热处理与其他处理相结合等[22]。此次试验选用了干热处理的方法,找到了抑制离体菌丝生长的合适处理温度和处理时间。供试菌株是从进境美国大豆中分离出来的,此批大豆还分离到其他真菌,由于没有只携带该菌的大豆样品,所以本研究仅对离体条件下的D. novem进行干热处理。在今后的研究中,可以将该病菌接种于大豆,对发病大豆进行检疫处理研究,还可以采用不同的热处理方法并进行比较,找出针对该病菌最适宜的处理方式。
近年来,近红外光谱(NIRS)快速分析技术广泛应用于分析化学和检测领域。该技术具有制样简单、无污染、易操作、速度快的优点。本试验利用近红外光谱分析仪测定干热处理后大豆籽粒的部分品质指标,后续可以对经处理大豆的其他品质指标、营养成分、种子活力等方面进行进一步研究。
参考文献
[1] 沈洁, 高强. 新形势下我国大豆进口面临的风险与对策[J]. 中国经贸导刊(中), 2020(9): 17-20.
[2] 左武荣. 我国大豆进口贸易的影响及对策研究[J]. 分子植物育种, 2022, 20(2): 601-606.
[3] 杨辉, 林嘉柏, 林佳. 外生冲击下中国大豆产业安全:现状、挑战与机遇[J]. 大豆科学, 2022, 41(3): 352-357.
[4] 张莹, 胡佳续, 滕少娜, 等. 进境美国大豆中值得关注的真菌Diaporthe novem[J]. 菌物学报, 2022, 41(3): 412-419.
[5] Santos J M, Vrandečić K, Ćosić J, et al. Resolving the Diaporthe species occurring on soybean in Croatia[J]. Persoonia, 2011, 27: 9-19.
[6] van Rensburg J C J, Lamprecht S C, Groenewald J Z, et al. Characterization of Phomopsis spp. associated with die-back of rooibos (Aspalathus linearis) in South Africa[J]. Studies in Mycology, 2006, 55: 65-74.
[7] Petrović K, Riccioni L, Djordjevic V, et al. Diaporthe pseudo longicolla: The new pathogen on soybean seed in Serbia[J]. Ratarstvoi Povrtarstvo, 2018, 55(2): 103-109.
[8] Rekab D, Del Sorbo G, Reggio C, et al. Polymorphisms in nuclear rDNA and mtDNA reveal the polyphyletic nature of isolates of Phomopsis pathogenic to sunflower and a tight monophyletic clade of defined geographic origin[J]. Mycology Research, 2004, 108(4): 393-402.
[9] Thompson S M, Tan Y P, Neate S M, et al. Diaporthe novem isolated from sunflower (Helianthus annuus) and other crop and weed hosts in Australia[J]. European Journal of Plant Pathology, 2018, 152(3): 823-831.
[10] Díaz G A, Latorre B A, Jara S, et al. First report of Diaporthe novem causing postharvest rot of kiwifruit during controlled atmosphere storage in Chile[J]. Plant Disease, 2014, 98(9): 1274.
[11] Díaz G A, Latorre B A, Lolas M, et al. Identification and characterization of Diaporthe ambigua, D. australafricana, D. novem, and D. rudis causing a postharvest fruit rot in kiwifruit[J]. Plant Disease, 2017, 101(8): 1402-1410.
[12] Niekerk J M, Groenewald J Z, Farr D F, et al. Reassessment of Phomopsis species on grapevines[J]. Australasian Plant Pathology, 2005, 34: 27-39.
[13] Guarnaccia V, Crous P W. Emerging citrus diseases in Europe caused by species of Diaporthe[J]. IMA Fungus, 2017, 8: 317-334.
[14] Petrović K, Riccioni L, Djordjevic V, et al. Diaporthe pseudolongicolla: The new pathogen on soybean seed in Serbia[J]. Ratarstvoi Povrtarstvo, 2018, 55(2): 103-109.
[15] Santos J M, Correia V G, Phillips A J L. Primers for mating-type diagnosis in Diaporthe and Phomopsis: their use in teleomorph induction in vitro and biological species definition[J]. Fungal Biology, 2010, 114(2-3): 255-270.
[16] Dissanayake A J, Camporesi E, Hyde K D, et al. Molecular phylogenetic analysis reveals seven new Diaporthe species from Italy[J]. Mycosphere, 2017, 8(5): 853-877.
[17] 康芬芬, 王仲敏, 孙佩珊, 等. 干热处理对奇亚籽的灭活效应及品质的影响[J]. 植物检疫, 2009, 33(3): 46-49.
[18] 王良华, 丁国云, 吴翠萍, 等. 大豆疫霉卵孢子致死温度的测定[J]. 植物检疫, 2008, 22(6): 351-353.
[19] 王颖, 杨伟东, 陈枝楠, 等. 大豆茎溃疡病菌的生物学特性及其传入我国的风险[J]. 植物检疫, 2009, 23(1): 23-25.
[20] 杜国兴, 周明华, 陈正桥, 等. 进口大豆检疫中存在的问题[J]. 植物检疫, 2003, 17(4): 249-250.
[21] 程瑜, 张瑞峰, 张莹, 等. 热水处理对丁香疫霉和脐橙的处理效果研究初报[J]. 植物检疫, 2016, 30(1): 25-28.
[22] 刘娟, 楼阁, 王娓辰, 等. 丁香疫霉热处理方法的比较与分析[J]. 食品研究与开发, 2017, 38(19): 191-195.
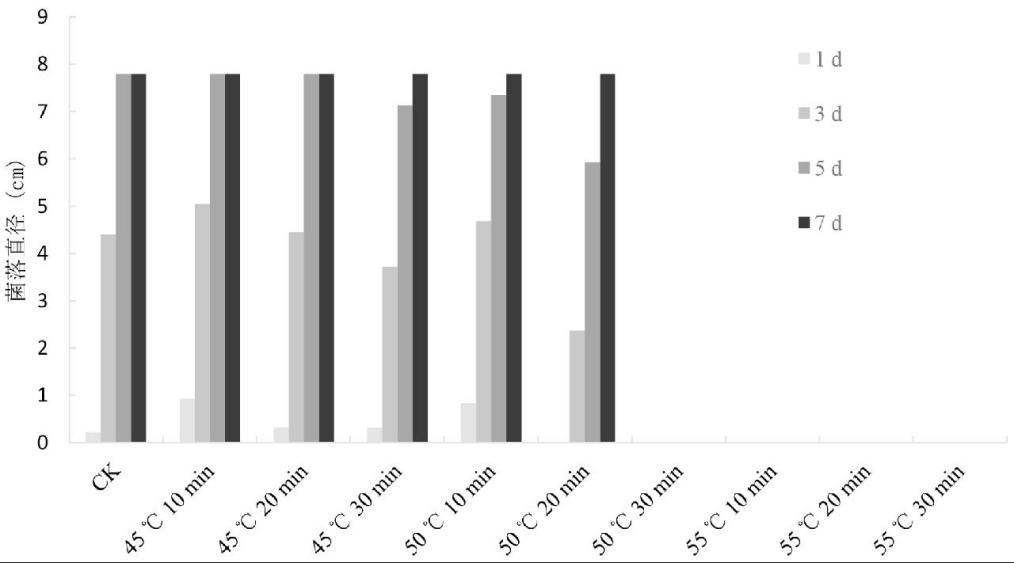
数据为每组处理重复3次的平均数
图1 D. novem菌丝体离体干热处理效果
Fig.1 Effects on dry heat treatment of D. novem mycelium in vitro
表1 干热处理对大豆籽粒品质影响
Table 1 Effects of dry heat treatment on soybean seed quality
处理 | 水分 (%) | 蛋白质 (%) | 蛋白质(干基) (%) | 含油 (%) |
对照 | 13.93±0.16a | 36.27±0.39a | 43.56±0.85a | 18.80±0.20ab |
45℃ 10 min | 13.75±0.43abc | 36.22±0.33a | 43.58±0.86a | 18.94±0.21ab |
45℃ 20 min | 13.74±0.42abc | 36.49±0.31a | 44.01±0.52a | 18.81±0.41ab |
45℃ 30 min | 13.65±0.63abc | 36.70±0.24a | 43.93±0.27a | 18.73±0.26ab |
50℃ 10 min | 13.80±1.05ab | 36.03±0.04a | 43.35±0.29a | 19.16±0.32a |
50℃ 20 min | 12.77±0.42c | 36.65±0.55a | 43.62±0.72a | 18.12±1.04b |
50℃ 30 min | 12.81±0.33bc | 36.48±0.28a | 43.63±0.54a | 18.05±0.07b |
55℃ 10 min | 12.84±0.35bc | 36.01±1.12a | 42.93±0.98a | 18.70±0.71ab |
55℃ 20 min | 12.79±0.51c | 36.16±0.35a | 43.59±0.48a | 18.54±0.46ab |
55℃ 30 min | 13.19±0.40abc | 36.86±0.67a | 43.93±0.55a | 18.27±0.34ab |
注: 同一列不同字母表示各处理之间存在显著差异(P<0.05); 数据为每个处理的3个重复的平均数







