CopyRight 2009-2020 © All Rights Reserved.版权所有: 中国海关未经授权禁止复制或建立镜像
隐蔽型伏马毒素研究进展
作者:胡玲 朱海强 程玉文
胡玲 朱海强 程玉文
伏马毒素是一类在玉米等农产品中广泛存在的真菌毒素,主要由镰刀菌属真菌产生,其化学骨架为19-或20-碳长链氨基多元醇,其中14-和15-位的羟基分别通过与一个丙三羧酸分子反应成酯[1]。根据化学结构上的差异,伏马毒素可分为A、B、C和P四大类,较常见的为B类,其中又以伏马毒素B1(fumonisin B1,FB1)和伏马毒素B2(fumonisin B2,FB2)与人类健康最为密切相关[2],如图1所示。随着研究的深入,人们在伏马毒素原型以外,又陆续发现了它们的多种转化产物,统称为隐蔽型伏马毒素,即化学结构在伏马毒素原型的基础上发生了改变,难以用常规分析方法检测到的伏马毒素衍生物[1, 3]。
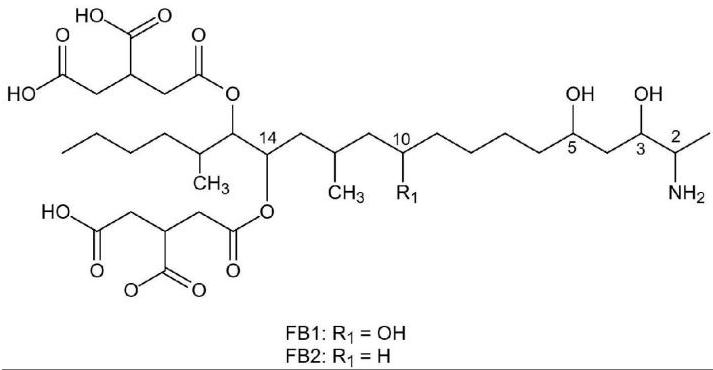
图1 伏马毒素B1和B2(FB1和FB2)的化学结构式
Fig.1 Chemical structure of fumonisins B1 and B2
(FB1 and FB2)
隐蔽型伏马毒素具有不同程度的毒性,是一种容易被忽略的潜在健康风险,其主要产生途径有:(1)动植物和微生物体内的Ⅰ相和Ⅱ相代谢,其中,Ⅰ相代谢通过氧化还原和水解反应使伏马毒素原型发生结构改变,Ⅱ相代谢则是通过一系列生化反应将生物体的内源小分子(如葡萄糖)与伏马毒素原型共价结合;(2)食品加工过程(如碱水解处理、热挤压)中发生的非酶促化学反应;(3)与农产品基质中的大分子(如蛋白质、多糖)发生共价结合[1,3]。本文从隐蔽型伏马毒素的种类、检测方法、污染状况和体内外毒性等方面对其研究进展进行综述,以期为相关研究提供参考。
1 隐蔽型伏马毒素的种类
目前已发现的隐蔽型伏马毒素中,以FB1的隐蔽型为主,其次为FB2的隐蔽型,主要可分为以下几种。
1.1 水解型或部分水解型伏马毒素
水解型或部分水解型伏马毒素最早被发现于经过碱处理的玉米制品中。以玉米为主食的墨西哥人在制作玉米面团时,通常会使用一种叫“nixtamalisation”的处理方法,即将玉米用石灰水煮过之后,再磨成糊状,在这个过程中,大量的伏马毒素被石灰水碱化,脱去1个或2个丙三羧酸基团,形成水解型或部分水解型伏马毒素[4]。以FB1为例:其经过不完全水解,失去1个丙三羧酸基团,转变为部分水解型FB1(partially hydrolyzed fumonisin B1,pHFB1),根据失去的丙三羧酸基团位置不同,又分为a型和b型;FB1经过完全水解,失去2个丙三羧酸基团,转变为水解型FB1(hydrolyzed fumonisin B1,HFB1),如图2所示。
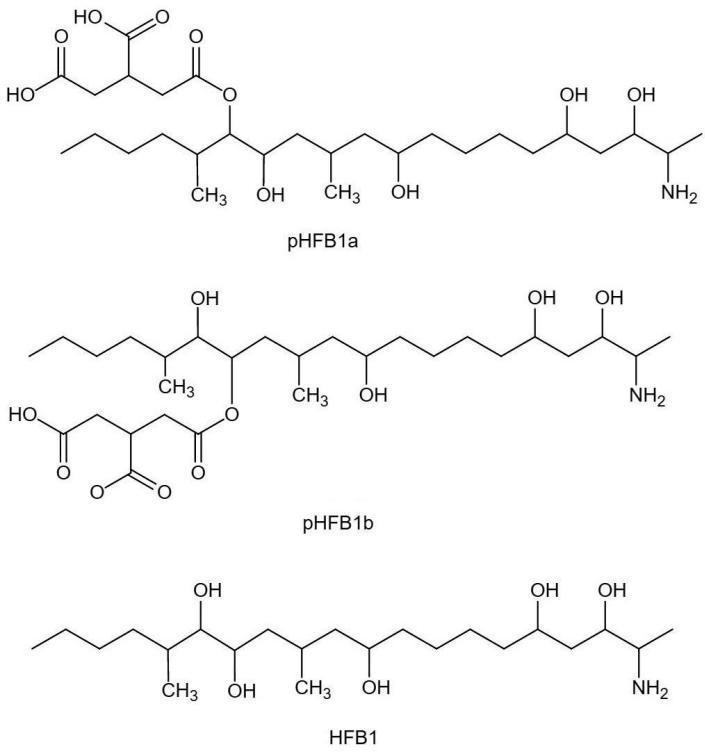
图2 部分水解FB1(pHFB1a和pHFB1b)和水解FB1(HFB1)的结构式
Fig.2 Chemical structures of pHFB1 (a and b) and HFB1
1.2 O-脂肪酰基化伏马毒素
伏马毒素的多个羟基(如FB1的3-、5-、10-位羟基)均可与脂肪酸发生酯化反应,形成O-脂肪酰基化的伏马毒素。Bartok等[5]首次报道从串珠镰刀菌(Fusarium verticillioides)的大米培养物中提取得到3种O-脂肪酰基化伏马毒素,并根据其高分辨质谱的精确分子量及质谱裂解规律,推测脂肪酰基对应的脂肪酸分别为棕榈酸、亚油酸和油酸。进一步的研究表明,O-脂肪酰基化伏马毒素的形成与真菌生长的基质种类密切相关,玉米比大米更有利于伏马毒素的O-脂肪酰基化,原因可能是玉米中的脂肪酸含量更高[6]。
1.3 N-脂肪酰基化伏马毒素
伏马毒素的2-位氨基亦可与脂肪酸(如棕榈酸、硬脂酸、油酸、亚油酸)发生缩合反应,形成各种N-脂肪酰基伏马毒素[7]。
1.4 N-羧甲基伏马毒素
虽然伏马毒素是一类热稳定性较强的毒素,但在食品热加工过程中,伏马毒素可能与食品中的还原糖发生美拉德反应,形成N-羧甲基伏马毒素,主要反应机理为伏马毒素的2-位氨基与还原糖的羰基反应,形成希夫碱,后者经Amadori重排,形成不稳定的中间产物N-(1-脱氧-D-果糖-1-基)伏马毒素,随后转变为稳定的终产物N-羧甲基伏马毒素[8]。目前研究报道的主要为N-羧甲基FB1,其化学结构式如图3所示。
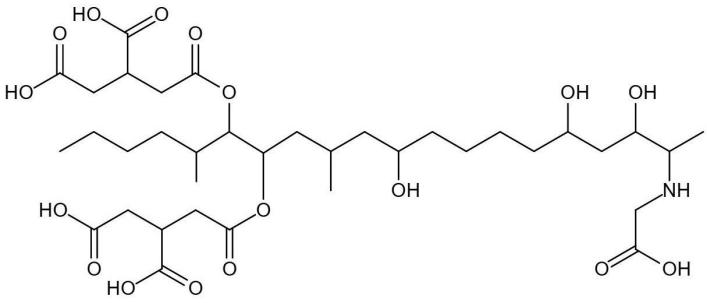
图3 N-羧甲基FB1的结构式
Fig.3 Chemical structures of N-carboxymethyl-FB1
1.5 与基质大分子结合的隐蔽型伏马毒素
伏马毒素还可通过其上的2个丙三羧酸侧链与基质中的蛋白质、多糖等大分子共价结合,从而导致常规方法无法将其提取出来,但在人体或动物胃肠道消化液的作用下,随着蛋白质、多糖等大分子的分解,这些隐蔽型伏马毒素又将以游离态的形式被释放[1]。
2 隐蔽型伏马毒素的检测方法
隐蔽型伏马毒素的检测方法可分为直接法和间接法两大类。直接法的最终检测对象为各种隐蔽型伏马毒素单体化合物;间接法则是首先通过碱处理或体外酶促消化使隐蔽型伏马毒素的化学结构发生转变,最后以转化产物为检测对象。
隐蔽型伏马毒素种类复杂多样,化学性质不尽相同,直接法需要根据它们各自的特点分别开发合适的检测方法,主要包括溶剂提取、净化、仪器分析等步骤。水解型伏马毒素和N-羧甲基伏马毒素的提取溶剂与其原型类似,常见的有甲醇-水、乙腈-水等体系,例如,以甲醇-乙腈-柠檬酸盐/磷酸盐缓冲液(25:25:50,v/v/v)为溶剂提取玉米中的伏马毒素、水解型伏马毒素和部分水解型伏马毒素[4],用甲醇-乙腈-水(25:25:50,v/v/v)提取玉米加工食品中的N-羧甲基伏马毒素[9]。O-脂肪酰基化伏马毒素的极性较其原型有所降低,提取溶剂中水的比例也相应降低,如可采用甲醇-水(75:25,v/v)溶剂体系[2]。Park等[7]用正己烷、氯仿提取玉米及其制品中的N-棕榈酰基FB1、N-油酰基FB1、N-亚油酰基FB1和N-硬脂酰基FB1,提取后的净化步骤则主要有固相萃取(如C18小柱)等,有的仅经过简单的稀释和微孔滤膜过滤。为达到满意的灵敏度和准确度,最后的仪器分析步骤普遍采用高效液相色谱-串联质谱法(LC-MS/MS),即将样品中的目标化合物经色谱有效分离后,再利用串联质谱根据其保留时间、母离子和二级碎片离子进行定性、定量。
Dall’Asta等[10]以碱水解为前处理手段,开发了一种间接检测方法,首先用常规方法提取、检测样品中的伏马毒素,再用2 mol/L氢氧化钠溶液水解常规提取后的样品残渣,将其中的多种隐蔽型伏马毒素一并转化为水解型,经乙酸乙酯萃取后,浓缩、过微孔滤膜,最后通过LC-MS/MS检测水解型伏马毒素。该方法步骤简便,可一步检测脂肪酰基化伏马毒素、水解和部分水解型伏马毒素,以及与样品中的大分子共价结合的隐蔽型伏马毒素,适用于玉米、小麦、大麦、大米及相关制品等多种食品基质[11-12]。需要说明的是,N-羧甲基伏马毒素在碱水解后转变成N-羧甲基水解型伏马毒素,而不是水解型伏马毒素,因此无法用碱水解法检测。此外,针对与基质大分子共价结合的隐蔽型伏马毒素,还可使用人工消化液对样品进行体外模拟消化,使伏马毒素从基质中释放出来,然后再使用常规方法检测其中的伏马毒素总量[13]。
总的来说,直接法虽然精准,但较为烦琐,此外由于缺乏标准物质,研究人员需首先合成并鉴定相应的化合物,才能进一步开发检测方法,因此限制了直接法的广泛应用。与之相比,间接法虽然无法获得各种隐蔽型伏马毒素的具体类别信息,但较为简便,适用于隐蔽型伏马毒素总量的测定。
3 隐蔽型伏马毒素的污染状况
目前,标准品的缺乏在很大程度上限制了隐蔽型伏马毒素污染状况调查的开展。在各种隐蔽型伏马毒素中,水解型伏马毒素是目前报道最多的一类,其标准品虽未商业化,但仅需将伏马毒素标准品进行碱水解后,再经简单的分离提取步骤即可制得,由此制得的标准品还可应用于间接法检测隐蔽型伏马毒素。近年来的研究表明,在玉米及其制品中,隐蔽型伏马毒素往往伴随着其原型存在,而在使用碱处理工艺的玉米加工食品(如墨西哥玉米饼)中,水解型伏马毒素尤为常见,其含量有时甚至可超过原型[14]。Zimmer等[15]调研了德国市售的272份谷物类食品,发现在“玉米片和玉米粒”这一类别样本中,HFB1的检出率高达62.4%,超过了其原型FB1的检出率(55.8%),HFB1含量的中位数为13 μg/kg,亦超过了FB1含量的中位数(10 μg/kg)。Hu等[16]用碱水解法检测了58份中国山东和浙江市场上的玉米粒、玉米片、爆米花等玉米相关食品,隐蔽型伏马毒素的检出率高出其原型20%,两者之比在0.1~4.2之间不等。Ezekiel等[17]在40份尼日利亚玉米粉、大米粉、山药粉等生粉样品中,检测到2.5~153 μg/kg含量水平的水解型FB1,检出率为40%。Andrade等[12]从巴西零售商店收集了85份玉米制品,除1份“早餐谷物”样品外,其余84份均检出隐蔽型伏马毒素,平均含量占伏马毒素总量(隐蔽型+原型)的5%。De Girolamo等[4]的研究发现,受伏马毒素污染的玉米粒经过1%或5%石灰水“nixtamalisation”处理后,FB1、HFB1和pHFB1的含量均有不同程度的增加,在这个过程中,原本与玉米中的淀粉、蛋白质等大分子共价结合或被物理吸附的FB1被释放出来,其中的一部分随后又通过碱水解转变成了HFB1和pHFB1。
在水解型伏马毒素以外,其他隐蔽型伏马毒素的污染状况尚只有零星报道。Falavigna等[2]分析了5份于自然条件下受到伏马毒素严重污染的玉米样本,其中均检测到了O-油酰基FB1和O-亚油酰基FB1,2种毒素的最高含量分别达763 μg/kg和810 μg/kg,两者之和占该玉米样本中FB1含量的6.1%。Park等[7]检测了38份玉米饼、玉米片及生玉米样品中的N-棕榈酰基FB1、N-油酰基FB1、N-亚油酰基FB1和N-硬脂酰基FB1,在其中1份墨西哥玉米片中检出总含量约为70 μg/kg的N-脂肪酰基FB1。Seefelder等[9]从德国市场上收集了10份玉米片等玉米加工食品,其中6份样品检出N-羧甲基FB1,含量水平为10~76 μg/kg。
4 隐蔽型伏马毒素的毒性
目前,关于隐蔽型伏马毒素的毒性的研究仍处于初步阶段,它们对于人体的毒性作用尚未见报道。由于难以获得足够数量的标准品,已有的毒性研究仍较为粗浅,且主要集中于水解型伏马毒素等少数几种隐蔽型伏马毒素。
4.1 隐蔽型伏马毒素的动物体内毒性
Hartl等[18]将卤虫(Artemia salina)分别暴露于不同浓度的伏马毒素、水解型伏马毒素、N-棕榈酰基伏马毒素和N-羧甲基伏马毒素中,结果显示,FB1、HFB1、N-羧甲基FB1的半数致死浓度(LC50)分别为2.7、17.9、285.3 μmol/L,提示FB1经完全水解后毒性有所降低,而食品热加工过程中容易产生的N-羧甲基FB1则毒性大大降低(2个数量级);FB2和HFB2的LC50提示了相似的规律,FB2经完全水解后,LC50从4.8 μmol/L提高到了11.8 μmol/L。
Hahn等[19]以雄性SD大鼠为试验对象,分别连续饲喂添加了FB1、pHFB1和HFB1(含量水平均为13.9 μmol/kg)的饲料,并在第7天、第14天、第21天分析尿液中的二氢神经鞘氨醇(Sa)和神经鞘氨醇(So)含量,以Sa/So比值升高作为受试物干扰鞘脂代谢的生物指标,发现除FB1组出现Sa/So比值显著升高外(P<0.05),pHFB1和HFB1组的Sa/So比值均与对照组无统计学差异。Howard等[20]采用含有不同剂量受试物的饲料连续饲喂雌性B6C3F1小鼠28 d,除FB1在高剂量组(72 μmol/kg和143 μmol/kg)观察到血清总胆汁酸、胆固醇和碱性磷酸酶水平上升外,其余包括FB2、HFB1、N-羧甲基FB1和N-乙酰基FB1在内的受试物均未观察到明显作用。Voss等[21]以LM/Bc孕鼠为试验动物,采用腹腔注射(i.p.)的给药方式研究了FB1和HFB1的致畸胎作用,结果表明,FB1在10 mg/kg·bw的剂量下,显著干扰母鼠鞘脂代谢,引发母鼠肝细胞凋亡,并在所有胎鼠中均观察到神经管畸形;而HFB1仅在20 mg/kg·bw的最高剂量组观察到轻微的母鼠鞘脂代谢异常,但未引起母鼠肝损伤或胎鼠神经管畸形。总的来说,现有的大鼠、小鼠体内毒性研究数据表明,水解型伏马毒素相对其原型而言毒性明显降低。
4.2 隐蔽型伏马毒素的体外毒性
Norred等[22]采用精密肝切片技术,研究了伏马毒素原型及若干种隐蔽型对大鼠肝脏的体外鞘脂代谢毒性,发现3种水解型伏马毒素(HFB1、HFB2和HFB3)在0.05、0.5和5 μmol/L浓度下的毒性约为其原型的30%~40%,但这种毒性效应不呈现浓度依赖性;N-乙酰基FB1在上述浓度下均未影响鞘脂代谢。
不同的体外细胞系毒性研究表明,水解型伏马毒素的毒性普遍低于其原型。Schmelz等[23]的研究发现,FB1可在10 μmol/L浓度下使人结肠癌HT29细胞数量减少30%,而HFB1则需在50 μmol/L浓度下方可达到同样的效果。火鸡外周血淋巴细胞增殖实验表明,HFB1的半数抑制浓度(IC50)为其原型FB1的10倍[1],猪小肠上皮细胞(IPEC-J2)和猪外周血单核细胞(PBMCs)实验亦表明HFB1的毒性小于FB1[24]。
此外,Meca等[25]通过猴肾Vero细胞实验发现,FB1的IC50为55 μmol/L,而在同样浓度下,N-羧甲基FB1未观察到明显抑制作用。
与水解型伏马毒素的毒性减弱相反,多个关于体外细胞毒性的报道表明,2-位氨基的脂肪酰基化使伏马毒素和水解型伏马毒素的毒性有所增强。Harrer等[26]的研究发现,N-棕榈酰基FB1、N-硬脂酰基FB1等长链N-脂肪酰基伏马毒素在20 μmol/L浓度下对人胚肾细胞(Hek)、人肝癌细胞(Hep3B)和人成纤维细胞具有显著毒性,培养8 h后,引起40%~80%细胞死亡,而同样浓度的FB1对上述细胞系均未表现出毒性。Abou-Karam等[27]采用小鼠成纤维细胞(3T3和KA31T)、犬肾上皮细胞(MDCK)和大鼠肝癌细胞(H4TG)为模型,比较了HFB1及其N-脂肪酰基化衍生物(即N-脂肪酰基HFB1)的体外细胞毒性,发现脂肪链长度为C8~C16的N-脂肪酰基HFB1对上述细胞系的毒性均显著超过HFB1,并在碳链长度为10和12时达到峰值。
5 结语
近年来,隐蔽型真菌毒素的潜在食品安全风险已引起越来越多的国内外研究者关注,其中,隐蔽型伏马毒素种类繁多,理化性质各异,可伴随伏马毒素原型存在于食品中。目前,受限于隐蔽型伏马毒素标准品的匮乏,相关的检测方法、污染状况和毒性等研究报道仍然十分有限。为进一步对隐蔽型伏马毒素进行科学的暴露和健康风险评估,未来还需开展更广泛的污染水平调查和更深入的毒理学研究,而相关标准品的研制则是亟需解决的重要问题之一。
参考文献
[1] EFSA Panel on Contaminants in the Food Chain. Appropriateness to set a group health-based guidance value for fumonisins and their modified forms [J]. EFSA Journal, 2018, 16(2): 5172.
[2] Falavigna C, Lazzaro I, Galaverna G, et al. Fatty acid esters of fumonisins: first evidence of their presence in maize [J]. Food Additives & Contaminants: Part A, 2013, 30(9): 1606-1613.
[3] 余佃贞, 田野, 武爱波. 粮食中隐蔽型真菌毒素污染的研究进展[J]. 食品安全质量检测学报, 2018, 9(2): 349-354.
[4] De Girolamo A, Lattanzio VMT, Schena R, et al. Effect of alkaline cooking of maize on the content of fumonisins B1 and B2 and their hydrolysed forms [J]. Food Chemistry, 2016, 192: 1083-1089.
[5] Bartok T, Tolgyesi L, Mesterhazy A, et al. Identification of the first fumonisin mycotoxins with three acyl groups by ESI-ITMS and ESI-TOFMS following RP-HPLC separation: palmitoyl, linoleoyl and oleoyl EFB1 fumonisin isomers from a solid culture of Fusarium verticillioides[J]. Food Additives & Contaminants: Part A, 2010, 27(12): 1714-1723.
[6] Falavigna C, Lazzaro I, Galaverna G, et al. Oleoyl and linoleoyl esters of fumonisin B1 are differently produced by Fusarium verticillioideson maize and rice based media [J]. International Journal of Food Microbiology, 2016, 217: 79-84.
[7] Park J W, Scott P M, Lau BPY. Analysis of N-fatty acyl fumonisins in alkali-processed corn foods [J].Food Science and Biotechnology, 2013, 22(S): 147-152.
[8] Howard P C, Churchwell M I, Couch L H, et al. Formation of N-(Carboxymethyl)fumonisin B1, following the reaction of fumonisin B1 with reducing sugars [J]. Journal of Agricultural and Food Chemistry, 1998, 46(9): 3546-3557.
[9] Seefelder W, Hartl M, Humpf H U. Determination of N-(carboxymethyl) fumonisin B1 in corn products by liquid chromatography/electrospray ionization-mass spectrometry [J]. Journal of Agricultural and Food Chemistry, 2001, 49(5): 2146-2151.
[10] Dall’Asta C, Galaverna G, Aureli G, et al. A LC/MS/MS method for the simultaneous quantification of free and masked fumonisins in maize and maize-based products [J]. World Mycotoxin Journal, 2008, 1(3): 237-246.
[11] Hu L, Zhu H Q, Ni M L, et al. Free and hidden fumonisins in HordeiFructusGerminatus and their transfer to the decoction [J]. World Journal of Traditional Chinese Medicine, 2020, 6(1): 106-111.
[12] Andrade P D, Dias J V, Souza D M, et al. Mycotoxins in cereals and cereal-based products: Incidence and probabilistic dietary risk assessment for the Brazilian population [J]. Food and Chemical Toxicology, 2020, 143: 111572.
[13] Dall’Asta C, Falavigna C, Galaverna G, et al.In vitro digestion assay for determination of hidden fumonisins in maize [J].Journal of Agricultural and Food Chemistry, 2010, 58(22): 12042-12047.
[14] Schaarschmidt S, Fauhl-Hassek C. Mycotoxins during the processes of nixtamalization and tortilla production [J]. Toxins, 2019, 11, 227.
[15] Zimmer I, Usleber E, Klaffke H, et al. Fumonisin intake of the German consumer [J]. Mycotoxin Research, 2008, 24(1): 40-52.
[16] Hu L, Liu HW, Yang J, et al. Free and hidden fumonisins in raw maize and maize-based products from China [J]. Food Additives & Contaminants: Part B, 2019, 12(2): 90-96.
[17] Ezekiel C N, Sulyok M, Ogara I M, et al. Mycotoxins in uncooked and plate-ready household food from rural northern Nigeria [J]. Food and Chemical Toxicology, 2019, 128: 171-179.
[18] Hartl M, Humpf H U. Toxicity assessment of fumonisins using the brine shrimp (Artemiasalina) bioassay [J]. Food and Chemical Toxicology, 2000, 38: 1097-1102.
[19] Hahn I, Nagl V, Schwartz-Zimmermann HE. Effects of orally administered fumonisin B1 (FB1), partially hydrolysed FB1, hydrolysed FB1 and N-(1-deoxy-D-fructos-1-yl) FB1 on the sphingolipid metabolism in rats [J]. Food and Chemical Toxicology, 2015, 76: 11-18.
[20] Howard PC, Couch LH, Patton RE, et al. Comparison of the toxicity of several fumonisin derivatives in a 28-day feeding study with female B6C3F1 mice [J]. Toxicology and Applied Pharmacology, 2002, 185: 153-165.
[21] Voss K A, Riley R T, Snook M E, et al. Reproductive and sphingolipid metabolic effects of fumonisin B1 and its alkaline hydrolysis product in LM/Bc mice: hydrolyzed fumonisin B1 did not cause neural tube defects [J]. Toxicological Sciences, 2009, 112(2): 459-467.
[22] Norred W P, Plattner R D, Dombrink-Kurtzman M A, et al. Mycotoxin-induced elevation of free sphingoid bases in precision-cut rat liver slices: specificity of the response and structure-activity relationships [J]. Toxicology and Applied Pharmacology, 1997, 147: 63-70.
[23] Schmelz E M, Dombrink-Kurtzman M A, Roberts P C, et al. Induction of apoptosis by fumonisin B1 in HT29 cells is mediated by the accumulation of endogenous free sphingoid bases [J]. Toxicology and Applied Pharmacology, 1998, 148(2): 252-260.
[24] Gu M J, Han S E, Hwang K, et al. Hydrolyzed fumonisin B1 induces less inflammatory responses than fumonisin B1 in the co-culture model of porcine intestinal epithelial and immune cells [J]. Toxicology Letters, 2019, 305: 110-116.
[25] Meca G, Fernandez-Franzon M, Ritieni A, et al. Formation of fumonisin B1-glucose reaction product, in vitro cytotoxicity, and lipid peroxidation on kidney cells [J]. Journal of Agricultural and Food Chemistry, 2010, 58(2): 1359-1365.
[26] Harrer H, Laviad E L, Humpf H U, et al. Identification of N-acyl-fumonisin B1 as new cytotoxic metabolites of fumonisin mycotoxins [J]. Molecular Nutrition & Food Research, 2013, 57(3): 516-522.
[27] Abou-Karam M, Abbas H K, Shier W T. N-fatty acylation of hydrolyzed fumonisin B1, but not of intact Fumonisin B1, strongly enhances in vitro mammalian toxicity [J]. Journal of Toxicology: Toxin Reviews, 2004, 23(1): 123-151.







