CopyRight 2009-2020 © All Rights Reserved.版权所有: 中国海关未经授权禁止复制或建立镜像
HS-SPME-GC/MS法对化妆品中二噁烷残留量的检测研究
作者:唐熙 邱凌 陈旻实 刘华建 武敏建 陈清兰
唐熙 邱凌 陈旻实 刘华建 武敏建 陈清兰
二噁烷,学名:1,4-二氧己环,又名二氧六环,无色液体,稍有香味。短时接触该物质的液体或蒸汽会对人体有刺激性,尤其对眼、呼吸道刺激性较大;长期接触可能损害神经系统和肾脏、肝脏,属微毒类物质。二噁烷在工业中主要用作乳化剂、去垢剂及溶剂等。
化妆品不会直接使用二噁烷作为原料或添加剂,其主要来源是由所使用的表面活性剂引入的。表面活性剂中所含的聚氧乙烯醚物质,在生产过程中容易氧化而产生二噁烷。因此,尤其是沐浴露和洗发水等洗去类产品,如果使用了含有聚氧乙烯醚结构的非离子表面活性剂,基本都含二噁烷[1]。《化妆品安全技术规范》(2015年版)[2](以下简称《规范》)将二噁烷列为安全通用要求,规定其在最终产品中含量不得大于30 mg/kg。《规范》中对二噁烷的检测采用顶空-气质联用的方法,检测限为1.0 mg/kg。由于化妆品形态多样,主要有液态水基、膏霜、凝胶等形态,且成分复杂,含有大量香精等易挥发成分,顶空萃取过程大量挥发性杂质将对目标物分析产生巨大干扰,影响检测结果的准确性[3-4]。
作为一种新型快速有效的萃取分离技术,固相微萃取(SPME)是固相萃取技术发展应用的一大进步。其原理来源于固相萃取,但其所拥有的操作简便、样品用量小、无需使用溶剂,以及萃取后直接色谱进样等优点是传统固相萃取技术无可比拟的,因此,固相微萃取虽然应用只有十多年,但已经涉及所有有机化学样品分析[5]。固相微萃取在实际操作时可以根据样品性质采用3种萃取方式,包括直接萃取(主要用于气态和液态样品)、膜保护萃取(主要用于固态样品)和顶空萃取(主要用于液态和固态样品)。3种萃取方式中应用最为广泛的是顶空萃取,这种萃取方式的优势在于最大程度减少样品基质中不挥发和难挥发物质造成的本底干扰。本研究采用顶空固相微萃取-气质联用技术对化妆品中的二噁烷进行检测,与《规范》方法相比,检测时间缩短,灵敏度有较大的提高,且抗干扰能力强,大大提高检测结果的准确度。
1 实验部分
1.1 仪器与试剂
气相色谱质谱联用仪:Agilent7890-5975C(美国安捷伦科技公司);固相微萃取进样手柄和75 μm PDMS 固相微萃取头(美国Supelco公司);恒温加热块(Dry Block 德国IKA公司);漩涡混合器(MS3 德国IKA公司);电子天平(AE240梅特勒公司);超纯水系统(MILIPORE,美国密理博公司)。
二噁烷标准品(德国Ehrenstorfer公司,纯度为99.5%,CAS No.123-91-1)。
1.2 标准溶液的配制
准确称取二噁烷标准样品,用超纯水溶解,配制成1000 μg/mL的标准储备液。准确移取一定量标准储备液,用超纯水配制成系列标准工作溶液。
1.3 实验方法
1.3.1 实验步骤
称取化妆品试样1.0 g(精确至0.001 g),置于20 mL螺纹顶空瓶中,准确移取5 mL超纯水,密封漩涡混匀后,置于加热块中70℃平衡10 min。随后将预先老化好的萃取头插入顶空瓶上部空间,萃取10 min。拔出萃取头,插入气质联用进样口,250℃下热解吸5 min。
1.3.2 仪器参数
色谱条件:HP-5MS毛细管色谱柱(30 m×0.25 mm×0.25 μm);进样口温度:250℃,分流比为2:1;升温程序:初始温度60℃,维持0.5 min;以10℃/min的升温速率升至200℃,维持2 min;然后以15℃/min的升温速率升至240℃,维持5 min;载气:高纯氦;流速:1.0 mL/min。
质谱条件:电离源(EI);电离能量:70 eV;气相-质谱接口温度:250℃;EI源温度:230℃;四级杆质量分析器温度:150℃;EI源开启时间:0 min;选择离子扫描(SIM),检测离子(m/z):88、58、43,其中88为定量离子。
2 结果讨论
2.1 色谱和质谱条件的优化
考察了不同极性色谱柱(极性:HP-INNOWAX,弱极性:HP-5,非极性:HP-1)对二噁烷的分离效果。结果表明,极性柱对二噁烷有较强的吸附性,色谱峰拖尾严重。二噁烷在非极性和弱极性柱上色谱峰型对称,但非极性柱对杂质分离效果不佳,容易在二噁烷出峰位置对检测造成干扰。综合考虑,选择弱极性柱(HP-5)作为色谱分离柱;采用全扫描方式对二噁烷标准溶液进行质谱分析,找出特征离子峰(m/z)为88、58、43;其中88信号最强,作为定量离子。
2.2 固相微萃取头涂层的选择
萃取头涂层是固相微萃取技术的关键,选择的原则是使目标化合物吸附于涂层之上,而干扰化合物与溶剂不吸附或少吸附,从而达到富集净化的目的。目前商品化的萃取头涂层有PDMS(非极性)、CAR/PDMS(石墨化炭黑吸附)、DVB/PDMS(弱极性)、PA(极性)。根据二噁烷能与水及多种有机溶剂相溶,极性稍弱于丙酮的性质,我们对比了上述4种涂层对二噁烷的萃取能力,见图1。从实验结果看,PDMS/DVB和PA涂层对二噁烷的萃取能力明显弱于PDMS和CAR/PDMS涂层,CAR/PDMS涂层萃取能力最优,说明CAR/PDMS涂层对二噁烷具有很强的吸附能力。但从总离子流图分析,CAR/PDMS涂层得到的谱图较PDMS涂层杂乱(见图2~3),说明CAR/PDMS涂层吸附的选择性不够好,在吸附目标物的同时,过多的杂质亦一并吸附,干扰影响较大;且实验过程中发现,使用CAR/PDMS涂层进行几次萃取后,必须对其进行高温老化处理,以消除残留。本实验综合考虑,选择PDMS涂层对二噁烷进行萃取。
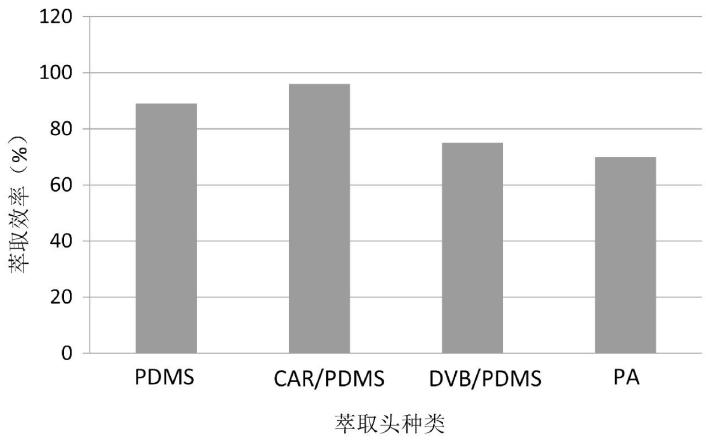
图1 不同种类萃取头对二噁烷的萃取能力
Fig.1 Effects of different extraction heads for dioxane
2.3 顶空平衡温度和萃取时间的优化
提高顶空体系的温度可以加快分子运动,使样品中挥发组分更快更完全逸散在样品上方的气体中,从而缩短平衡时间。但提高温度并不能对体系中所有化合物的灵敏度都有等效提高。同时固相微萃取是一个吸附-解吸的动态平衡过程,高温会使平衡往解吸方向移动,不利于待测化合物的富集。此外,高温也会增强体系中其他物质的挥发度,从而产生较大的背景干扰。《规范》方法中顶空平衡的温度设置为70℃。实验考察了不同顶空体系温度下对二噁烷的检测影响,见图4。由实验结果可知,萃取效率总体随温度升高而增加,70℃以上的萃取效率提升趋缓,因此,我们选择70℃作为顶空平衡温度。
图2 PDMS萃取物的总离子流图
Fig.2 TIC of extracts for PDMS
图3 CAR/PDMS萃取物的总离子流图
Fig.3 TIC of extracts for CAR/PDMS
顶空固相微萃取过程中,被分析物从气相转移至萃取固定相的速率远大于被分析物从液体/固体扩散至气相中的速率。根据这一性质,在相同条件下,顶空固相微萃取的时间少于普通顶空萃取。实验也证明了这一点,考察不同萃取时间下对二噁烷的检测影响,见图5。从结果分析可知,萃取效率在10 min左右达到最优,相比《规范》方法中40 min的平衡时间大为缩短,故我们选择萃取时间为10 min。
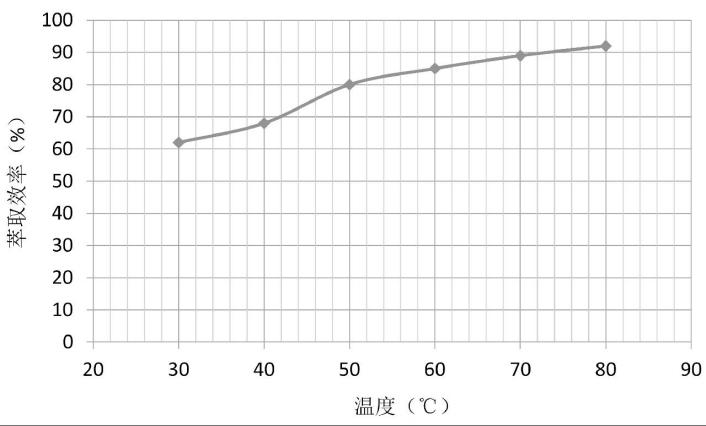
图4 平衡温度对结果的影响
Fig.4 Effects of equilibrium temperature

图5 萃取时间对结果的影响
Fig.5 Effects of extraction time
2.4 热解吸温度的优化
热解吸过程必须迅速且彻底。热解吸温度过低或解吸时间不够,会造成分析物在涂层中的残留,影响后续分析。但同时解吸温度太高会影响涂层的寿命。本实验对热解吸温度和时间进行比较,考察变化趋势,见图6。从结果分析可知,解吸温度越高,回收率越好,250℃进行解吸,回收率已达95%,随着温度上升,回收率继续增加,但趋于平稳。PDMS涂层使用温度上限为280℃,太接近温度上限,将缩短萃取头的使用寿命。本实验对二噁烷含量为50 mg/kg的样品进行萃取,250℃下解吸5 min,完成进样分析。将此萃取头在250℃下再次解吸5 min;对比分析两次进样的色谱图,第二次进样未检测出二噁烷,说明在250℃下解吸5 min,所吸附的二噁烷已解吸完全,不会对后续分析产生影响。
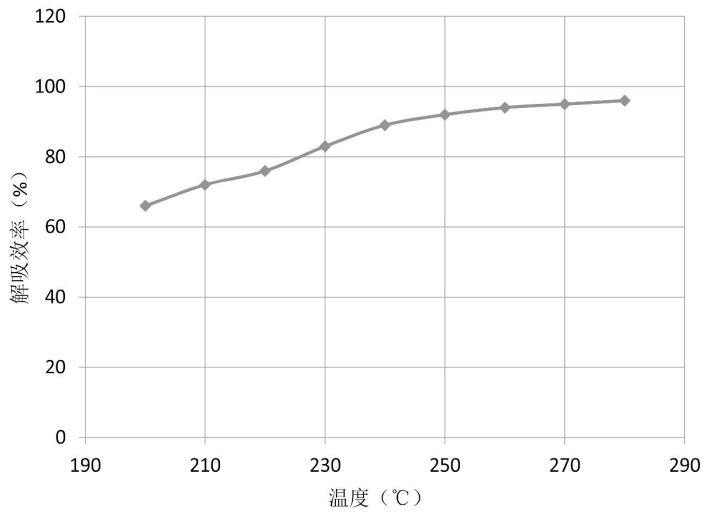
图6 热解吸温度对结果的影响
Fig.6 Effects of thermal desorption temperature
2.5 检测低限、定量限和线性
取经检测不含二噁烷的化妆品样品作为空白基质,分别往基质中加入二噁烷标准工作液,使基质中二噁烷浓度为0.5 mg/kg 、1.0 mg/kg、2.0 mg/kg、5.0 mg/kg、10.0 mg/kg,上机测定。以二噁烷浓度x与二噁烷定量离子色谱峰面积y进行线性拟合,绘制基质标准曲线,得到良好的线性关系,其相关系数r为0.9994。
取经检测不含二噁烷的化妆品样品,添加一定浓度的二噁烷标准工作液,测定方法检测低限和定量限。用公式LOD=3 S/N和LOQ=10 S/N分别计算检出限(LOD)和定量限(LOQ)。其中S/N为检测器信噪比,计算得出二噁烷的LOD为0.2 mg/kg,LOQ为0.5 mg/kg(表1)。
2.6 回收率和精密度
取3类不含二噁烷的化妆品样品(口红、沐浴液、润肤乳),往其中添加一定量的二噁烷标准工作液,每个样品添加3个浓度,每个添加水平平行测试6次,按“1.3”所述方法进行处理,计算回收率与相对标准偏差(RSD),见表2。
表1 二噁烷的线性范围、线性方程、相关系数、检出限和定量限
Table 1 Linear range, linear equation, correlation coefficient, limit of detection and limit of quantification of dioxane
(mg/kg) | 线性方程 | 相关系数 | (mg/kg) | (mg/kg) |
0.5~10 | y=230x+38.7 | 0.9994 | 0.2 | 0.5 |
表2 二噁烷回收率和相对标准偏差
Table 2 Dioxane recovery rate and relative standard deviation
样品 | 添加浓度 (mg/kg) | 回收率 (%) | RSD (%) |
口红 | 0.8 | 85.6 | 4.5 |
2.0 | 90.5 | 3.1 | |
5.0 | 93.1 | 2.6 | |
沐浴液 | 0.8 | 87.4 | 3.7 |
2.0 | 89.3 | 2.4 | |
5.0 | 94.0 | 1.9 | |
润肤乳 | 0.8 | 88.7 | 4.0 |
2.0 | 91.6 | 3.5 | |
5.0 | 93.3 | 2.3 |
2.7 实际样品的测定
随机选取市售化妆品及化妆品原料共5份,按照建立的方法对其进行二噁烷的测定。洗去类产品存在微量二噁烷,原料中二噁烷含量较高,但都未超出《规范》30 mg/kg的限量要求,见表3。
3 结论
本文建立了顶空固相微萃取-气质联用技术测定化妆品中的二噁烷,优化了固相微萃取萃取头涂层,热平衡温度、时间,热解吸温度、时间等实验条件,并进行了方法学评价。结果表明,二噁烷在质量浓度0.5~10 mg/kg范围内的相关系数为0.9994,方法定量限为0.5 mg/kg。相比《规范》对二噁烷的检测标准,该方法既克服了化妆品种类多、成分复杂给检测带来的不利影响,同时降低了检测限,为了解化妆品质量安全提供了一种快捷准确的方法。
参考文献
[1] BLACK R E, HURLEY F J, HAVERY D C. Occurrence of 1,4-dioxane in cosmetics raw materials and finished cosmetic products[J]. J AOAC Int, 2001, 84(3): 666-670.
[2]国家食品药品监督管理总局. 关于发布化妆品安全技术规范(2015年版)的公告(2015年第268号) [EB/OL]. (2015-12-23)http://www.sda.gov.cn/WS01/CL0087/140161.html
[3]张智宏, 孙晓娟. 烷基醇聚氧乙烯醚中1,4-二噁烷的测定[J]. 色谱, 1998, 16(3): 244-246.
[4]马健, 钱春英, 陈建华. 顶空气相色谱法测定醇醚硫酸盐中1,4-二噁烷的含量[J]. 表面活性剂工业, 2000, 2: 41-43.
[5]奚星林, 鲍伦军, 等. 化妆品及其原料中的1,4-二噁烷的测定[J]. 日用化学工业, 2003, 33(6): 390-392.
[6]张永祥, 高继民, 王然, 等. 顶空固相微萃取-气相色谱法测定水中1,4-二氯苯[J]. 工业水处理, 2013, 33(9): 76-79.
[7]王玉飞, 李继革, 施家威. 顶空固相微萃取-气相色谱法测定水中痕量多氯酚[J]. 中国卫生检验杂志, 2013, 23(14): 2891-2892.
[8]杜仁军, 曹志斌, 王晋宇, 等. 顶空固相微萃取-气相色谱法测定水中四乙基铅[J] . 理化检验-化学分册, 2013, 49(6): 691-696.
[9]李建勋, 杜丽平, 王超, 等. 顶空固相微萃取-气质联用法分析黑茶香气成分[J] .食品科学, 2013, 34(1): 1-8.
[10]周围, 魏玉梅, 毕阳. 顶空固相微萃取气相色谱质谱联用技术[C]. 首届中日西部地区色谱学术交流会论文集, 2006: 8.







