CopyRight 2009-2020 © All Rights Reserved.版权所有: 中国海关未经授权禁止复制或建立镜像
甘草提取物中赭曲霉毒素A标准物质的研制
作者:胡玲 莫超琳 夏才军 徐晓 黄昕
胡玲 莫超琳 夏才军 徐晓 黄昕
赭曲霉毒素A(ochratoxin A,OTA)是一种广泛存在于谷物、香料、葡萄酒等多种农产品中的真菌毒素,主要由曲霉属(Aspergillus)和青霉属(Penicillium)真菌产生,具有肾毒、基因毒性等,可致癌[1-3],已被国际癌症研究机构(International Agency for Research on Cancer,IARC)列为2B类致癌物[4]。
甘草和甘草提取物,由于其药用和保健价值,海内外市场广阔,但易受到OTA污染。目前,我国对甘草及其制品中的OTA尚未出台限量标准。欧盟于2010年规定甘草和甘草提取物中OTA的限量分别为20 μg/kg和80 μg/kg[5]。若出口的甘草提取物中OTA含量超标,容易受到欧盟食品和饲料类快速预警系统(RASFF)[6]通报并予以退货、销毁等处理。
准确测定甘草提取物中OTA的含量,是保障其质量的重要手段之一。由于甘草提取物基质成分复杂,给OTA的准确定量带来了一定难度,在检测过程中单纯使用纯品标准物质难以保证结果的可靠性。基体标准物质作为一种具有实际样品特性的标准物质,其性质与实际样品较纯品标准物质更为接近,因而在检测过程中使用基体标准物质作为质控样有助于提高检测结果的准确性[7]。
1 材料与方法
1.1 仪器和试剂
AB SciexQtrap 5500串联质谱仪(美国ABSciex公司);LC-30AD高效液相色谱仪(日本Shimadze公司);氮吹仪(美国Organomation公司);Sorvall ST 40R离心机(美国Thermo公司);XS205万分之一天平(瑞士梅特勒-托利多公司);Multi Reax振荡器(德国Heidolph公司);Vortex Genie2(美国Scientific Industries公司);超声波清洗器(上海科导公司);Milli-Q超纯水仪(美国Millipore公司)。
甲醇、甲酸(色谱纯,美国Tedia公司);磷酸盐缓冲液(PBS,pH 7.2,德国Merck公司);水为自制Milli-Q超纯水。OTA免疫亲和柱(奥地利Romer Labs公司);0.22 μm尼龙滤膜(北京迪马公司)。标准品:OTA溶液标准物质(1.9 μg/mL,国家粮食和物资储备局科学研究院);[13C20]-OTA内标溶液(10 μg/mL,奥地利Romer Labs公司)。
1.2 实验方法
1.2.1 样品前处理
称取甘草提取物样品粉末5.0 g(精确至0.001 g),用移液管准确加入25 mL甲醇-水(80∶20,v/v)溶液,振荡提取60 min,5000 r/min离心5 min,取1 mL上清,用10 mL容量瓶定容后取1 mL稀释液,加入4 ng [13C20]-OTA(200 μL×20 ng/mL)和4 mL PBS过免疫亲和柱,用2×10 mL PBS冲洗,再用3 mL甲醇洗脱OTA,洗脱液用氮吹仪浓缩至约1.0 mL,过0.22 μm滤膜,用于上机检测。
1.2.2 高效液相色谱-串联质谱检测条件
安捷伦Eclipse XDB-C8色谱柱(4.6 mm×150 mm,5μm);液相色谱流动相为0.1%甲酸水溶液(A)-甲醇(B);质谱采用电喷雾电离(ESI)离子源,正离子扫描,多反应监测(MRM)模式。配制OTA∶[13C20]-OTA浓度比分别为1∶10至10∶1的系列标准溶液,以OTA∶[13C20]-OTA浓度比为横坐标,以两者峰面积比为纵坐标,建立标准曲线,内标法定量。具体检测参数、标准曲线绘制及含量计算公式参照文献[8]。
2 甘草提取物中赭曲霉毒素A样品的制备
选取在自然条件下受OTA污染甘草的干燥根和根茎为原料,根据《中华人民共和国药典》甘草浸膏(licorice extract)的制法[9],润透,切片,加水煎煮3次,每次2 h,合并水煎液,放置过夜使沉淀,取上清液,经喷雾干燥使成细粉,即得粉末状甘草提取物,105℃烘干2 h。为保证样品的均匀性,再经混匀仪混匀后,在分装前从中随机抽取15份样品(每份5 g),进行均匀性初检,合格后分装成30 g/袋的最小包装单元,其内层为聚乙烯(PE)自封袋,外层为铝箔袋并用封口机热封。共制备300袋,于4℃冷藏保存,后续从中随机抽取样品进行均匀性评估、稳定性评估以及定值。
3 均匀性评估
从总共300袋甘草提取物中随机抽取m袋样品(m = 15),每袋取n个子样(n = 3),按照1.2节中所述方法测定其中的OTA(测定值见表1),采用单因素方差分析法对测定结果进行统计分析,具体结果见表2。其中,总平均值 ,组间差方和
,组间差方和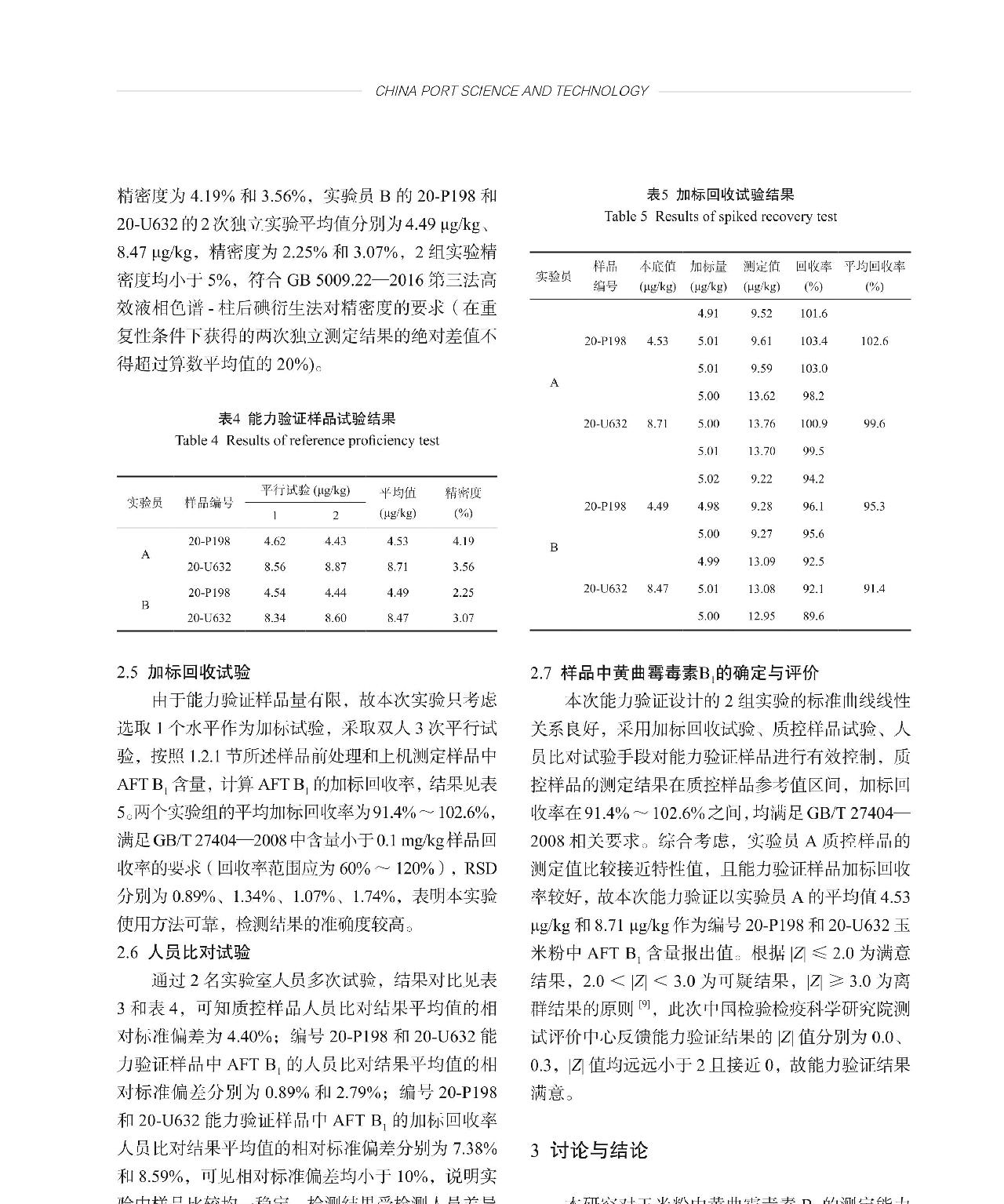 ,组内差方和
,组内差方和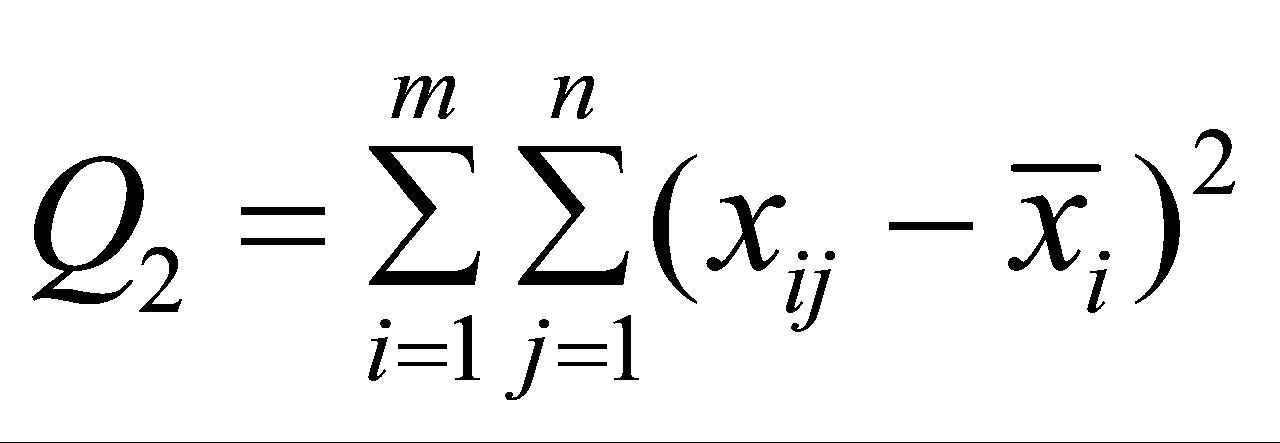 ,组间自由度
,组间自由度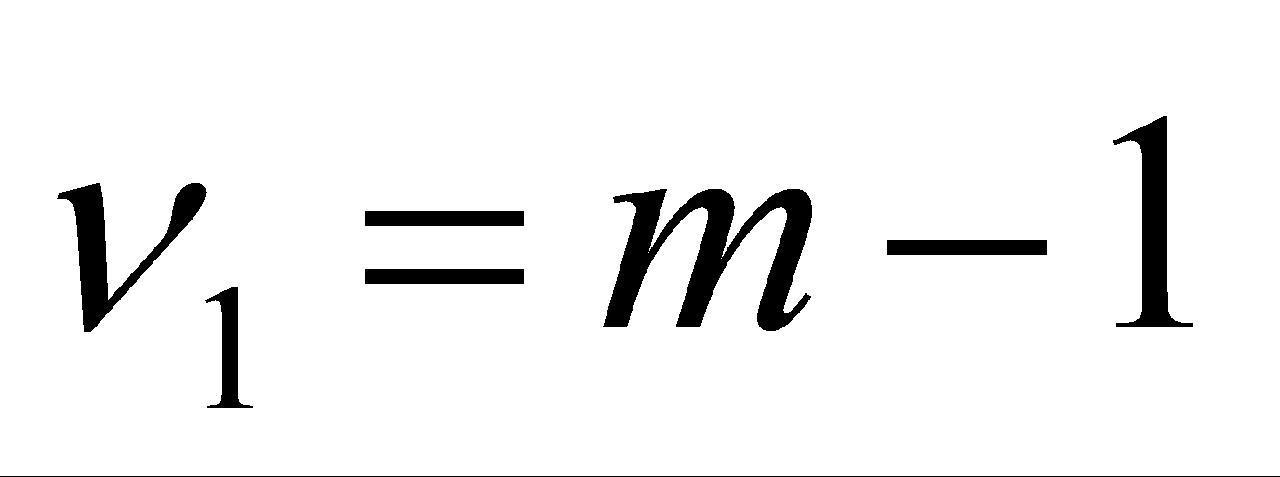 ,组内自由度
,组内自由度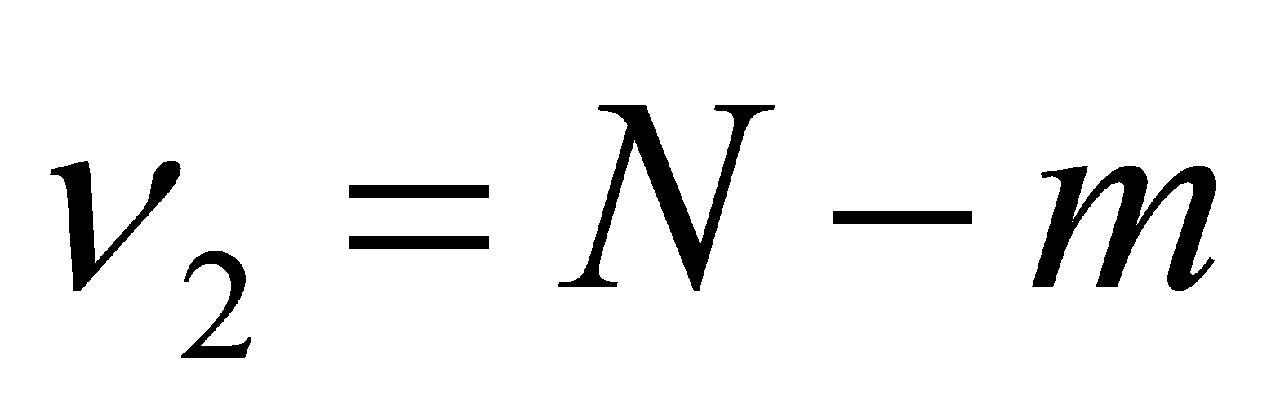 (N为总测量数),组间方差
(N为总测量数),组间方差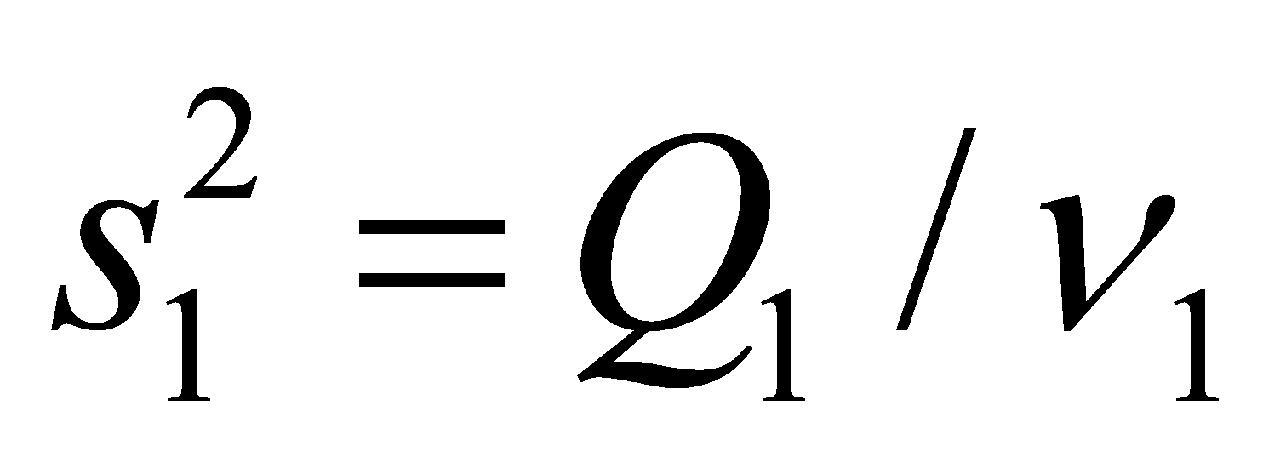 ,组内方差
,组内方差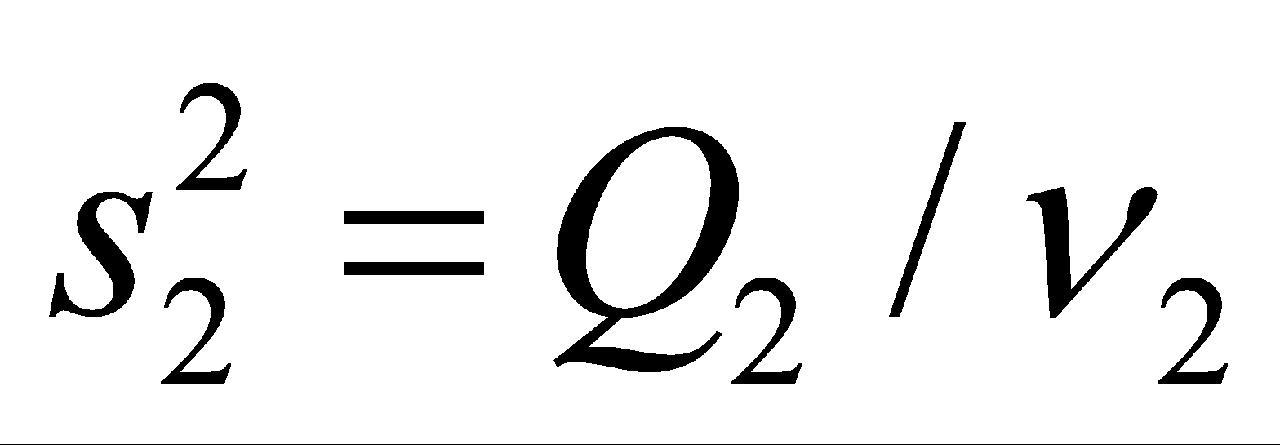 。根据以上结果,作统计量
。根据以上结果,作统计量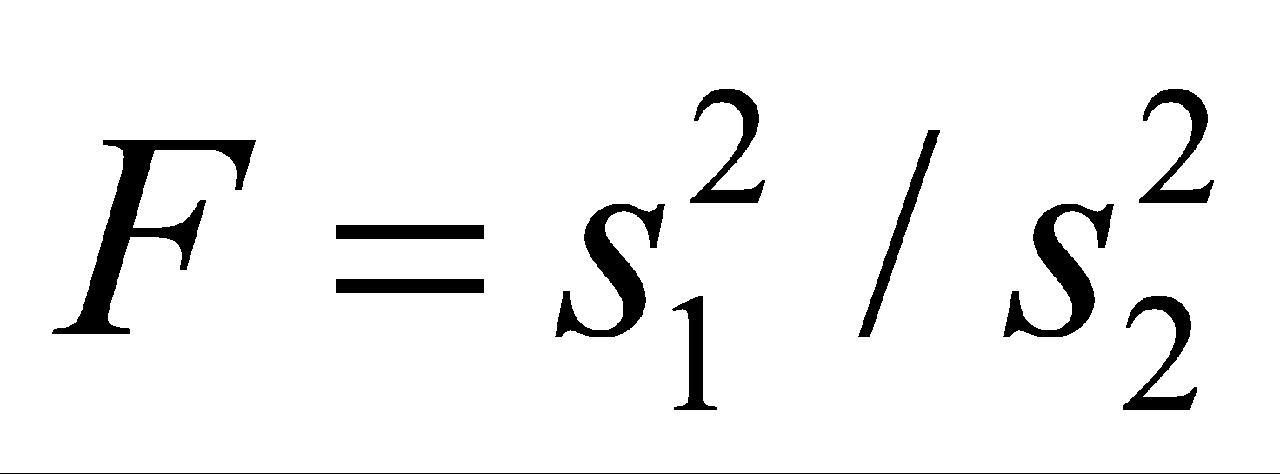 。F值小于临界值F0.05(14,30),因此,判断该标准物质的均匀性符合要求。
。F值小于临界值F0.05(14,30),因此,判断该标准物质的均匀性符合要求。
表1 均匀性评估OTA测定值
Table 1 OTA levels determined in homogeneity evaluation
样品编号 | OTA (μg/kg) | (μg/kg) | ||
子样1 | 子样2 | 子样3 | ||
1 | 84.0 | 84.3 | 88.1 | 85.4 |
2 | 83.1 | 86.8 | 84.4 | 84.8 |
3 | 82.4 | 82.0 | 84.6 | 83.0 |
4 | 80.0 | 87.0 | 86.6 | 84.5 |
5 | 76.9 | 78.5 | 83.2 | 79.5 |
6 | 84.6 | 89.8 | 87.6 | 87.3 |
7 | 83.4 | 82.0 | 85.9 | 83.8 |
8 | 84.6 | 89.2 | 88.8 | 87.6 |
9 | 82.6 | 81.0 | 80.1 | 81.2 |
10 | 83.5 | 83.2 | 84.8 | 83.8 |
11 | 85.5 | 84.4 | 88.0 | 86.0 |
12 | 90.0 | 84.2 | 84.3 | 86.2 |
13 | 87.8 | 81.3 | 85.0 | 84.7 |
14 | 87.4 | 85.6 | 83.7 | 85.6 |
15 | 86.8 | 86.6 | 79.8 | 84.4 |
4 稳定性评估
4.1 长期稳定性评估
根据先密后疏的原则,分别于第0个月、第1个月、第2个月、第4个月、第7个月,随机抽取3袋样品测定OTA(测定值见表3),每个时间点的测量结果取该时间点3个样品测量结果的平均值,结果见表4。由于甘草提取物中OTA的潜在动力学机理未知,故采用经典线性模型进行稳定性评估: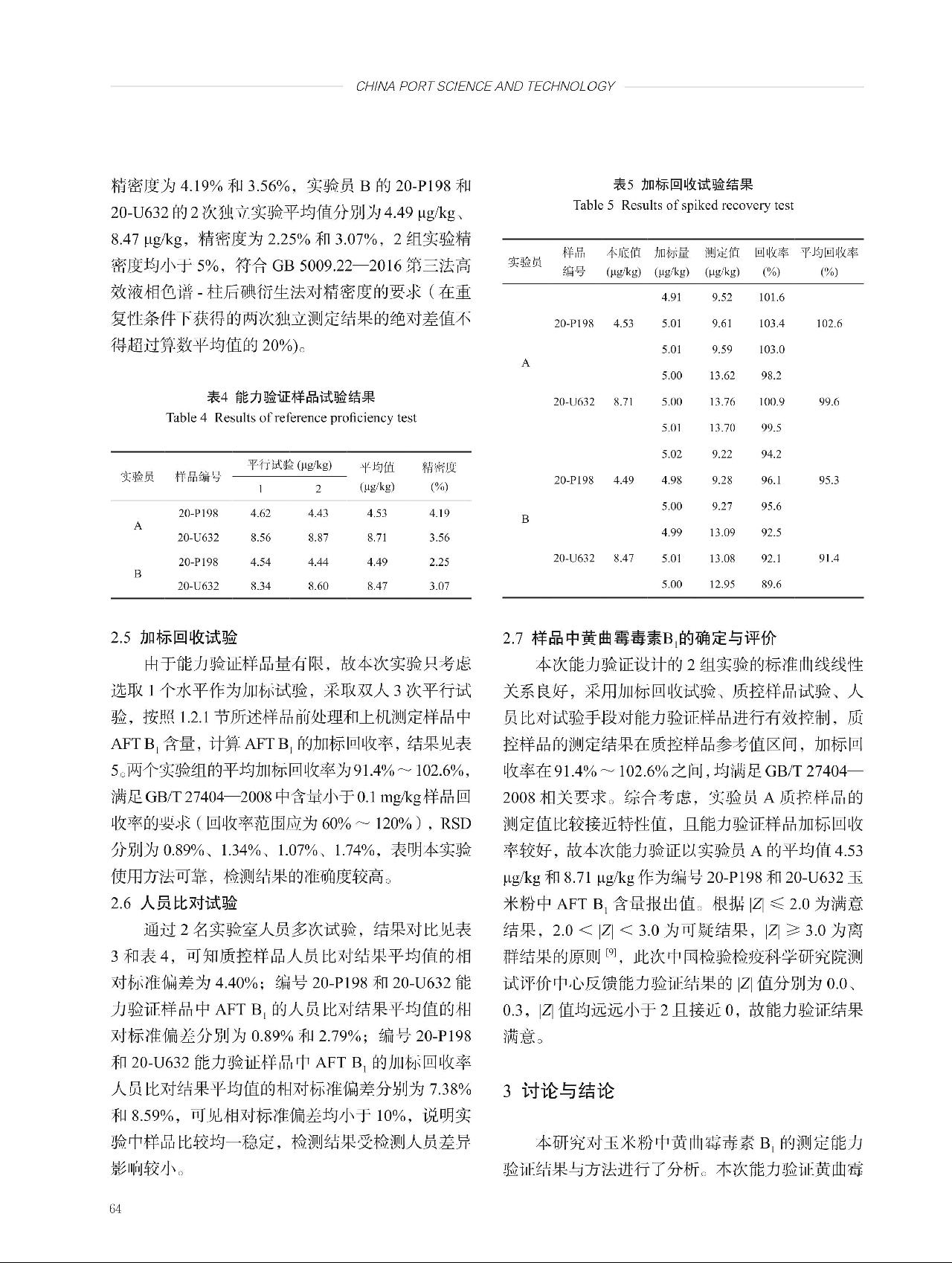 。式中,β0、β1为回归系数,X为时间,Y为标准物质候选物的特性值。斜率
。式中,β0、β1为回归系数,X为时间,Y为标准物质候选物的特性值。斜率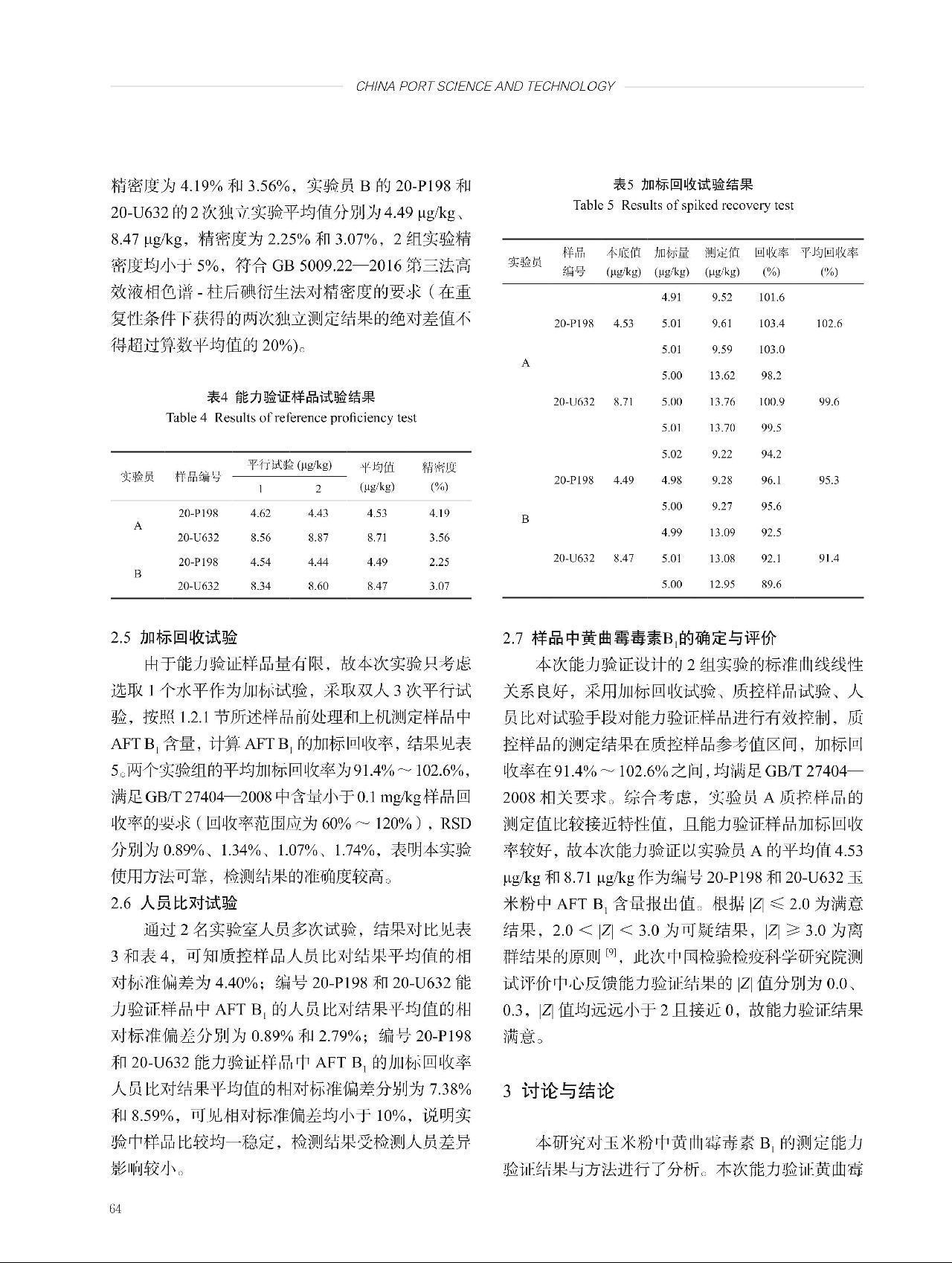 ,式中,Xi为第i个时间点,Yi为第i个时间点的观测值,
,式中,Xi为第i个时间点,Yi为第i个时间点的观测值, 为所有时间点的平均值,
为所有时间点的平均值,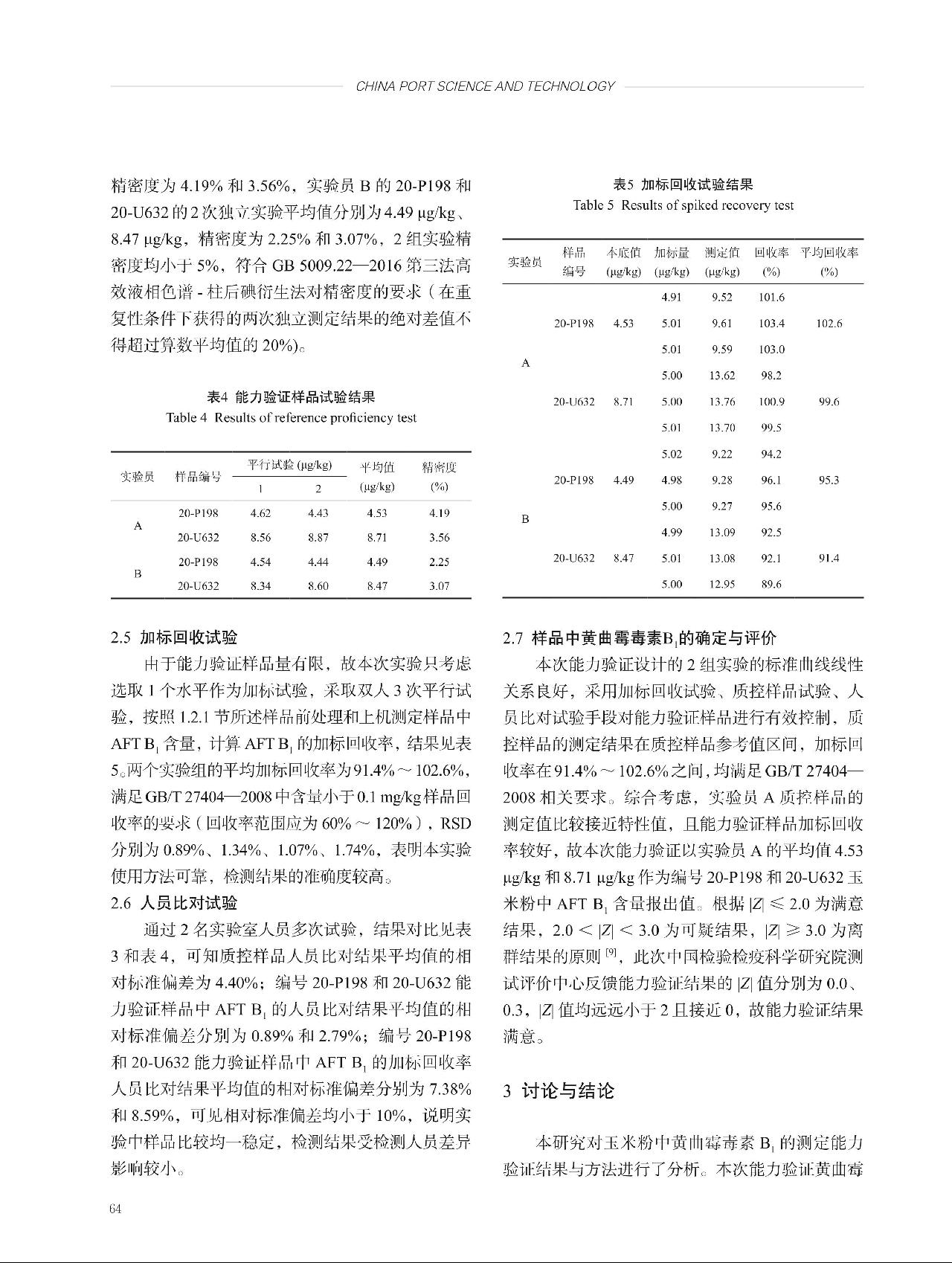 为所有观测值的平均值。截距
为所有观测值的平均值。截距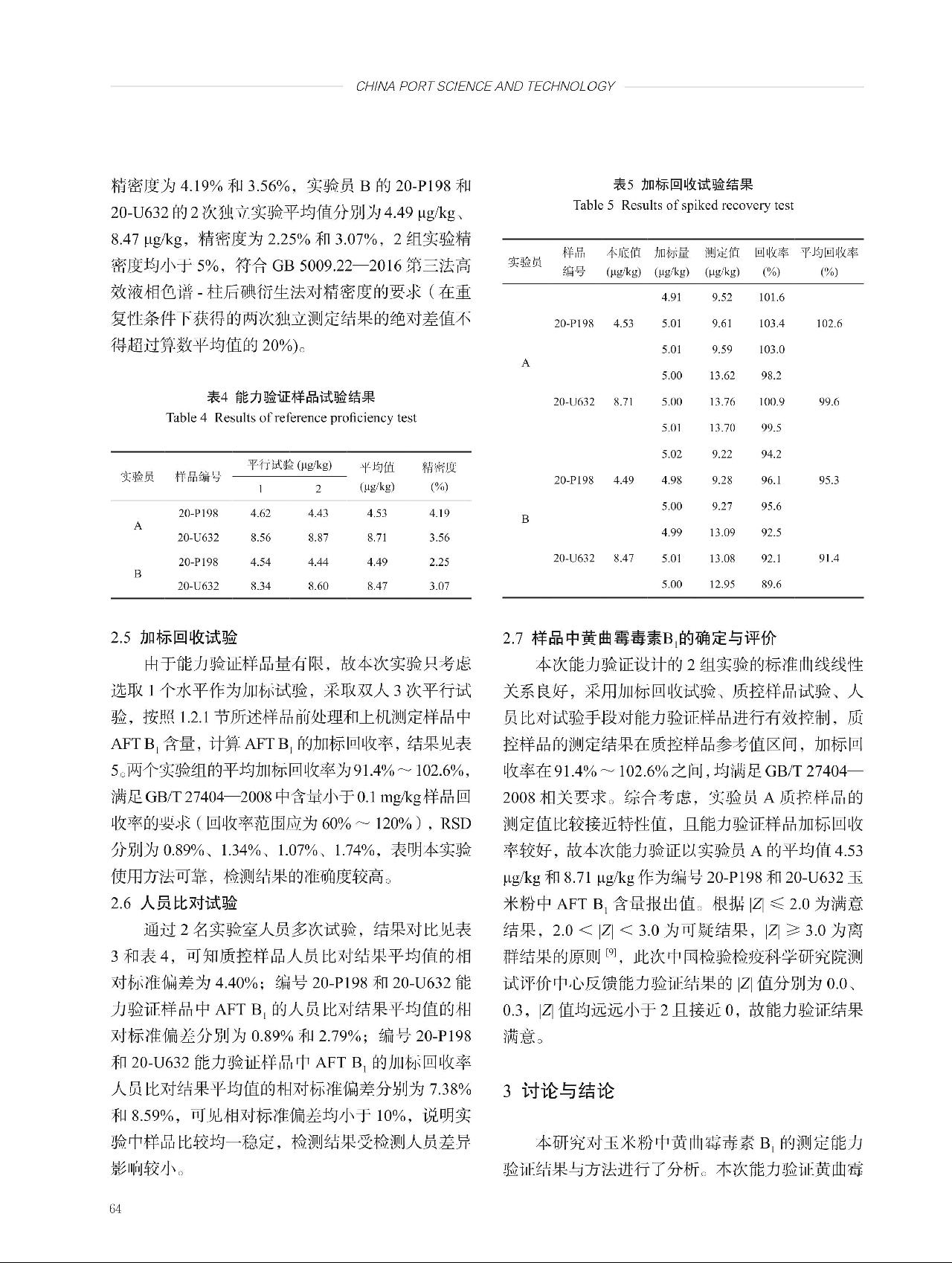 。基于β1和β1的标准偏差,根据t检验评估稳定性。依据表4中的数据,│β1│= 0.661,计算得t(0.05, 3)·s(β1) = 1.24,查t临界值表得t(0.05, 3) = 3.18,结果满足│β1│<t(α, n-2)·s(β1),表明甘草提取物中的OTA在本研究考察时间范围内是稳定的。
。基于β1和β1的标准偏差,根据t检验评估稳定性。依据表4中的数据,│β1│= 0.661,计算得t(0.05, 3)·s(β1) = 1.24,查t临界值表得t(0.05, 3) = 3.18,结果满足│β1│<t(α, n-2)·s(β1),表明甘草提取物中的OTA在本研究考察时间范围内是稳定的。
表3 长期稳定性评估OTA测定值
Table 3 OTA levels determined in long-term stability evaluation
评估时间点 | OTA平均值 (μg/kg) |
第0月 | 84.6 |
第1月 | 87.9 |
第2月 | 89.5 |
第4月 | 86.3 |
第7月 | 91.3 |
4.2 短期稳定性评估
短期稳定性考察标准物质在运输过程中的稳定性。本研究在60℃烘箱中模拟运输过程中可能出现的极端高温条件,随机抽取12袋样品置于烘箱中,分别于第0天、第2天、第7天、第14天取出3个样品,放入4℃冰箱中,于第14天统一按照1.2节中所述的方法测定其中的OTA(测定值见表5)。结果判定方法同长期稳定性评估方法。根据表6数据,│β1│= 0.216,计算得t(0.05, 3)·s(β1) = 0.82,查t临界值表得t(0.05, 2) = 4.30,结果满足│β1│<t(α, n-2)·s(β1),表明甘草提取物中的OTA在60℃下存放14 天是稳定的,极端高温条件下可以运输。
表4 长期稳定性评估参数值
Table 4 Long-term stability evaluation parameter values
统计量 | 计算值 |
β1 | 0.661 |
β0 | 86.040 |
s2 | 4.695 |
s(β1) | 0.390 |
表5 短期稳定性评估OTA测定值
Table 5 OTA levels determined in short-term stability evaluation
评估时间点 | OTA平均值 (μg/kg) |
第0天 | 87.7 |
第2天 | 83.4 |
第7天 | 85.5 |
第14天 | 83.0 |
表6 短期稳定性评估参数值
Table 6 Short-term stability evaluation parameter values
统计量 | 计算值 |
β1 | -0.216 |
β0 | 86.123 |
s2 | 4.280 |
s(β1) | 0.191 |
5 定值
采用同位素稀释高效液相色谱-串联质谱法,由8家实验室合作定值,每个实验室测定4袋样品,每袋取2个子样测定。
合并8家实验室定值结果,对合并后的64个数据进行Shapiro-Wilk正态性检验(置信概率取95%),结果表明,P值为0.106,大于0.05,故判断各组数据均服从正态分布。将每家实验室的测量结果作为一组独立数据,用格拉布斯(Grubbs)法和狄克逊(Dixon)法检验是否存在异常值,结果表明均无异常值,故全部予以保留。用科克伦(Cochran)法对各组数据进行等精度检验,结果表明各组数据等精度。将表7中各组数据平均值再次计算平均值,求出总平均值,即为标准值83.2 μg/kg。
表7 多家实验室合作定值结果
Table 7 Results of multi-laboratory collaborative valuation
实验室编号 | 组内均值 (μg/kg) | 组内RSD (%) |
实验室1 | 82.3 | 6.1 |
实验室2 | 78.0 | 3.2 |
实验室3 | 87.7 | 6.1 |
实验室4 | 85.5 | 5.8 |
实验室5 | 82.0 | 5.6 |
实验室6 | 86.3 | 5.0 |
实验室7 | 84.4 | 4.1 |
实验室8 | 79.3 | 3.9 |
6 不确定度评定
定值结果的不确定度由3个部分组成,分别为不均匀性引入的不确定度、不稳定性引入的不确定度、定值过程引入的不确定度。
6.1 不均匀性引入的不确定度评定(ubb)
根据表1中的均匀性检验结果,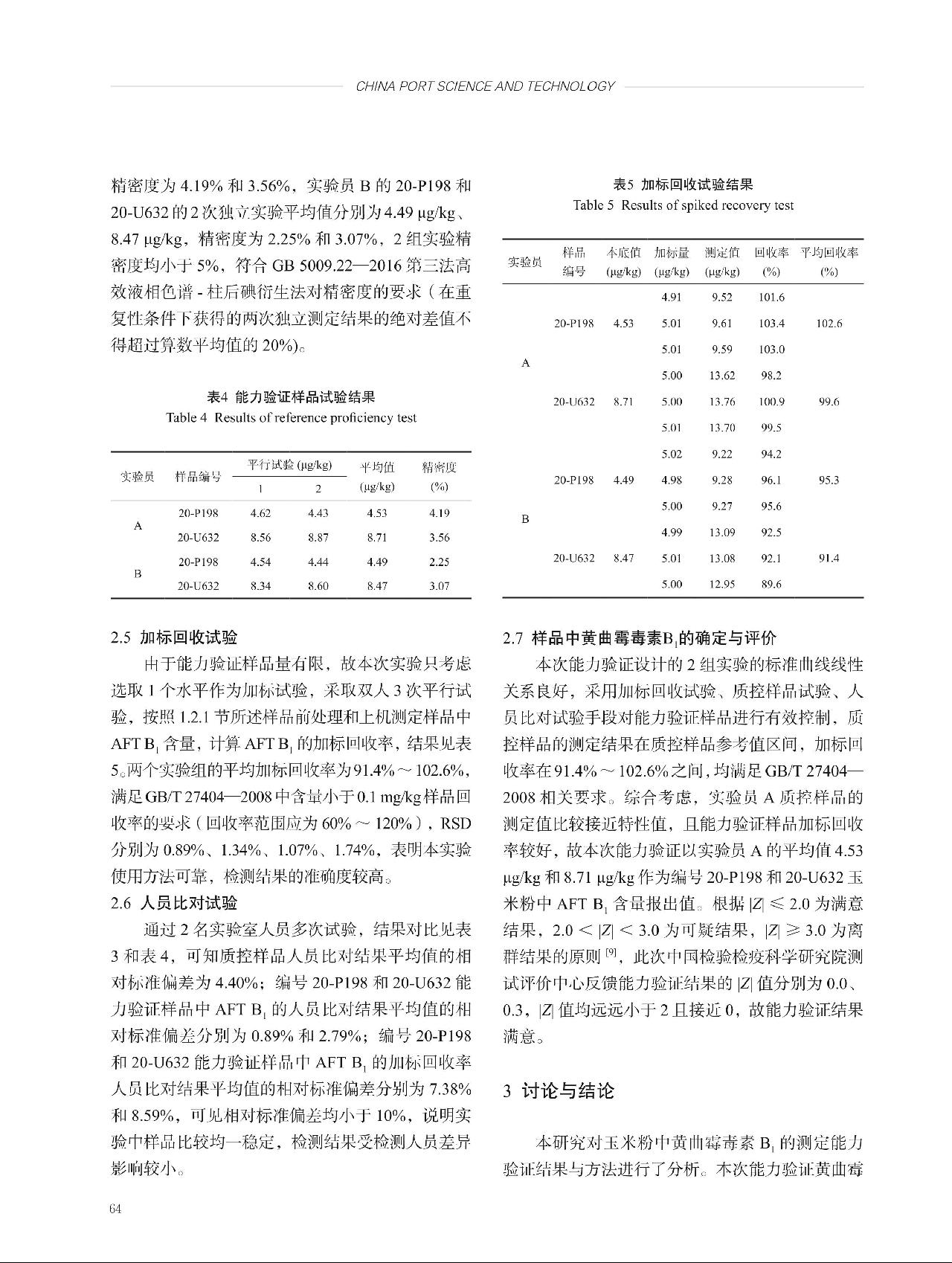 = 13.53,
= 13.53,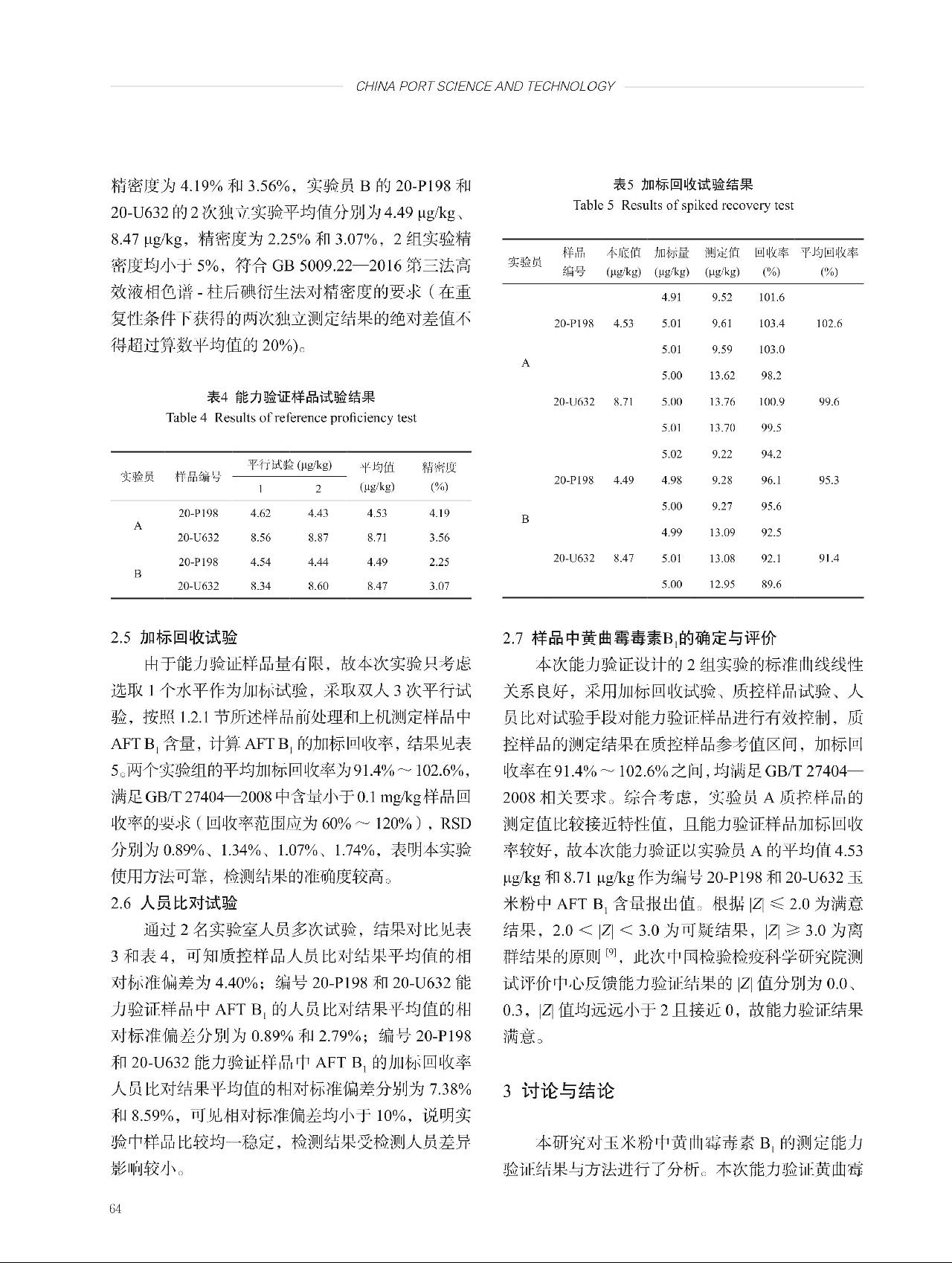 = 6.71,即
= 6.71,即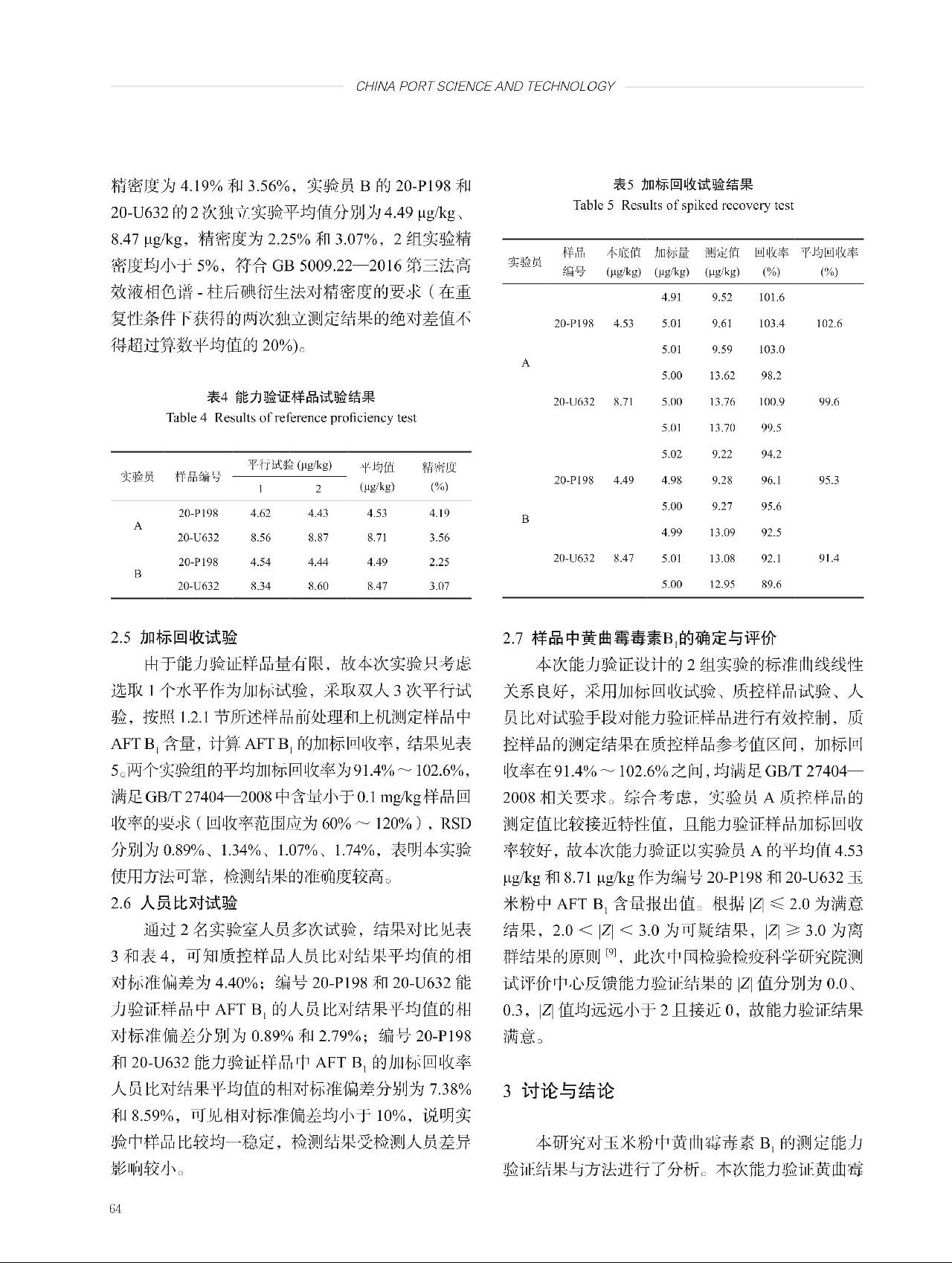 >
>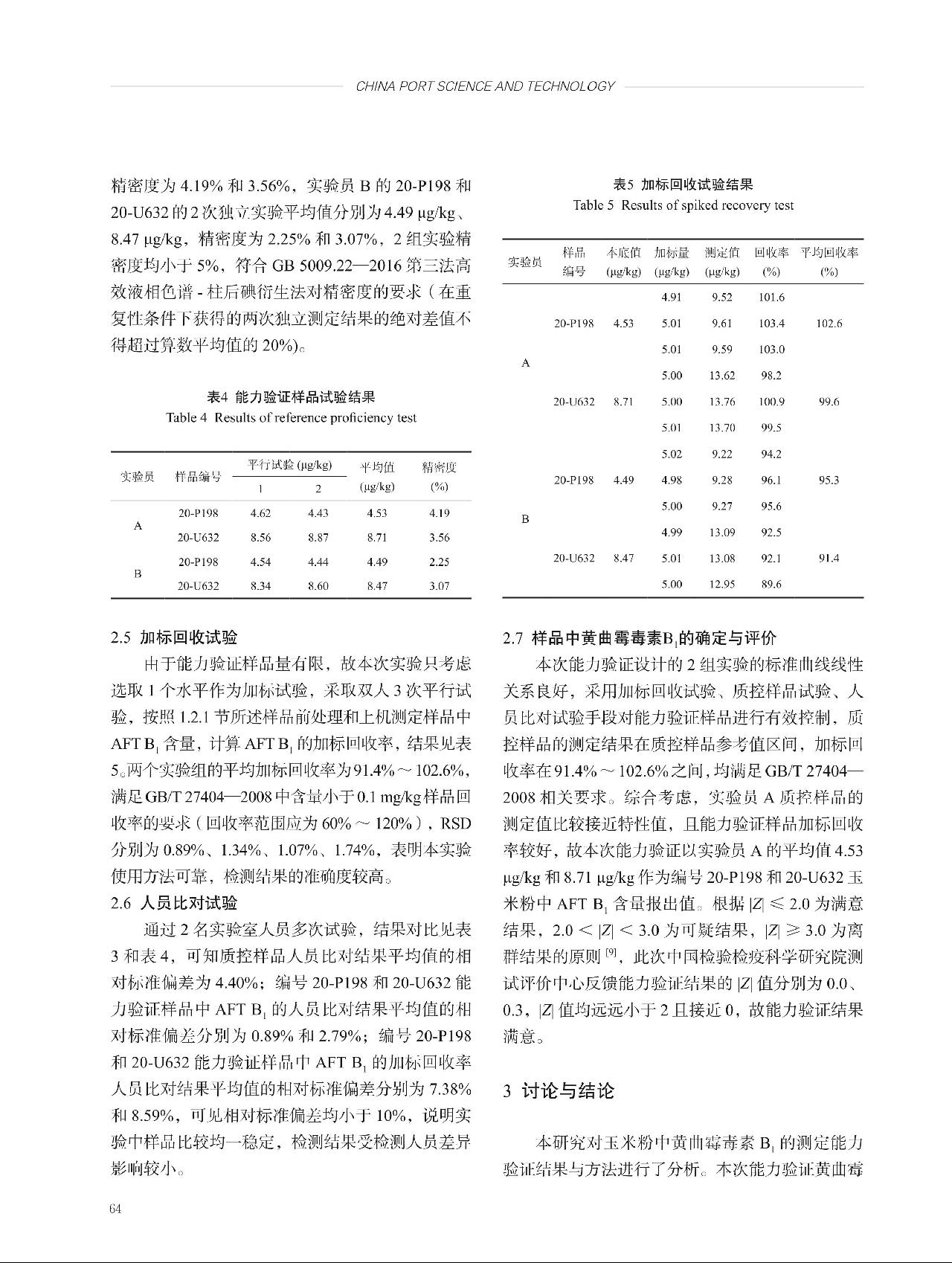 。因此,样品不均匀性引入的不确定度ubb = sbb=
。因此,样品不均匀性引入的不确定度ubb = sbb= ,式中,ubb为瓶间不均匀性导致的不确定度分量,sbb为瓶间标准偏差,
,式中,ubb为瓶间不均匀性导致的不确定度分量,sbb为瓶间标准偏差,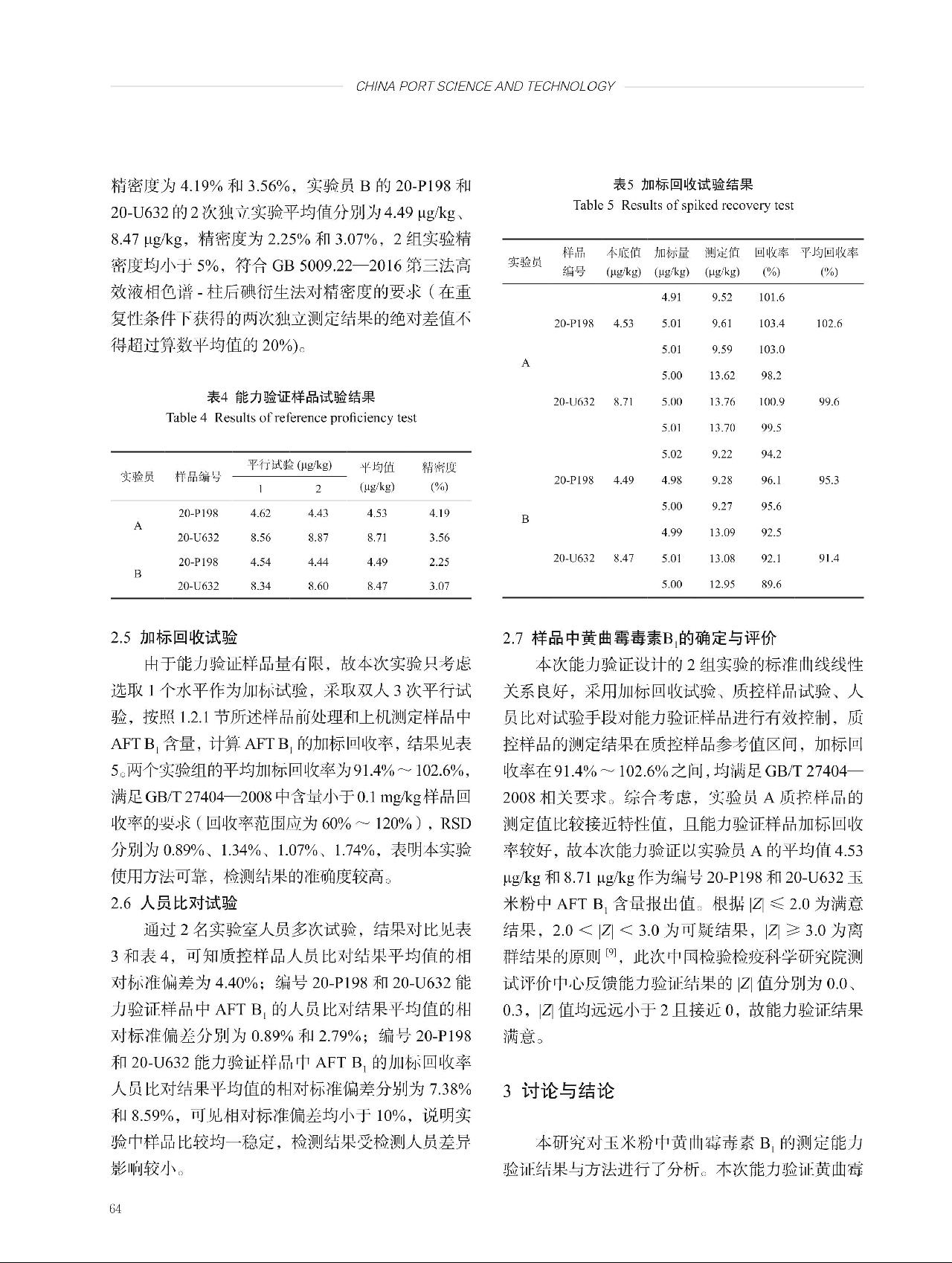 为组间方差,
为组间方差,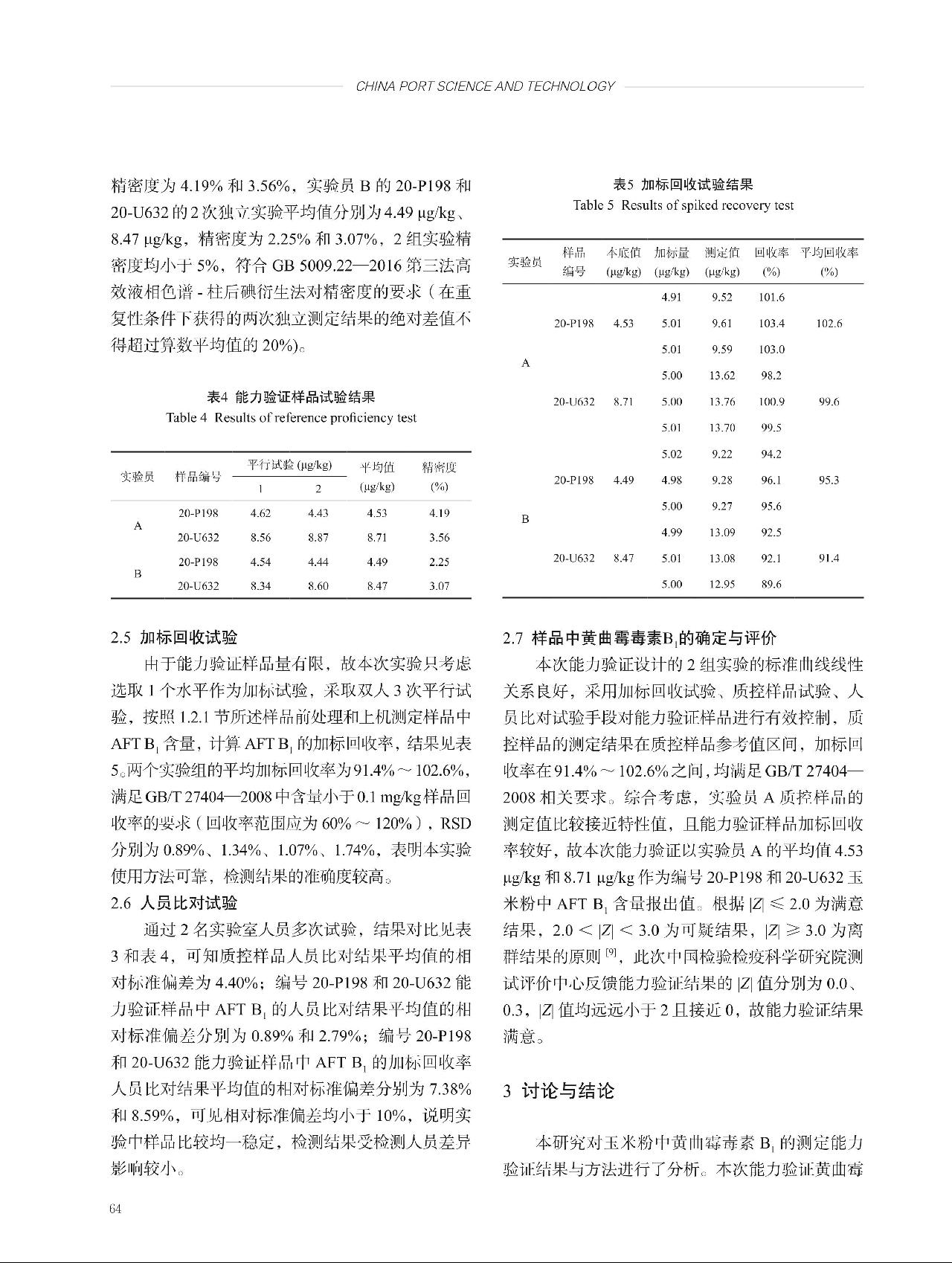 为组内方差,n为组内测量次数。经计算,不均匀性引入的不确定度为ubb = sbb=
为组内方差,n为组内测量次数。经计算,不均匀性引入的不确定度为ubb = sbb=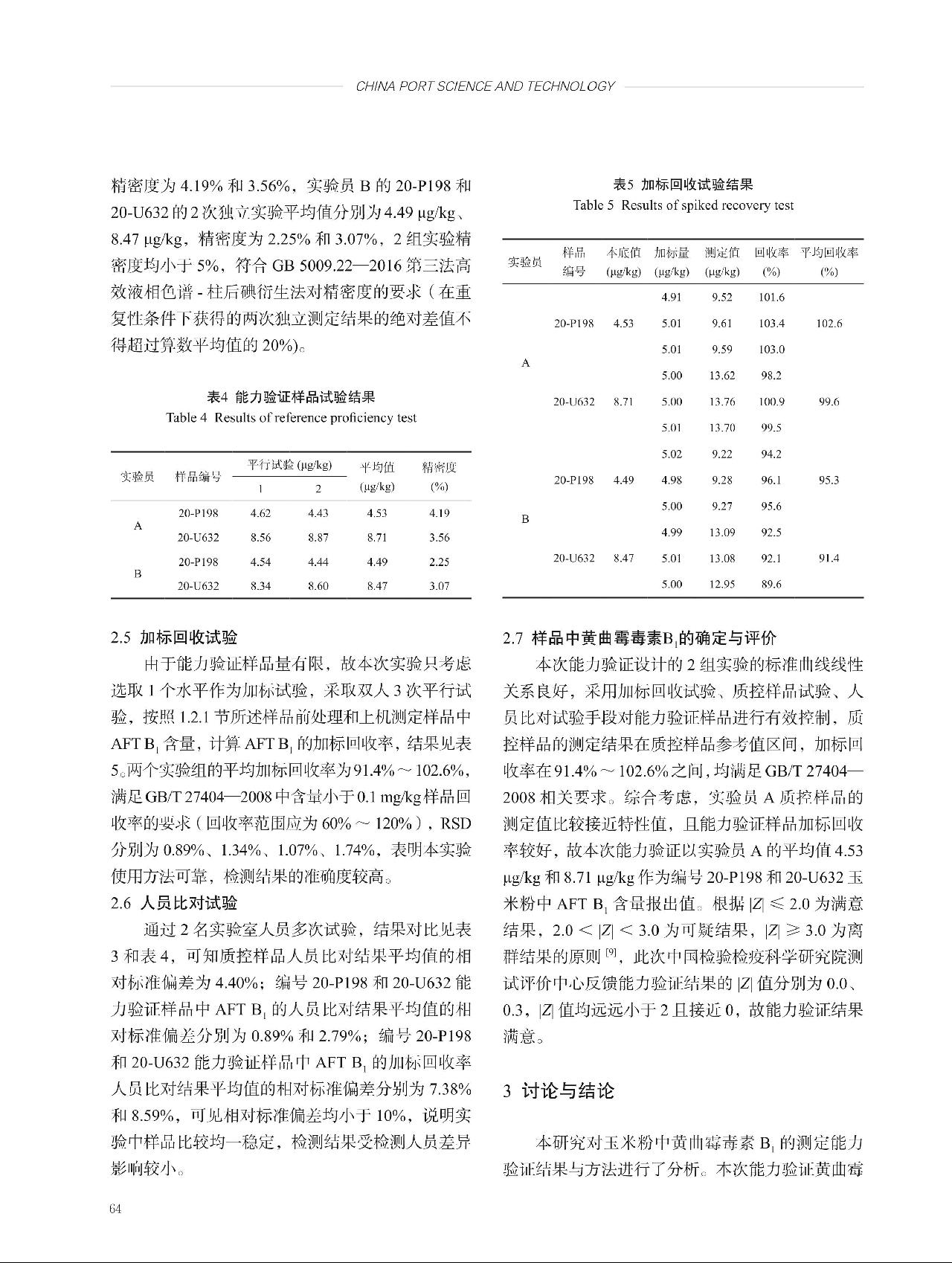 = 1.508,不均匀性引入的相对标准不确定度为ubb(rel) = 0.018。
= 1.508,不均匀性引入的相对标准不确定度为ubb(rel) = 0.018。
6.2 不稳定性引入的不确定度评定(usl和uss)
候选标准物质经长期稳定性检验和短期稳定性检验,均没有观察到不稳定性,因此,不稳定性引入的不确定度us = s(β1)·X,式中,s(β1)为β1的标准偏差s(β1),X为给定的保存期限。将表4中的长期稳定性检验结果代入上式计算,得到长期不稳定性引入的不确定度为usl = 2.733,长期不稳定性引入的相对标准不确定度为usl(rel) = 0.031。将表6中的短期稳定性检验结果代入上式计算,得到短期不稳定性引入的不确定度为uss=2.681,短期不稳定性引入的相对标准不确定度为uss(rel) = 0.032。
6.3 定值过程引入的不确定度评定(uchar)
6.3.1 定值过程引入的A类不确定度(uA)
多个实验室合作定值引入的A类不确定度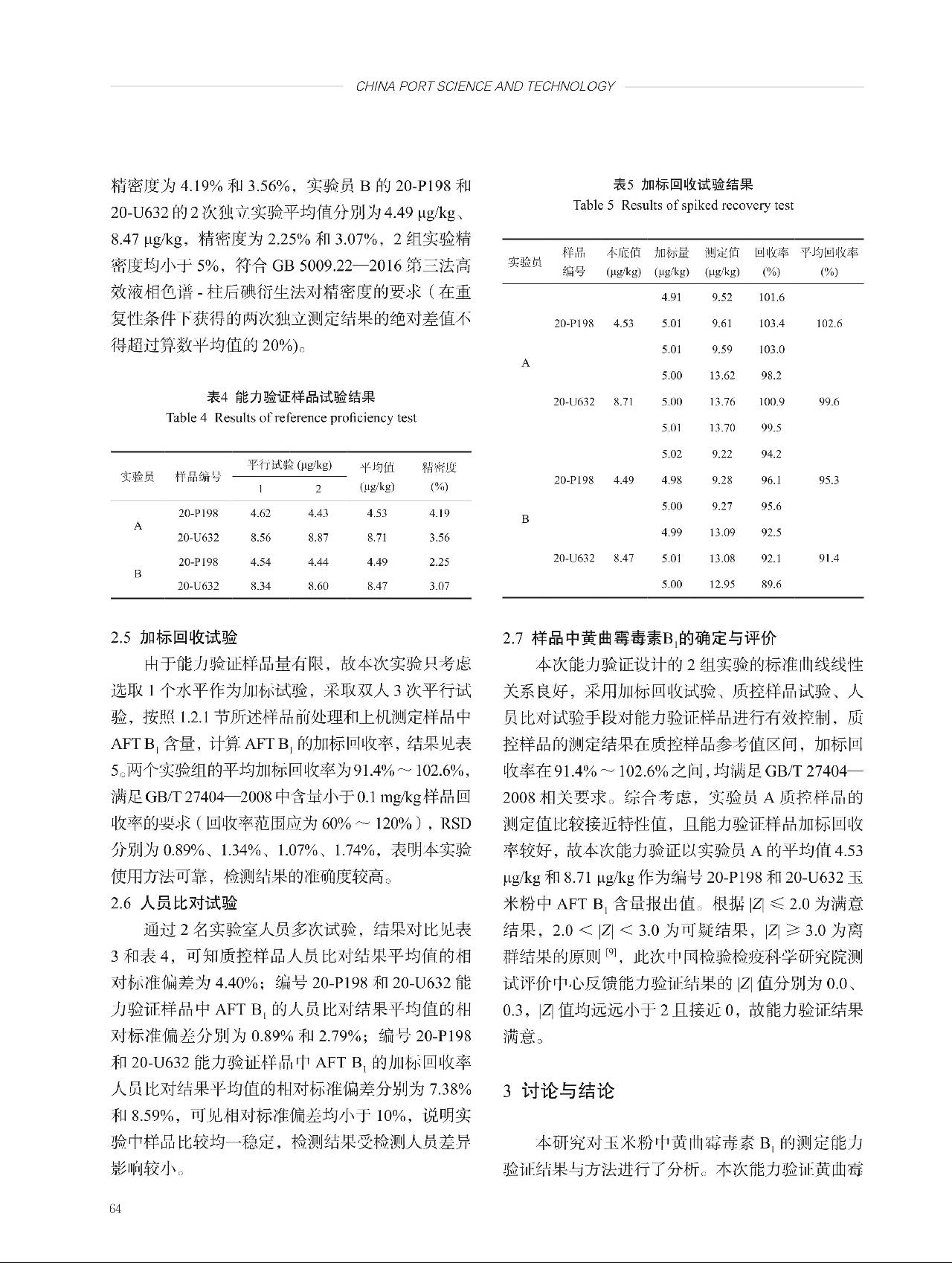 ,式中,
,式中,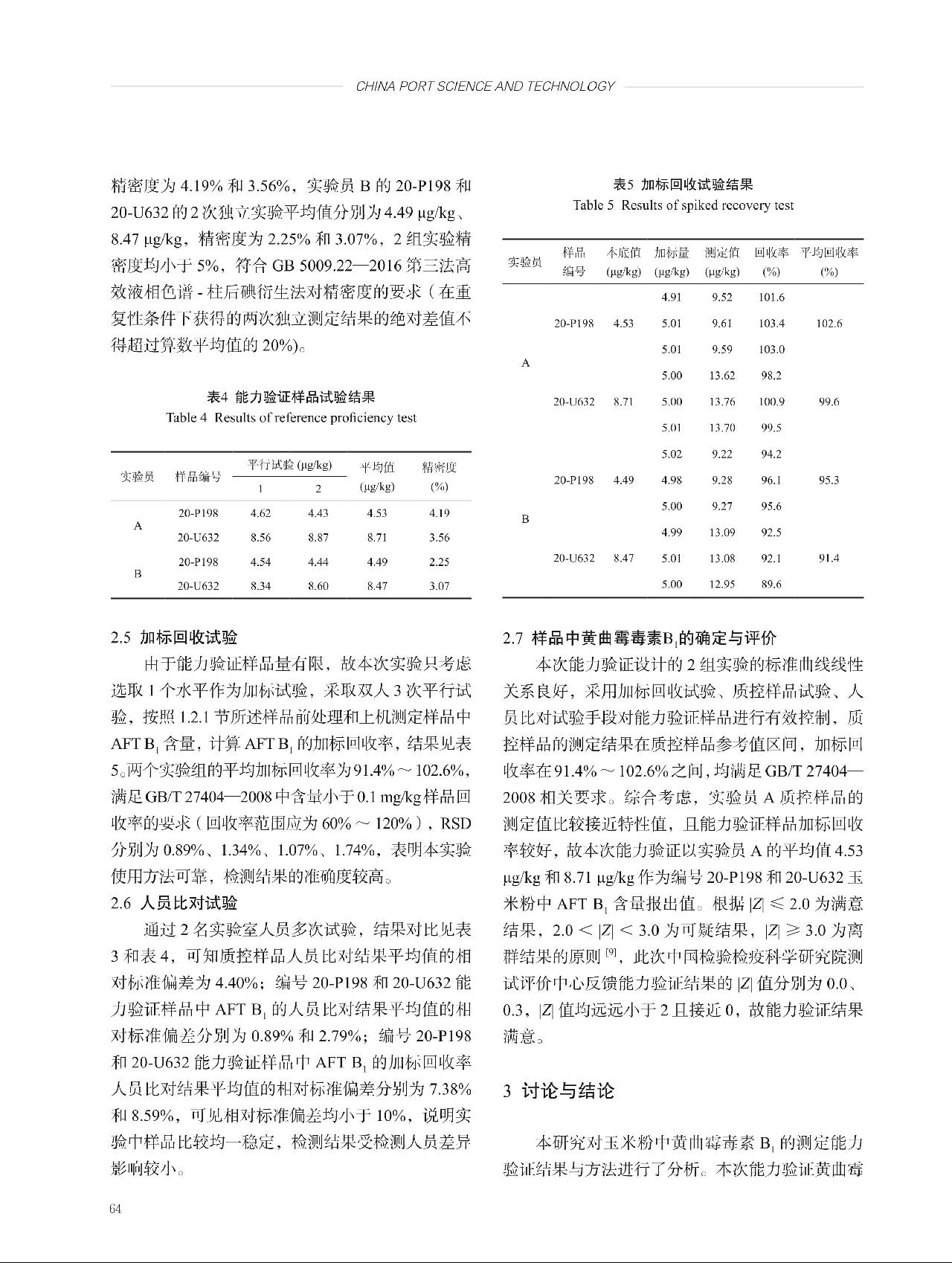 为总平均值的标准偏差,
为总平均值的标准偏差, 为每个实验室的测定平均值,
为每个实验室的测定平均值, 为总平均值,m为参与定值的实验室数目。将表7中的多个实验室合作定值结果代入上式计算,定值过程引入的A类不确定度为uA = 1.209,定值过程引入的A类相对标准不确定度为uA(rel) = 0.015。
为总平均值,m为参与定值的实验室数目。将表7中的多个实验室合作定值结果代入上式计算,定值过程引入的A类不确定度为uA = 1.209,定值过程引入的A类相对标准不确定度为uA(rel) = 0.015。
6.3.2 定值过程引入的B类不确定度(uB)
本研究采用的甘草提取物中OTA定量方法为同位素稀释高效液相色谱-串联质谱法,通过对各个步骤进行分析,确定定值过程引入的B类不确定度主要来自于标准曲线引入的不确定度和样品前处理过程引入的不确定度,具体的不确定度分量计算方式参照文献[8],以下作简述。
1)标准曲线引入的不确定度
①标准物质溶液引入的不确定度
定值用OTA标准物质为国家有证标准物质GBW(E)100303甲醇中OTA溶液标准物质,证书给出的标准值为1.9 μg/mL,扩展不确定度为0.1 μg/mL(k = 2),由该标准物质引入的相对标准不确定度为uB1(rel) = 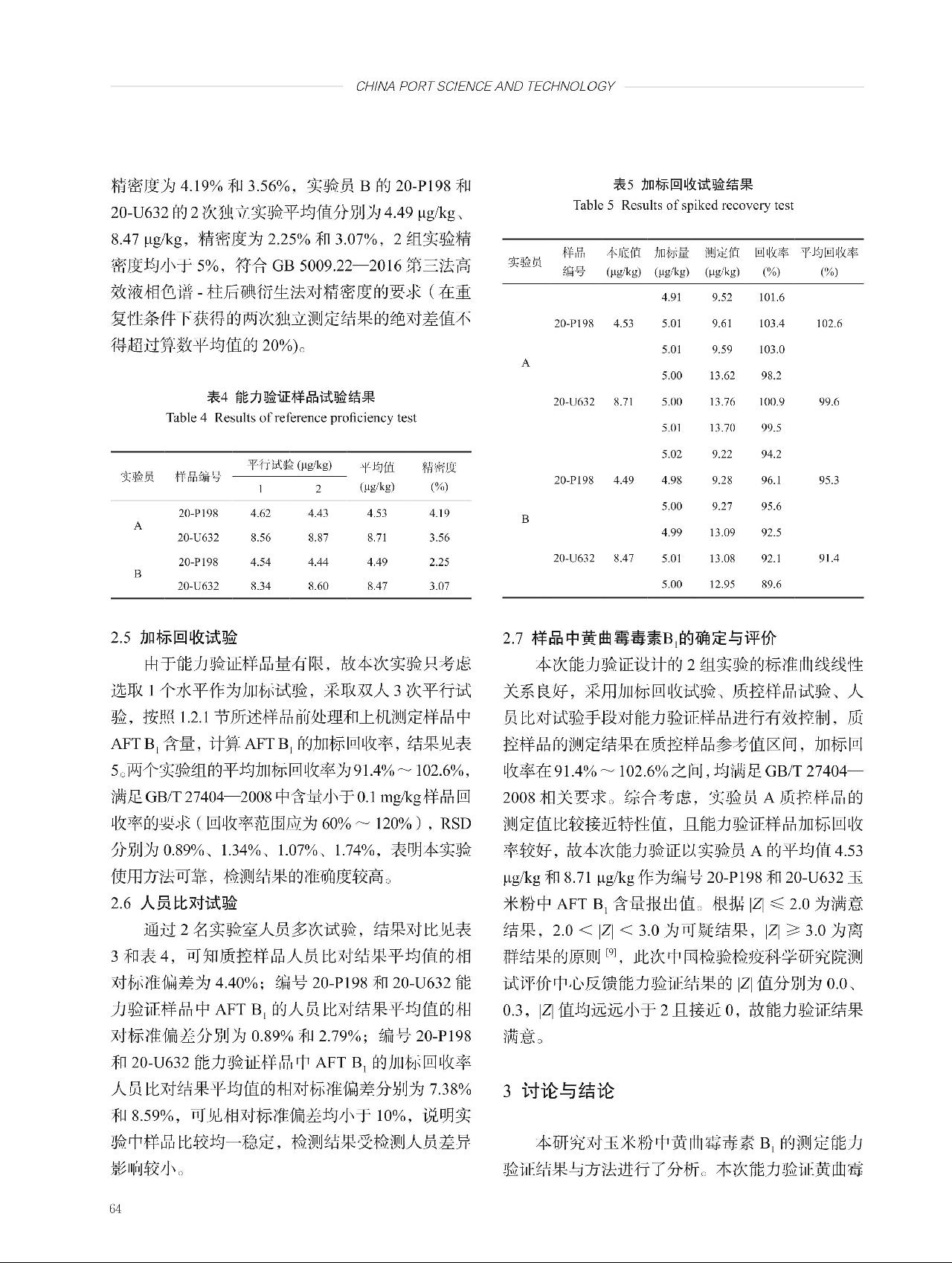 0.02632。
0.02632。
②标准曲线溶液配制引入的不确定度
标准曲线配制过程的不确定度主要来源于量具的误差及溶剂因环境温度引起的体积变化,本研究涉及的量具包括100 mL容量瓶和不同型号的移液枪(200 μL、1 mL),使用的溶剂为甲醇。标准曲线溶液配制引入的相对不确定度uB2(rel) = 0.01409。
③标准曲线拟合引入的不确定度
标准曲线采用最小二乘法进行线性拟合,由此引入的不确定度按以下公式计算:
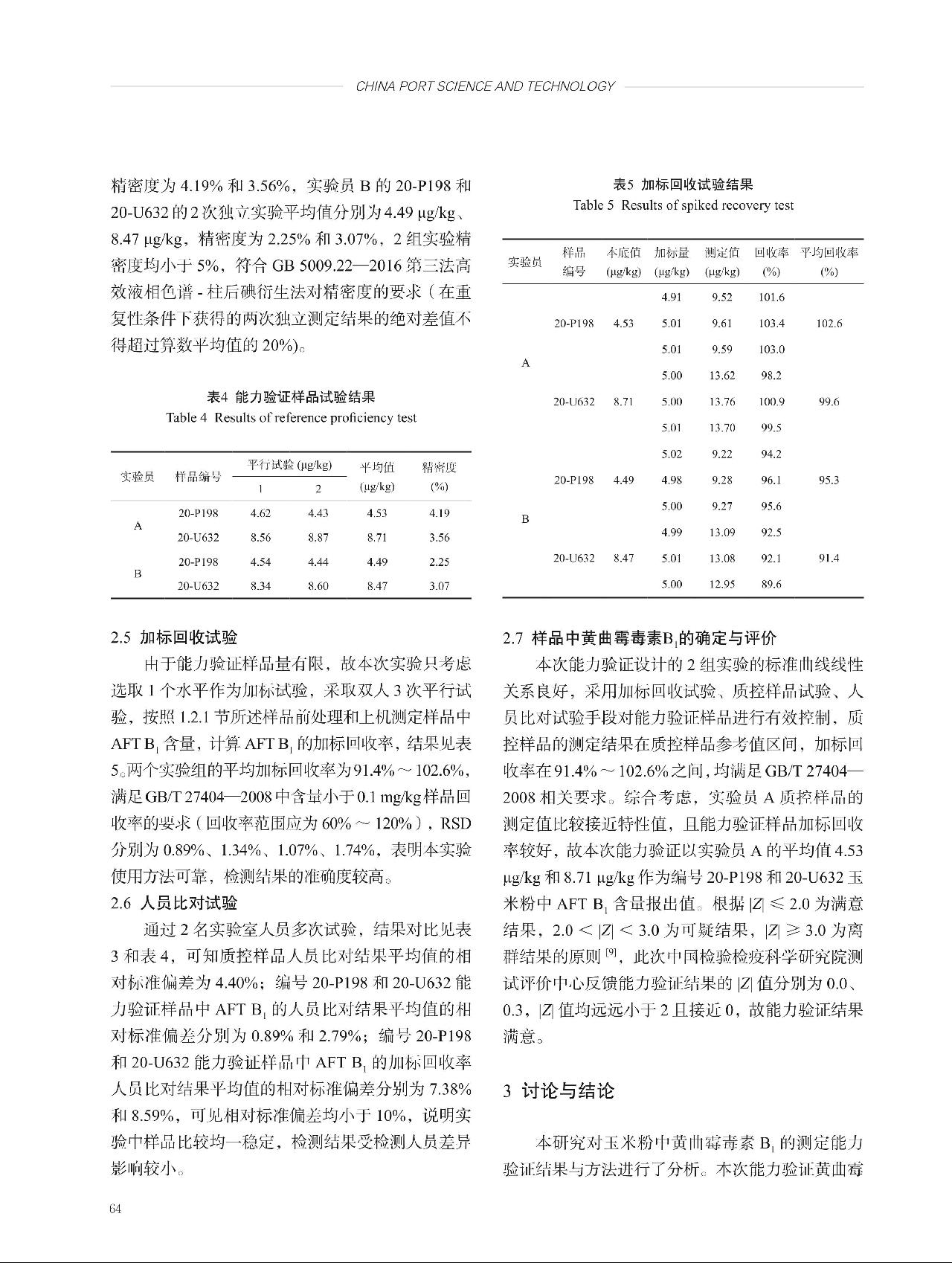
本研究中,标曲拟合所得回归方程为:Y = 1.65X + 0.0275,相关系数r = 0.9998,其中Y为OTA与内标的峰面积比值,X为OTA与内标的浓度比值。由标准曲线拟合引入的相对不确定度uB3(rel) =  。
。
2)样品前处理过程引入的不确定度
①样品称量引入的不确定度
定值过程使用万分之一电子天平称量样品,当试验载荷为5.0 g时,该天平的扩展不确定度U = 0.00016 g(k = 2),由此引入的相对标准不确定度为:uB4(rel) = 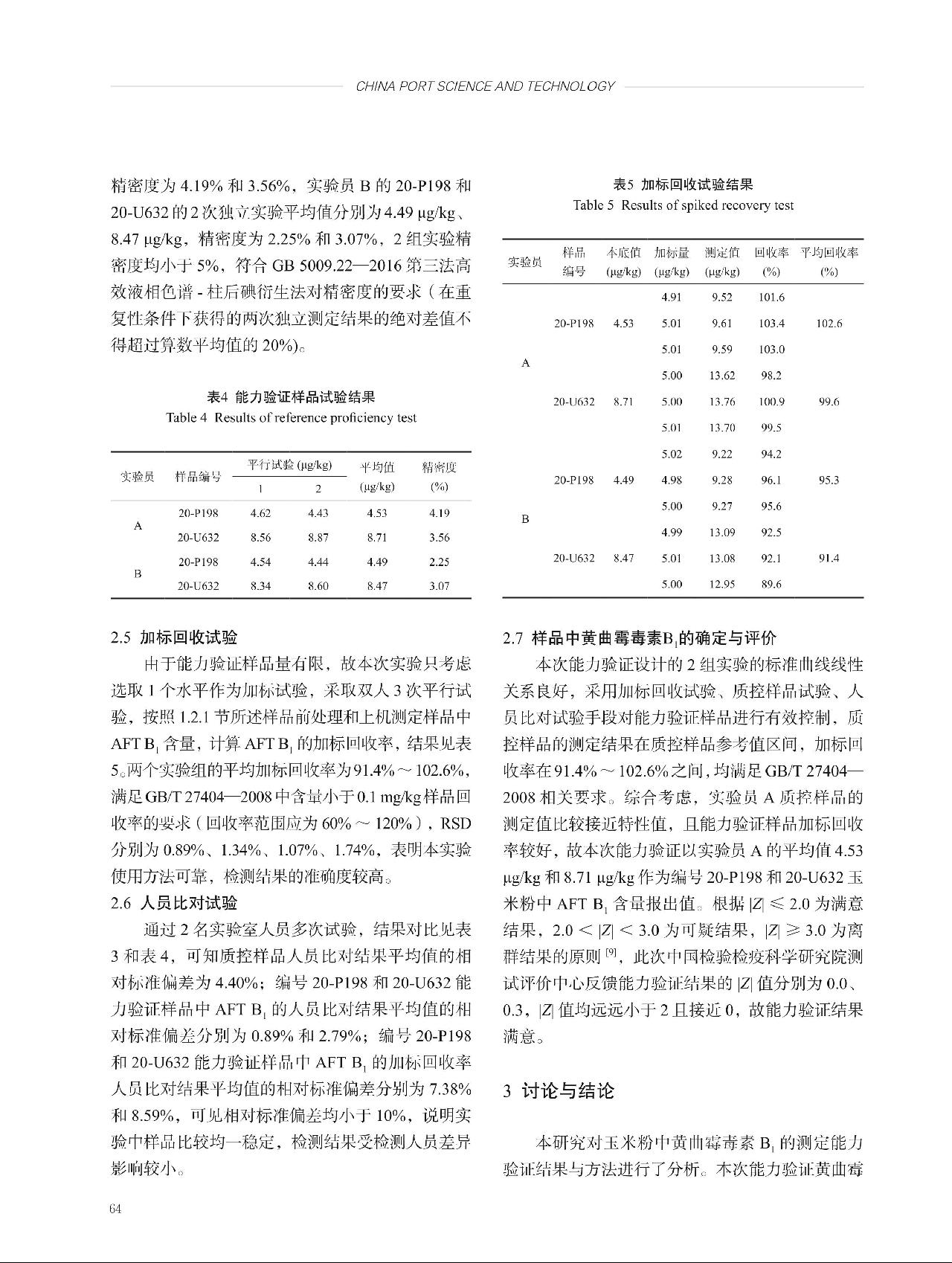 。
。
②提取和稀释过程引入的不确定度
样品提取时使用25 mL玻璃移液管量取甲醇-水(80∶20,v/v)提取溶液,样品提取后,用1 mL移液枪移取1 mL上清液,用10 mL容量瓶定容后过免疫亲和柱净化。根据容量瓶的容量允差、移液枪的扩展不确定度,并结合溶剂(甲醇、水)的体积膨胀系数,计算该过程引入的相对不确定度为uB5(rel) = 4.29×10−3。
③添加内标引入的不确定度
定值过程中使用200 μL移液枪添加[13C20]-OTA内标,根据其扩展不确定度,结合甲醇的体积膨胀系数,计算由此引入的不确定度为:uB6(rel)=3.04×10−3。
综上,定值过程引入的B类相对标准不确定度为uB(rel) =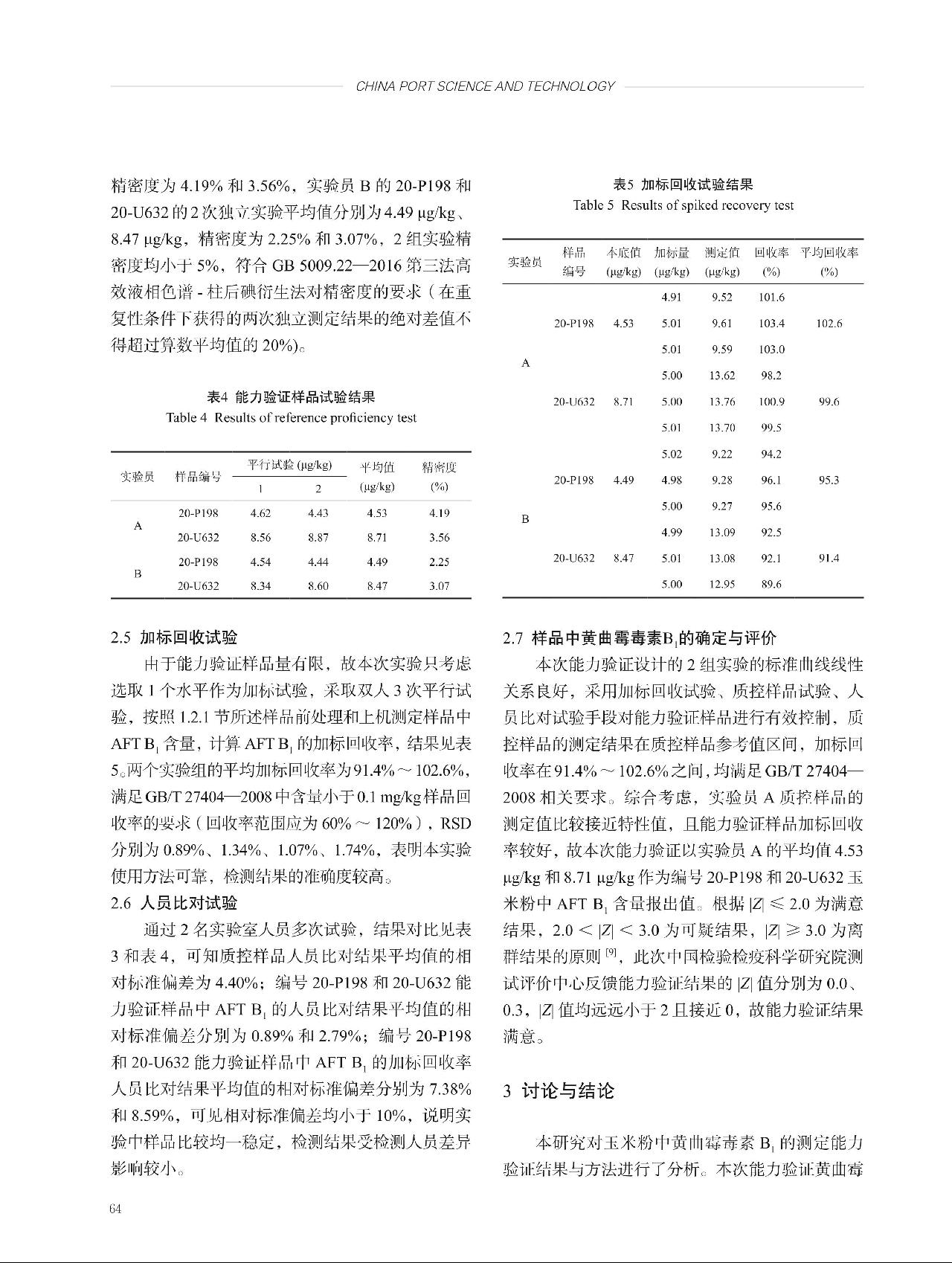 = 0.031。
= 0.031。
6.4 合成标准不确定度(uc)
将不均匀性引起的相对标准不确定度、不稳定性引起的相对标准不确定度、定值过程引入的相对标准不确定度合并,即得标准物质的合成相对标准不确定度

 ,则合成标准不确定度uc = uc(rel)×
,则合成标准不确定度uc = uc(rel)×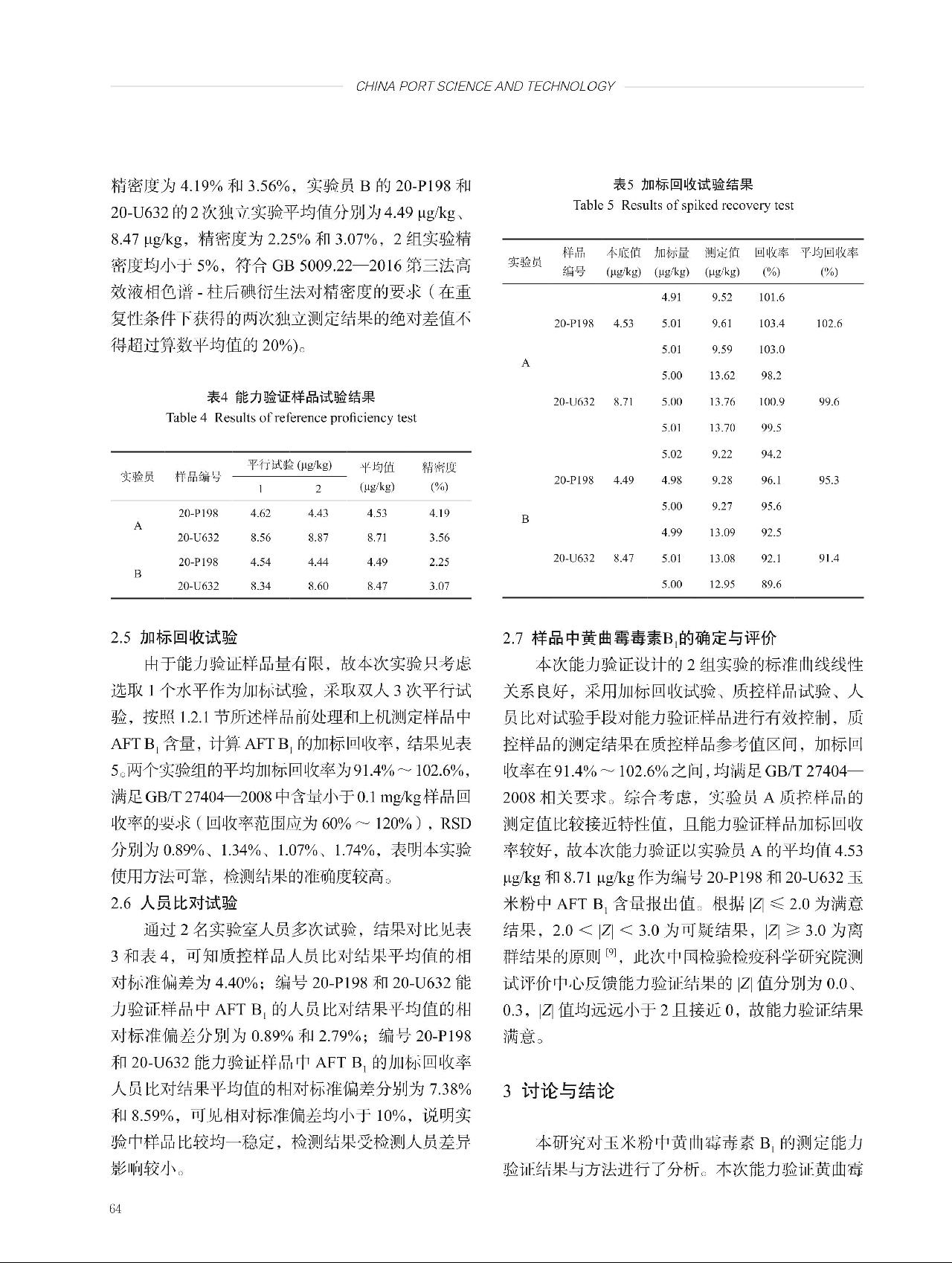 = 4.90 μg/kg。
= 4.90 μg/kg。
6.5 扩展不确定度(U)
扩展不确定度U = k·uc,k为包含因子,一般取k = 2。本研究中,U = k·uc = 9.8 μg/kg。甘草提取物中赭曲霉毒素A的最终测量结果表示为(83.2±9.8)μg/kg,k = 2。
7 结语
基体标准物质有助于提高检测结果的准确性,已在食品污染物、食品添加剂等领域得到了广泛应用。本研究制备的甘草提取物中OTA标准物质均匀性良好,在长期稳定性和短期稳定性评估期间均没有观察到不稳定性,可用于相关产品中OTA分析检测过程的方法验证、质量控制和实验室能力验证等,满足国内外实验室对该类基体标准物质的需求。
参考文献
[1] Magan N, Olsen M. Mycotoxins in food Detection and control[M]. Woodhead Publishing Limited, Cambridge, England, 2004: 247-255.
[2] Liu W-C, Pushparaj K, Meyyazhagan A, et al. Ochratoxin A as an alarming health threat for livestock and human: A review on molecular interactions, mechanism of toxicity, detection, detoxification, and dietary prophylaxis[J]. Toxicon, 2022, 213: 59-75.
[3] Pleština R. Nephrotoxicity of ochratoxin A[J]. Food Addit Contam, 1996, 13 (Suppl.): 49-50.
[4] International Agency for Research on Cancer (IARC). IARC Monographs on Evaluation of Carcinogenic Risk to Humans[M]. IARC Press, France, 1993.
[5] Commission Regulation (EC) No 105/2010 amending Regulation (EC) No 1881/2006 setting maximum levels for certain contaminants in foodstuffs as regards ochratoxin A [S], Official Journal of the European Union, 2010, L 35/7-8.
[6] RASFF Notification 2021.6698. Ochratoxin A above the legal limits in licorice powder [DB/OL]. https://webgate.ec.europa.eu/rasff-window/screen/notification/518490.
[7]李梦怡, 王宏伟, 董喆, 等. 猪肉粉中亚硝酸钠标准物质的研制[J]. 化学分析计量,2022, 31(2): 1-6.
[8]胡玲, 马侦, 王如坤, 等. 高效液相色谱-串联质谱法测定甘草中赭曲霉毒素A的不确定度评定[J]. 食品安全质量检测学报, 2020, 11(12): 3965-3969.
[9]国家药典委员会. 中华人民共和国药典一部[M]. 北京:中国医药科技出版社, 2015.
基金项目:中央本级重大增减支项目(2060302)
第一作者:胡玲(1984—),女,汉族,浙江宁波人,博士,高级工程师,主要从事污染物分析工作,E-mail: hulyn@126.com
1. 宁波海关技术中心 宁波 315012
2. 宁波检验检疫科学技术研究院 宁波 315000
3. 宁波海关 宁波 315012
1. Ningbo Customs District Technology Center, Ningbo 315012
2. Ningbo Academy of Inspection and Quarantine, Ningbo 315000
3. Ningbo Customs District, Ningbo 315012
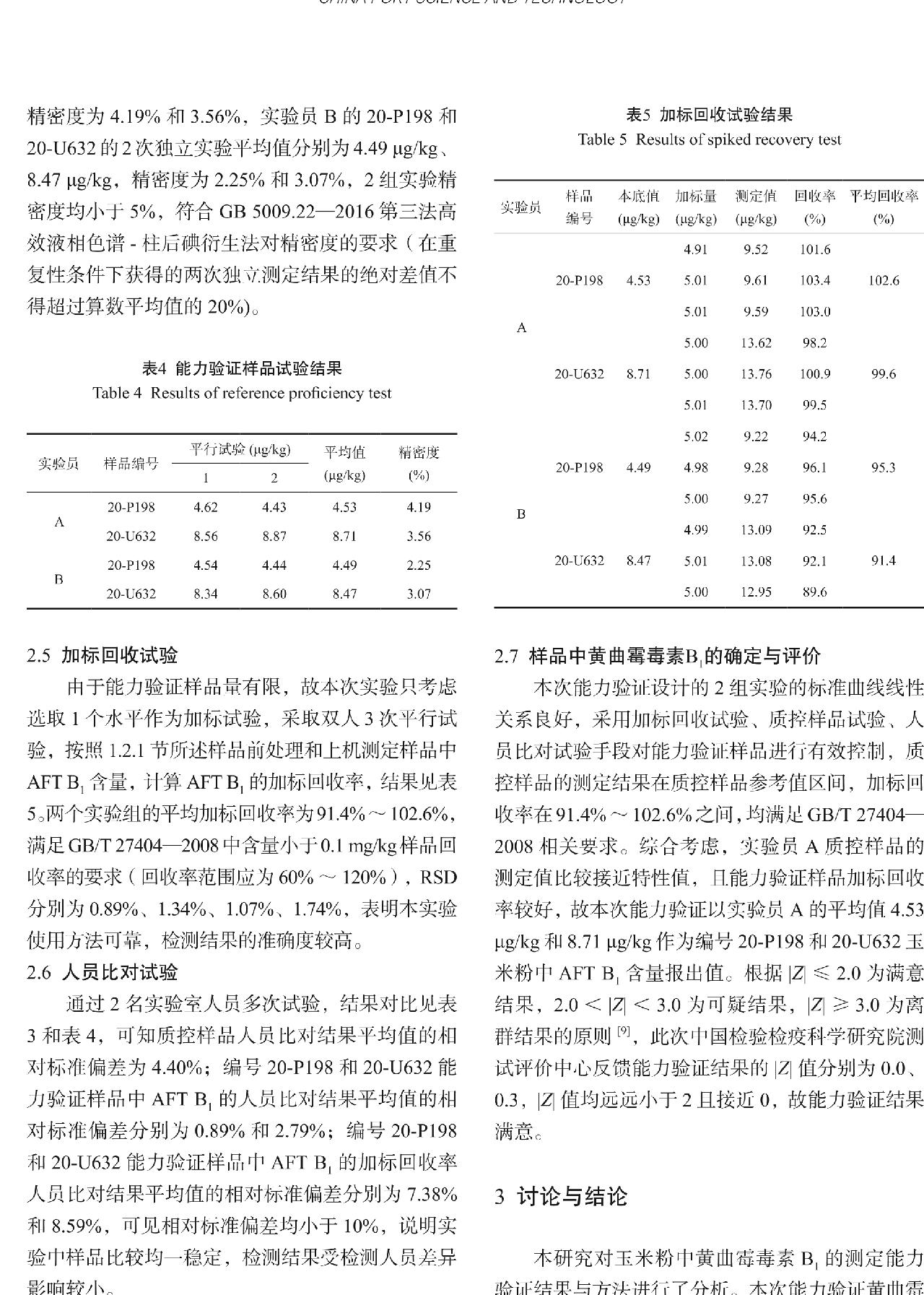
表2 均匀性评估参数值
Table 2 Homogeneity evaluation parameter values
统计量 | 计算值 |
Q1 | 189.4 |
Q2 | 201.2 |
ν1 | 14 |
ν2 | 30 |
| 13.53 |
| 6.71 |
F | 2.02 |
F0.05(14,30) | 2.04 |
基金项目:国家标准化管理委员会项目(S2019327);福州海关科研项目(FK2021-17)
第一作者:王丹红(1969—),女,汉族,浙江苍南人,高级工程师,本科,主要从事进出口食品理化检测工作,E-mail: wdh5539@163.com
通信作者:陈练洪(1980—),女,汉族,福建漳州人,工程师,硕士,主要从事进出口食品理化检测工作,E-mail: clh1128@126.com
1. 福州海关技术中心 福州 350001
1. Technical Center of Fuzhou Customs, Fuzhou 350001










