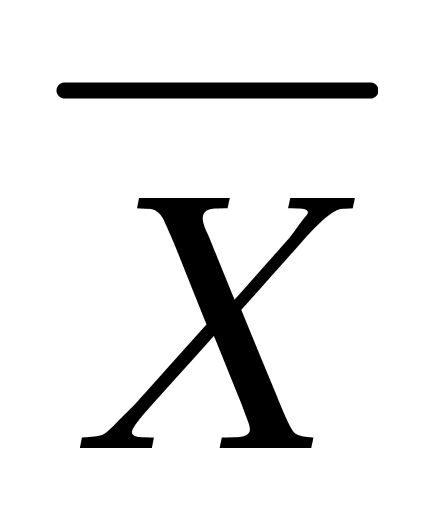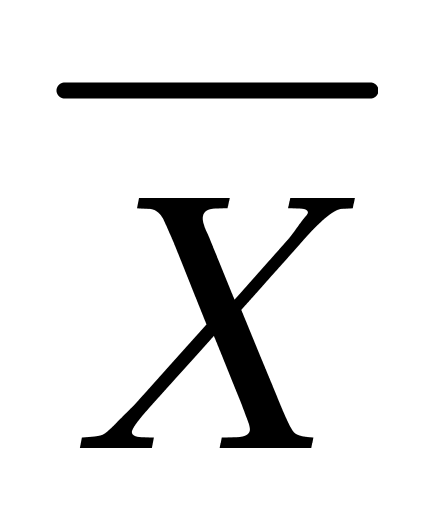CopyRight 2009-2020 © All Rights Reserved.版权所有: 中国海关未经授权禁止复制或建立镜像
吸水性树脂泡发球玩具的安全性评价
作者:陈小青 付燕 金敏 马明 刘汉伟 王燕
陈小青 付燕 金敏 马明 刘汉伟 王燕
Abstract Infrared spectrum detection and acute oral toxicity test, acute dermal toxicity test, skin sensitization test, acute skin irritation/corrosion test, acute eye irritation/corrosion test and acute fish toxic test were used to evaluate the chemical characteristics and toxic effects of absorbent resin expandable toy. Infrared spectrum detection results showed that the main component of the absorbent resin expandable toy was polyacrylamide. The oral LD50>5000 mg/kg, the toxicity level was low toxicity; the dermal LD50>2000 mg/kg, the toxicity level was low toxicity; the sensitive rate of 48 h of sodium metasilicate pentahydrate was 20%. The level of sensitive strength was 2nd class and the substance was slightly skin sensitive; in skin irritation/corrosion test, slight erythema symptom was observed at the animals, which indicated that the substance had slight irritation to skin; in eye irritation/corrosion test, slight conjunctival hyperemia appeared after the rabbit eye was dosed, which indicated that the substance had slight irritation to eye; in the acute fish toxic test, 96 h LC50 was between 10-100 mg/L. In summary, absorbent resin expandable toy has a certain health toxicity, especially in skin irritation, eye irritation and acute fish toxicity. Therefore, in order to ensure children’s health and safety, relevant departments and families should actively carry out health education for children, and to urge children should strictly do the corresponding preventive work in the process of playing with absorbent resin expandable toy to ensure health and safety. At the same time, the relevant manufacturers should also improve the process to produce water-absorbent resin expandable toys, or use non-toxic substances if necessary, to further enhance the quality of absorbent resin expandable toys.
Keywords absorbent resin; expandable ball; toys; toxicology; safety assessment
在儿童成长过程中,玩具扮演着不可或缺的角色。随着科学技术的发展,新型玩具层出不穷。各类玩具在给儿童带来快乐的同时,其安全性也不容忽视。近年来,一种吸水性树脂泡发球玩具深得儿童喜爱,这种吸水性树脂泡发球玩具也叫“水精灵”“水晶弹”“泡大珠”“吸水弹”等,除作为玩具外,还被广泛应用于盆栽保水、室内装饰等。虽然名称众多,但其材质基本相同,主要为吸水性树脂。吸水性树脂泡发球玩具在几小时内能够吸收高于自身重量50~100倍的水,吸水后体积显著膨胀。然而,随着使用人数的增多,吸水性树脂泡发球玩具所引起的健康危害事件报道也越来越多,如误食引起肠梗阻、肠坏死甚至危及生命等[1-3]。此外,吸水性树脂泡发球玩具种类繁多、质量良莠不齐,部分采用劣质色素,其安全性值得关注。但除本项目组外,未见有其他关于吸水性树脂泡发球玩具安全性评价的相关报道。本研究采用红外光谱法以及急性经口毒性试验、急性经皮毒性试验、皮肤致敏试验、急性皮肤刺激性/腐蚀性试验、急性眼刺激性/腐蚀性试验和鱼类急性毒性试验等方法对吸水性树脂泡发球玩具的主要化学成分和急性毒性效应进行评价,旨在为吸水性树脂泡发球玩具的生产和使用提供参考依据。
1 材料与方法
1.1 实验动物
共使用SD大鼠、ICR小鼠、新西兰白色家兔和白色豚鼠4种实验动物,均由浙江省实验动物中心提供。其中,SD大鼠和ICR小鼠在SPF环境中进行饲养,家兔和豚鼠在普通级环境中进行饲养。实验动物给予全价营养颗粒饲料,自由摄食和饮水。动物经检疫合格后在本饲养室中进行了为期5 d的环境适应。本机构实验动物使用许可证号为SYXK(浙)2021-0032(原编号为SYXK(浙)2016-0012)。相关动物试验经本机构实验动物福利伦理管理小组审查批准实施(动物伦理审查报告编号为2016071201)。另外,本研究还采用稀有鮈鲫鱼进行了鱼类急性毒性试验。
1.2 受试物
吸水性树脂泡发球玩具购自市场,为颜色各样的小颗粒。
1.3 受试物处理
直接用原样品进行红外检测。毒理学安全性评价则在试验前将13.0325 g吸水性树脂泡发球玩具加入3.5 L纯水使其充分浸泡,浸泡7 d后过滤收集浸泡液作为试验原液。
1.4 主要设备和试剂
VERTEX 70 红外光谱仪(布鲁克);AL204 电子天平(梅特勒·托利多,精度0.1 mg);CPA8201 电子天平(赛多利斯,精度0.1 g);2,4-二硝基氯苯,皮肤致敏试验阳性对照(CAS号97-00-7,Dr. Ehrenstorfer GmbH公司,批号70531,99.0%)。
1.5 毒性评价剂量设置及试验方法
本研究中提及的毒理试验方法均参照化学品系列国家标准的相应方法(包括GB/T 21603—2008《化学品 急性经口毒性试验方法》、GB/T 21606—2008《化学品 急性经皮毒性试验方法》、GB/T 21608—2008《化学品 皮肤致敏试验方法》、GB/T 21609—2008 《化学品 急性眼刺激性/腐蚀性试验方法》、GB/T 21604—2008《化学品 急性皮肤刺激性/腐蚀性试验方法》、GB/T 27861—2011《化学品 鱼类急性毒性试验》)以及本研究团队所进行的具体操作流程[4-5]。
1.5.1 急性经口毒性试验
使用10只ICR小鼠,雌雄各半,并采用最大限量法进行试验。染毒剂量设置为5000 mg/kg BW。试验前禁食4 h,饮水不限。采用一次经口灌胃法对每组动物进行染毒。染毒后继续禁食3~4 h后再恢复给食。观察染毒过程和观察期内动物的中毒和死亡情况并及时记录,观察周期为14 d。观察期结束后,处死存活动物并进行大体解剖。根据试验结果得出LD50并查表进行毒性分级(见GB/T 21606—2008表C.6 急性毒性分级标准)。
1.5.2 急性经皮毒性试验
使用10只SD大鼠,雌雄各半,并采用2000 mg/kg限量法进行试验。受试物于染毒前现配现用。试验期间单笼饲养。试验前24 h,剪去或剔除动物躯干拟染毒区域的被毛,去毛面积不少于动物体表面积的10%。固定好动物,将受试样品均匀涂布于动物的去毛区,并用玻璃纸和两层纱布覆盖,再用无刺激性胶带加以固定,采用封闭性试验。染毒24 h后,去除覆盖物,用温水洗净皮肤残留的受试样品。观察染毒过程和观察期内动物的中毒和死亡情况并及时记录,观察周期14 d。观察期结束后,处死存活动物并进行大体解剖。根据试验结果得出LD50并查表进行毒性分级(见GB/T 21606—2008表C.6 急性毒性分级标准)。
1.5.3 皮肤致敏试验
使用60只豚鼠,雌雄各半。根据预试验结果,选择0.10 mL浸泡液作为诱导剂量(用生理盐水稀释至0.4 mL),选择0.05 mL浸泡液作为激发剂量(用生理盐水稀释至0.4 mL)。阴性对照组诱导剂量用0.4 mL生理盐水,激发剂量同受试物组。阳性对照组诱导剂量为0.4 mL 0.6%的2,4-二硝基氯苯溶液,激发剂量使用0.4 mL 0.3%的2,4-二硝基氯苯溶液。分别于第0 d、7 d、14 d进行诱导染毒,每次染毒6 h。末次诱导后14 d,即第28 d再进行激发染毒6 h。激发接触结束后于24 h和48 h观察皮肤反应,进行评分并计算得出样品所致的致敏率,查表进行致敏强度分级(见GB/T 21608—2008 表2 皮肤致敏反应试验分级标准)。
1.5.4 急性皮肤刺激性/腐蚀性试验
使用3只健康成年新西兰白色家兔,并采用封闭性贴敷法进行试验。因怀疑该受试物可能具有腐蚀性,所以先采用1只动物并最多使用3块试验贴(每块试验贴均取0.5 mL受试物滴于2.5 cm×2.5 cm纱布上)在不同的时间点作用于动物皮肤。另一侧去毛区作为自身对照,不进行任何处理。其中,任何一步如果观察到腐蚀性反应均应立即结束试验。在移除受试物后1 h、24 h、48 h和72 h观察贴覆部位皮肤反应并进行评分。根据24 h、48 h和72 h各观察时点的最高积分均值,进行皮肤刺激强度分级,查表进行皮肤刺激强度分级(见GB/T 21604—2008表2 皮肤刺激强度分级)。
1.5.5 急性眼刺激性/腐蚀性试验
使用1只健康成年新西兰白色家兔。取0.1 mL受试物涂抹到家兔右侧眼结膜囊内进行染毒。染毒后不进行冲洗眼睛操作。另一侧眼睛作为自身对照,不进行任何处理。染毒结束后1 h、24 h、48 h、72 h、4 d和7 d内对家兔眼睛进行检查和评分(包括角膜、虹膜和结膜),并记录观察到其他眼部组织损伤和临床表现。根据染毒前4 d的最高加权总积分均值、刺激反应持续时间及其分值来判定受试物对眼刺激或腐蚀作用及强度,查表进行皮肤刺激强度分级(见GB/T 21609—2008 表A.2 眼刺激性分级及其评价标准)。
1.5.6 鱼类急性毒性试验
使用稀有鮈鲫鱼作为受试生物并采用静水式试验法。试验用水选取高质量的饮用水(经除氯处理pH为6.92~7.72,水硬度为115 mg/L,试验开始前充分曝气)。试验期间不间断充氧,共设1 mg/L、10 mg/L、100 mg/L3个剂量组和1个空白对照组。每个试验容器中投入10尾鱼。当试验溶液调节至相应温度后,随机取10尾鱼并迅速放入各试验容器中进行染毒。转移期间因处理不当而受到损伤的鱼均应弃除。染毒24 h、48 h、72 h和96 h后分别检查受试鱼的死亡状况并及时记录,试验周期共96 h。
1.5.7 数据处理与分析
将所有试验数据输入excel进行整理汇总,采用SPSS 19.0软件计算得出均数和标准差。LD50/LC50及其95%可信区间则由查表得出。
2 结果与分析
2.1 化学成分分析结果
采用红外光谱仪对吸水性树脂泡发球玩具的化学成分进行了分析。红外光谱仪设备参数为:扫描波数400~4000 cm-1,扫描次数16次,样品量为0.2 g。结果显示3285 cm-1的宽峰为-NH2(胺基)和缔合的-NH2吸收峰(由于含水,致使3300 cm-1附近峰展宽,因此此波数也包括了水中-OH吸收峰),1661 cm-1为C = O(羰基)的特征吸收峰,1568 cm-1为N-H(仲酰胺)的弯曲振动吸收峰,1407 cm-1为-CH2(亚甲基)变形的吸收峰。由此推断,该吸水性树脂泡发球玩具的主要成分为聚丙烯酰胺。
聚丙烯酰胺是一种高分子化合物,基本物质在多数有机溶剂中都不相溶,有非常良好的絮凝性质,能有效降低液体之间的相应摩擦阻力,其水解体具有增稠作用[6]。聚丙烯酰胺的毒性主要来自其残留单体丙烯酰胺(AN)。丙烯酰胺属中等毒性物质,具有多种生物毒性[7],如防护不当会造成中毒,如影响肺组织氧化损伤[8]、血糖代谢及脏器功能[9],还会造成血液毒性[10]。其红外图谱如图1所示。
2.2 急性经口毒性试验
染毒后的ICR小鼠出现皮毛蓬松、精神萎靡症状。至试验结束,未见ICR小鼠死亡,大体解剖未见异常。动物死亡和体重变化情况见表1,从数据可得LD50>5000 mg/kg BW,毒性分级为低毒级(见GB/T 21606—2008表C.6 急性毒性分级标准)。
2.3 急性经皮毒性试验
染毒期间SD大鼠表现出不安、萎靡等症状。染毒后24 h去除动物背部贴敷物时发现皮肤稍见红斑。24 h后再次观察时已恢复正常。观察期结束时进行大体解剖,所有SD大鼠的主要脏器均未发现异常改变。结果显示,SD大鼠急性经皮毒性LD50>2000 mg/kg,毒性分级为低毒级(见GB/T 21606—2008表C.6急性毒性分级标准),具体见表2。
表2 急性经皮毒性试验结果汇总表
Table 2 Summary of results of acute dermal toxicity test
性别 | (只) | 体重 ( | (只) | (%) | ||
0 d | 7 d | 14 d | ||||
雄 | 5 | 266.3±6.7 | 309.6±7.3 | 351.8±11.2 | 0 | 0 |
雌 | 5 | 233.4±9.2 | 253.8±11.3 | 272.3±15.4 | 0 | 0 |
2.4 皮肤致敏试验
阳性对照组24 h和48 h致敏率分别为85.0%和80.0%,致敏强度为五级,具有极强的皮肤致敏性。阴性对照组24 h和48 h致敏率均为0%。受试物组在24 h和48 h的致敏率分别为15.0%和20.0%,如表3所示。查表得知该受试物对豚鼠的致敏强度为Ⅱ级,具有轻度的皮肤致敏性(见GB/T 21608—2008表2 皮肤致敏反应试验分级标准)。
2.5 急性皮肤刺激/腐蚀试验
动物染毒后,观察发现家兔对照组皮肤正常,但试验组皮肤出现轻微红斑。结果显示,最高积分均值为0.75,该受试物对家兔皮肤具有轻刺激性(见GB/T 21604—2008表2 皮肤刺激强度分级)。具体结果见表4、图2—图3。

图2 对照组皮肤
Fig.2 Dermal of the control group
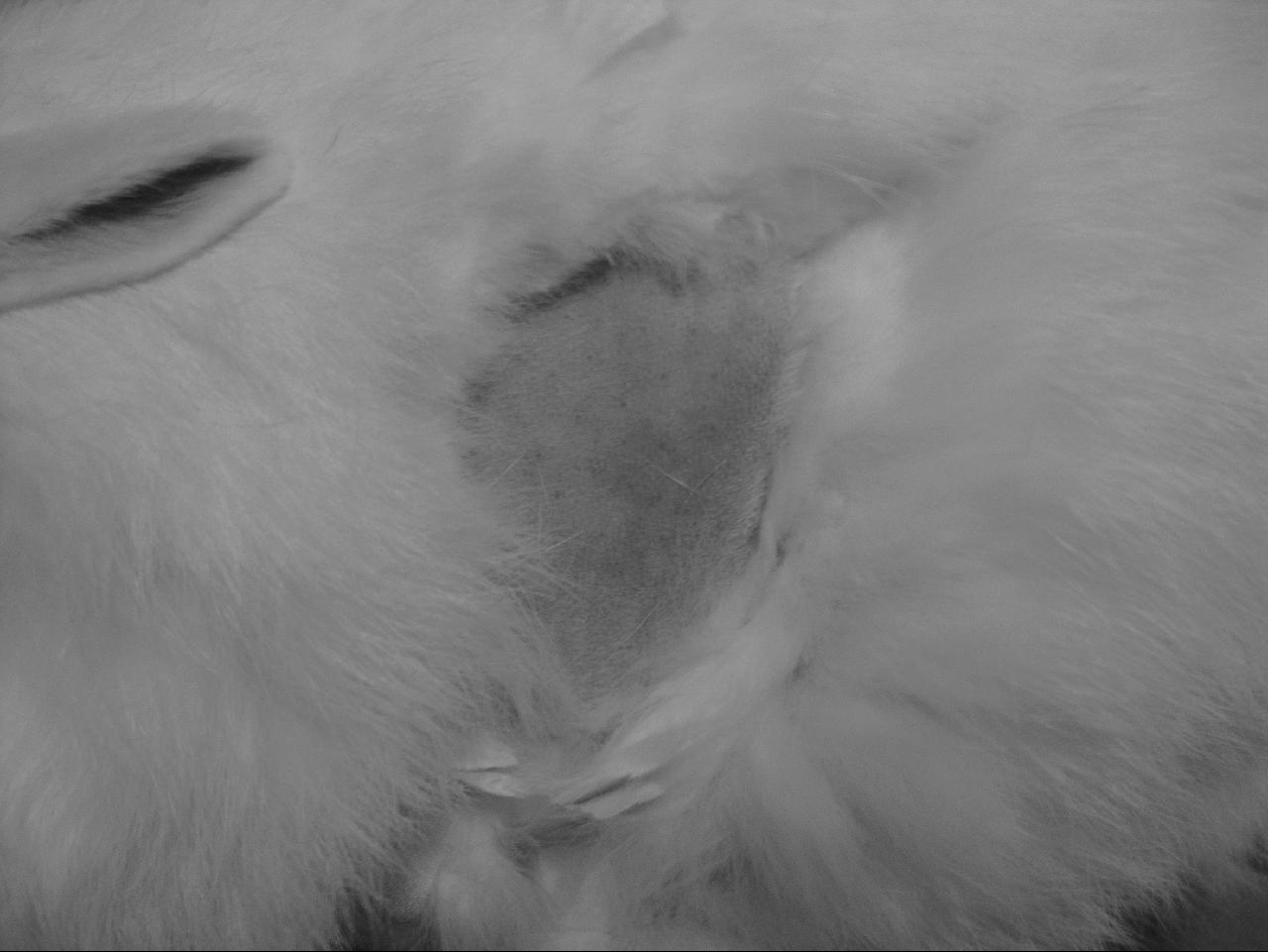
图3 试验组皮肤
Fig.3 Dermal of the experiment group
2.6 急性眼刺激/腐蚀试验
滴入受试物后动物开始尖叫,并不断抓挠染毒侧眼睛。动物眼部角膜、结膜和虹膜损伤评分结果见表5以及图4—图5。结果显示,染毒后动物眼睛出现结膜充血症状,于试验第7 d恢复正常,结果判定为具有微刺激性(见GB/T 21609—2008表A.2 眼刺激性分级及其评价标准)。

图4 对照组眼睛
Fig.4 The eye of the control group
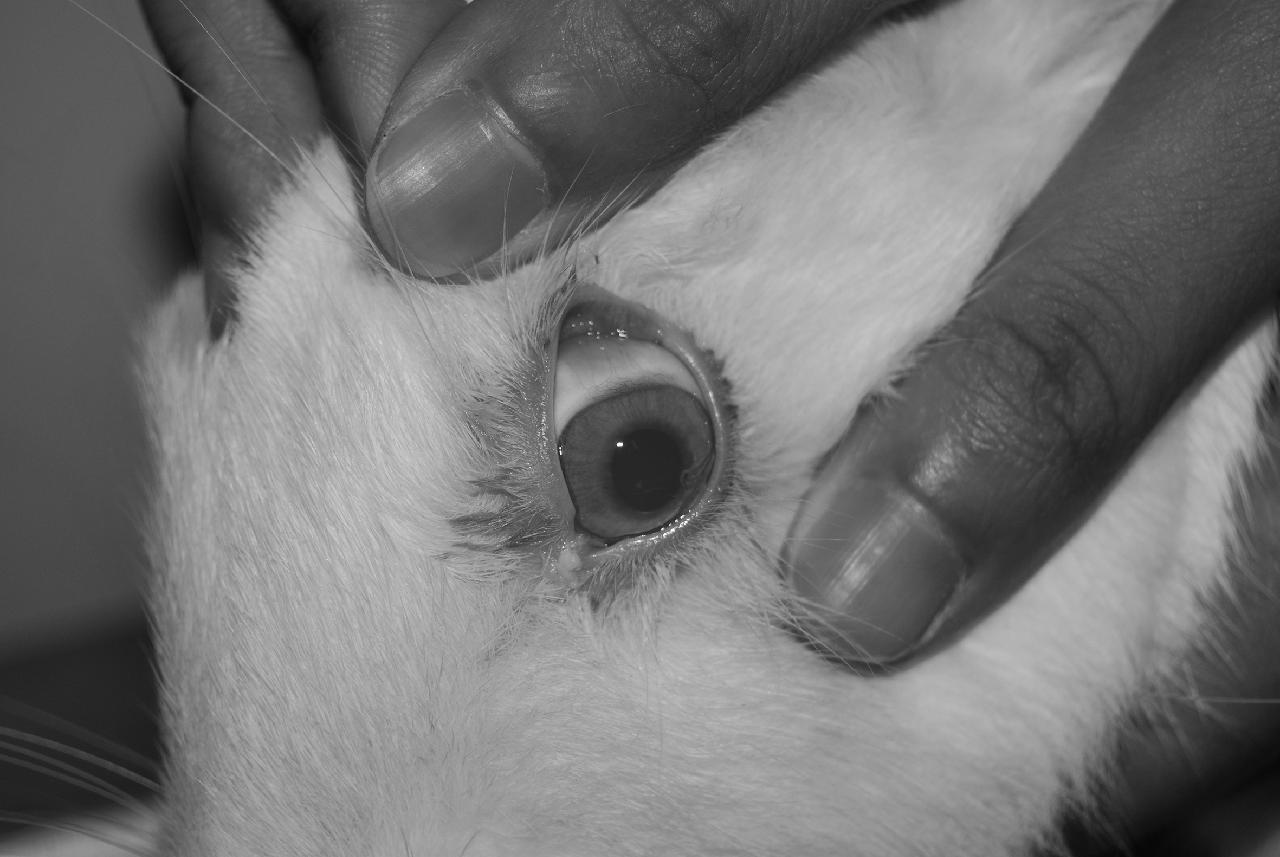
图5 试验组眼睛
Fig.5 The eye of the experiment group
2.7 鱼类急性毒性试验
本试验各剂量组中的监测指标均符合GB/T 27861—2011要求,见表6。96 h静水式鱼类毒性试验结果显示,100.00 mg/L剂量组染毒后,2 h内鱼全部死亡,沉入缸底;10.00 mg/L剂量组染毒后,24 h内鱼未见死亡;1.00 mg/L剂量组和空白对照组,试验至96 h,所有鱼均未死亡。根据GB/T 27861—2011和GB/T 21281—2007《危险化学品鱼类急性毒性分级试验方法》所述标准,该吸水性树脂泡发球玩具的96 h LC50位于10~100 mg/L之间,毒性级别为急性Ⅲ级。试验结果见表7、图6。
3 结论
本研究采用红外光谱法以及包括急性经口毒性试验方法、急性经皮毒性试验方法、皮肤致敏试验方法、急性眼刺激性/腐蚀性试验方法、急性皮肤刺激性/腐蚀性试验方法和鱼类急性毒性试验等方法对吸水性树脂泡发球玩具的主要化学成分和毒性效应进行较为系统的评价研究,旨在为水精灵泡发球玩具的相关生产商和使用者提供一定的参考依据。红外光谱法检测结果显示,吸水性树脂泡发球玩具的主要成分为聚丙烯酰胺。急性经口毒性试验测得LD50>5000 mg/kg,分级为低毒级;急性经皮毒性测得LD50>2000 mg/kg,分级为低毒级;受试物组48 h的致敏率均为20%,为轻度致敏性,2级;皮肤刺激/腐蚀试验显示皮肤轻微红斑症状,轻微刺激性;眼刺激/腐蚀试验显示眼染毒后出现结膜轻微充血,具有微刺激性。鱼类急性毒性试验测得96 h LC50位于10~100 mg/L之间。本研究结果提示劣质的吸水性树脂泡发球玩具对健康具有一定程度的影响,尤其表现在皮肤刺激、眼刺激性和鱼类急性毒性。因此,结合实际情况,提出以下建议:1)就家长和儿童等消费者而言,应购买质量可靠的吸水性树脂泡发球玩具;2)就社会和家庭而言,应加强健康教育,提醒儿童在玩耍过程中做好防范工作,不要徒手直接抓取浸泡后的吸水性树脂泡发球玩具,更不要吞食;3)就生产厂商而言,应改进工艺,改用明胶等无毒无害物质生产吸水性树脂泡发球玩具,以切实保障儿童的健康安全。
参考文献
[1]郭利霞, 顾志成, 徐永根, 等. 消化道异物致儿童肠梗阻一例[J]. 临床小儿外科杂志, 2021, 20(5):498-500.
[2]高瑞杰, 余日胜, 李炳荣, 等. 1例婴儿误吞水晶球致小肠梗阻CT征象分析和优化CT检查设想[J]. 温州医科大学学报, 2021, 51(2): 158-159.
[3]李晓英, 杨秀珍, 徐彬, 等. 超声诊断水晶球致小儿肠梗阻3例[J]. 临床小儿外科杂志, 2019, 18(6): 527-528.
[4]陈小青, 马中春, 孙运, 等. 3,3-二甲基-2-氧代丁酸的急性毒性效应评价研究[J]. 现代预防医学, 2016, 43(12): 2220-2224.
[5]陈小青, 马中春, 苏亦青, 等. 五水偏硅酸钠的毒性效应研究[J]. 人人健康, 2017(22): 277-278.
[6]余荣和. 聚丙烯酰胺的特性及应用[J]. 石化技术, 2016, 23(10): 16, 14.
[7]雷艾彤, 苏丹, 聂春超, 等. 丙烯酰胺风险暴露及毒性控制研究进展[J]. 食品研究与开发, 2022, 43(6): 181-189.
[8]卜文婕, 林爱琴, 高继光, 等. 青春期丙烯酰胺暴露对小鼠肺组织氧化损伤的影响[J]. 中国实验动物学报, 2023, 31(1): 43-50.
[9]谢依婷, 彭非, 娄爱华, 等. 膳食丙烯酰胺暴露对2型糖尿病大鼠血糖代谢及脏器功能的影响[J]. 食品科学, 2023, 44(7): 151-160.
[10]王小博, 梁斯, 陈齐, 等. 丙烯酰胺对小鼠血液毒性的研究[J]. 中国实验动物学报, 2021, 29(4): 506-511.
图1 红外检测结果图谱
Fig.1 Results of infrared spectrum detection
表1 急性经口毒性试验结果汇总表
Table 1 Summary of results of acute oral toxicity test
性别 | (mg/kg BW) | (只) | 体重 ( | (只) | (%) | |||
0 d | 7 d | 14 d | 14 d增重 | |||||
雄 | 5000 | 5 | 20.1±1.1 | 30.8±2.0 | 31.2±2.7 | 11.1±1.9 | 0 | 0 |
雌 | 5000 | 5 | 19.9±1.2 | 24.6±0.8 | 27.5±0.8 | 7.7±1.2 | 0 | 0 |

表3 皮肤致敏试验结果汇总表
Table 3 Summary of results of skin sensitization test
组别 | (只) | 剂量 | 剂量 | (h) | 皮肤反应强度 | (%) | |||||||||
红斑 | 水肿 | ||||||||||||||
0 | 1 | 2 | 3 | 4 | 0 | 1 | 2 | 3 | |||||||
阴性对照 | 20 | mL | mL | 24 | 20/20 | 0/20 | 0/20 | 0/20 | 0/20 | 0/20 | 0/20 | 0/20 | 0/20 | 0 | |
48 | 20/20 | 0/20 | 0/20 | 0/20 | 0/20 | 0/20 | 0/20 | 0/20 | 0/20 | 0 | |||||
受试物组 | 20 | mL | mL | 24 | 16/20 | 2/20 | 2/20 | 0/20 | 0/20 | 18/20 | 2/20 | 0/20 | 0/20 | 15.0 | |
48 | 16/20 | 4/20 | 0/20 | 0/20 | 0/20 | 17/20 | 3/20 | 0/20 | 0/20 | 20.0 | |||||
阳性对照 | 20 | 0.6% | 0.3% | 24 | 3/20 | 11/20 | 5/20 | 1/20 | 0/20 | 3/20 | 11/20 | 3/20 | 3/20 | 85.0 | |
48 | 4/20 | 13/20 | 3/20 | 0/20 | 0/20 | 4/20 | 11/20 | 4/20 | 1/20 | 80.0 | |||||
表4 急性皮肤刺激反应结果汇总表
Table 4 Summary of results of acute dermal irritation test
编号 | 性别 | (kg) | 皮肤刺激反应评分 | |||||||||||||||||||||||
24 h | 48 h | 72 h | ||||||||||||||||||||||||
试验组 | 对照组 | 试验组 | 对照组 | 试验组 | 对照组 | |||||||||||||||||||||
红斑 | 水肿 | 总分 | 红斑 | 水肿 | 总分 | 红斑 | 水肿 | 总分 | 红斑 | 水肿 | 总分 | 红斑 | 水肿 | 总分 | 红斑 | 水肿 | 总分 | |||||||||
1 | 雄 | 2.2 | 1 | 0 | 1 | 0 | 0 | 0 | 1 | 0 | 1 | 0 | 0 | 0 | 1 | 0 | 1 | 0 | 0 | 0 | ||||||
2 | 雌 | 2.5 | 1 | 0 | 1 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | ||||||
3 | 雄 | 2.0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | ||||||
4 | 雌 | 2.4 | 1 | 0 | 1 | 0 | 0 | 0 | 1 | 0 | 1 | 0 | 0 | 0 | 1 | 0 | 1 | 0 | 0 | 0 | ||||||
积分均值 | 0.75 | 0 | 0.5 | 0 | 0.5 | 0 | ||||||||||||||||||||
最高积分均值 | 0.75 | |||||||||||||||||||||||||
表5 急性眼刺激性/腐蚀性试验结果汇总表
Table 5 Summary of results of eye irritation/corrosion test
观察时间点 | 角膜 | 虹膜 | 结膜 | 总积分 | ||||||||
(O) | (A) | (O×A×5) | (I) | (I×5) | (R) | (S) | (D) | (R+S+D)×2 | ||||
1 h | 0 | 0 | 0 | 0 | 0 | 1 | 0 | 0 | 2 | 2 | ||
24 h | 0 | 0 | 0 | 0 | 0 | 1 | 0 | 0 | 2 | 2 | ||
48 h | 0 | 0 | 0 | 0 | 0 | 1 | 0 | 0 | 2 | 2 | ||
72 h | 0 | 0 | 0 | 0 | 0 | 1 | 0 | 0 | 2 | 2 | ||
4 d | 0 | 0 | 0 | 0 | 0 | 1 | 0 | 0 | 0 | 2 | ||
7 d | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 | ||
表6 测试环境监测结果汇总表
Table 6 Summary of results of test environment monitoring
剂量 (mg/L) | 监测指标 | 不同观察期 (h) 内监测数据 | 是否合格 | |||
24 | 48 | 72 | 96 | |||
100 | pH | 6.99 | 7.13 | 7.55 | 7.27 | 是 |
温度 (℃) | 21.2 | 20.8 | 22.3 | 24.1 | 是 | |
溶解氧含量 (%) | 71 | 66 | 64 | 70 | 是 | |
受试物浓度 (mg/L) | 99.9 | 99.8 | 99.8 | 99.6 | 是 | |
10 | pH | 6.92 | 7.56 | 7.68 | 7.51 | 是 |
温度 (℃) | 22.6 | 21.9 | 25.7 | 23.5 | 是 | |
溶解氧含量 (%) | 72 | 69 | 74 | 66 | 是 | |
受试物浓度 (mg/L) | 9.9 | 9.9 | 9.8 | 9.7 | 是 | |
1 | pH | 7.13 | 7.68 | 7.55 | 7.72 | 是 |
温度 (℃) | 22.4 | 21.9 | 20.8 | 23.7 | 是 | |
溶解氧含量 (%) | 69 | 72 | 68 | 75 | 是 | |
受试物浓度 (mg/L) | 0.9 | 0.9 | 0.9 | 0.9 | 是 | |
对照 | pH | 7.08 | 7.62 | 7.57 | 7.38 | 是 |
温度 (℃) | 20.5 | 21.7 | 23.9 | 23.0 | 是 | |
溶解氧含量 (%) | 71 | 66 | 65 | 73 | 是 | |
受试物浓度 (mg/L) | 0 | 0 | 0 | 0 | 是 | |
表7 鱼类急性毒性试验结果汇总表
Table 7 Summary of results of acute fish toxicity test
剂量 (mg/L) | 试验鱼数量 (尾) | 不同观察期内斑马鱼死亡数量 (尾) | 96 h死亡率 (%) | |||
24 h | 48 h | 72 h | 96 h | |||
100.00 | 10 | 10 | — | — | — | 100 |
10.00 | 10 | 0 | 0 | 0 | 0 | 0 |
1.00 | 10 | 0 | 0 | 0 | 0 | 0 |
空白对照 | 10 | 0 | 0 | 0 | 0 | 0 |
图6 鱼类急性毒性试验照片
Fig.6 Acute fish toxicity test
基金项目:山东省重点研发计划重大科技创新工程(2021CXGC011306)
第一作者:刘迪(1995—),女,汉族,山东潍坊人,硕士,主管技师,主要从事病原体检测及病媒生物鉴定工作,E-mail: liudi7979@163.com
通信作者:滕新栋(1987—),男,汉族,山东青岛人,博士,副主任技师,主要从事病原体检测及病媒生物鉴定工作,E-mail: tengxindong@163.com
1. 青岛海关 青岛 266071
2. 青岛中心医院 青岛 266042
1. Qingdao Customs, Qingdao 266071
2. Qingdao Central Hospital, Qingdao 266042