CopyRight 2009-2020 © All Rights Reserved.版权所有: 中国海关未经授权禁止复制或建立镜像
显色双层平板法定量检测即食水产品中副溶血性弧菌
作者:田卓 顾晗潇 李长征 李辉 麻丽丹
田卓 顾晗潇 李长征 李辉 麻丽丹
摘 要 本研究参照GB 4789.2—2016、GB 4789.7—2013中方法,使用具备计数和显色功能的培养基,分别对副溶血性弧菌标准菌株、调味杂色蛤肉、腌青虾和冰鲜八爪鱼样品进行副溶血性弧菌检测。实验结果显示,在显色双层平板上副溶血性弧菌菌落呈淡紫色,调味杂色蛤肉、腌青虾和冰鲜八爪鱼样品人工染菌样品实验与3% NaCl NA平板的结果无显著差异。结果表明,本研究建立的显色双层平板方法具备灵敏度高、快速、操作简便等优点,适合用于即食水产制品中副溶血性弧菌直接定量检测,能够如实反映即食水产品受污染的情况。
关键词 副溶血性弧菌;显色双层平板;定量法;即食水产品
Chromogenic Bilayer Plate Method for Quantitative Detection of Vibrio parahaemolyticus in Ready-to-eat Aquatic Products
TIAN Zhuo 1 GU Han -X iao 2 LI Chang -Z heng 3 LI Hui 3 MA Li-Dan 4 *
Abstract This study referred to the methods in GB 4789.2-2016 and GB 4789.7-2013, and used culture media with counting and colorimetric functions to detect Vibrio parahaemolyticus in standard strains of Vibrio parahaemolyticus, seasoned variegated clam meat, pickled green shrimp, and iced octopus samples. The experimental results showed that the colony of Vibrio parahaemolyticus appeared light purple on the chromogenic bilayer plate, and there was no significant difference between the results of artificial contaminated bacteria samples of seasoned variegated clam meat, pickled green shrimp, and iced octopus and those on the 3% NaCl NA plate. The results indicate that the chromogenic bilayer plate method established in this study has advantages of high sensitivity, rapidity and easy operation, and is suitable for direct quantitative detection of Vibrio parahaemolyticus in ready-to-eat aquatic products. It can accurately reflect the contamination of ready-to-eat aquatic products.
Keywords Vibrio parahaemolyticus; chromogenic bilayer plate; quantitative method; ready-to-eat aquatic products
基金项目:大连海关科研项目(2022DK06)
第一作者:田卓(1982—),女,汉族,辽宁沈阳人,硕士,高级工程师,主要从事食品安全研究工作,E-mail: tianzhuo1113@163.com
通信作者:麻丽丹(1976—),女,汉族,浙江丽水人,硕士,正高级工程师,主要研究方向为食品微生物检测工作,E-mail: 2212097@163.com
1. 大连海关技术中心 大连 116000
2. 大连海关综合技术服务中心 大连 116000
3. 大东港海关综合技术服务中心 东港 118399
4. 丹东海关综合技术服务中心 丹东 118000
1. Technology Center of Dalian Customs District, Dalian 116000
2. Dalian Customs Comprehensive Technical Service Center, Dalian 116000
3. Comprehensive Technical Service Center of Dadonggang Customs, Donggang 118399
4. Comprehensive Technical Service Center of Dandong Customs, Dandong 118000
副溶血性弧菌(Vibrio parahaemolyticus,VP)是革兰氏阴性弧菌,在含有0.5%~8%氯化钠的环境中旺盛生长[1-3],广泛分布于海产品、海水及盐渍食品中[4-6]。副溶血性弧菌是一种食源性致病菌[7],摄入未充分煮熟、被弧菌污染的水产品会引起食物中毒,引发胃肠炎、呕吐、腹泻等症状[8-10],是我国食源性细菌中毒事件中主要致病菌之一[11-13]。近年来,由副溶血性弧菌引发的食物安全事件呈上升趋势,对人类的身体健康造成了严重的威胁[14-19]。李薇薇等[20]研究报道称2003—2017年我国食源性疾病相关病例报告中由副溶血性弧菌引发的食源性疾病占11.3%,该致病因子位居流行病原菌的第2位。我国副溶血性弧菌所致的食源性疾病70%以上由动物性水产品引起[21-22]。这是由于我国水产品养殖多以近海养殖或滩涂养殖为主,海水温度较高,为副溶血性弧菌的生存和繁殖提供了适宜的环境条件。因此,对水产品中副溶血性弧菌进行定量检测和实时监控具有重要意义。
GB 4789.7—2013《食品安全国家标准 食品微生物学检验 副溶血性弧菌检验》[23]中副溶血性弧菌的定量检测使用最大可能数(Most probable number,MPN)计数法,但该法采用多管发酵技术,存在操作繁琐、耗时长等问题,既给企业自检自控带来了困难,也不利于出口水产品的快速检验和通关放行[24]。随着生物技术的不断发展,选择性更强、灵敏度更高的培养基[25](包括液体增菌液和显色分离培养基)被应用到检测过程中。例如,弧菌显色培养基就是利用弧菌对亚硝酸盐的还原作用,使培养基中的亚硝酸盐还原成亚氨基化合物,从而产生红色染色反应,来鉴别弧菌的感染,这样不仅有利于目标菌的富集,使目标菌易于识别,更重要的是有效提高了筛选效率。基于以上原理,本研究采用显色双层平板涂布方法对副溶血性弧菌进行定量检测,上层非选择性培养基对副溶血性弧菌起到壮大作用,下层选择性培养基(显色培养基)可以抑制非目标菌生长并使目标菌表现出区别于非目标菌的明显生长形态特征,达到定量检测副溶血性弧菌的目的。
1 材料与方法
1.1 材料与仪器
ATCC 17802副溶血性弧菌标准菌株购自中国工业菌种保藏中心(CICC),保存于-80℃;调味杂色蛤肉、腌青虾和冰鲜八爪鱼购自本地水产市场;弧菌显色培养基购自法国科玛嘉CHROMagar公司;3%氯化钠胰蛋白胨大豆琼脂(3% NaCl TSA)、3%氯化钠营养琼脂(3% NaCl NA)、3%氯化钠三糖铁琼脂(3% NaCl TSI)、无盐胰胨水、3%氯化钠碱性蛋白胨水(3% NaCl APW)、6% NaCl胰胨水、8%NaCl胰胨水、10% NaCl胰胨水购自青岛海博生物技术有限公司;API 20E鉴定试剂条购自法国梅里埃公司;BAGMIXER 400均质器购自美国Interscience公司;恒温培养箱购自德国宾得公司。
1.2 实验方法
1.2.1 显色双层平板的制备
倾注已融化的10~15 mL的3% NaCl NA琼脂培养基于培养皿中,待其冷却凝固后于2~8℃保存备用。按照GB 4789.10—2016《食品安全国家标准 食品微生物学检验 金黄色葡萄球菌检验》[26]平板计数法接种待检测的样品稀释液后置于(36±1)℃培养箱中培养2~4 h,再在上面倾倒约5 mL弧菌显色培养基,凝固后置于(36±1)℃培养箱中培养18~24 h,平板上的紫红色菌落即为副溶血性弧菌,对紫红色菌落进行计数。
1.2.2 定量检测平板的筛选
副溶血性弧菌标准菌株参照GB 4789.28—2013《食品安全国家标准 食品微生物学检验 培养基和试剂的质量要求》[27]方法制备菌液,将标准菌株ATCC 17802接种到3% NaCl APW中,于(36±1)℃培养18~24 h。用3% NaCl APW对菌悬液进行连续梯度稀释,至稀释度为10-5 CFU/g和10-6 CFU/g,2个稀释度各吸取0.3 mL、0.3 mL和0.4 mL菌悬液分别接种于3% NaCl NA平板、TCBS平板和显色双层平板,培养后观察菌落特征,挑选典型菌落进行氧化酶试验、嗜盐性试验、涂片镜检、API 20E生化鉴定试剂盒鉴定。
1.2.3 显色双层平板定量检测方法的应用
1)样品本底中副溶血性弧菌检测。将调味杂色蛤肉、腌青虾和冰鲜八爪鱼样品25 g加入225 mL 3% NaCl APW,均质混合,稀释液划线于TCBS平板,于(36±1)℃培养18~24 h。
2)人工染菌样品的显色双层平板法定量检测。吸取1 mL副溶血性弧菌标准菌株菌悬液于已均质混匀的调味杂色蛤肉、腌青虾和冰鲜八爪鱼样品中,作为人工染菌样品,参照1.2.2进行梯度稀释、培养和计数,计算每克人工染菌样品中副溶血性弧菌菌落形成单位。
1.3 数据处理
采用GraphPad Prism 9分析软件,对检测结果进行处理和分析。
2 结果与分析
2.1 定量检测平板的筛选
副溶血性弧菌标准菌株在弧菌显色培养基上菌落形态为大小均匀、淡紫色,在TCBS平板上菌落形态为绿色圆形的半透明菌落。生化鉴定结果为氧化酶试验阳性,革兰氏染色阴性、棒状,有鞭毛,无芽孢,无氯化钠的胰胨水中不生长,6% NaCl胰胨水中生长,8% NaCl胰胨水中生长,10% NaCl的胰胨水中不生长,API 20E鉴定结果为副溶血性弧菌。
以3% NaCl NA为对照,显色双层平板上菌落数量无显著性差异,并且显示明显的淡紫色,可方便快捷地识别非目标菌与目标菌,同时可实现直接定量。而TCBS平板上菌落数量显著减少,因此选择显色双层平板为副溶血性弧菌定量检测平板进行后续试验。副溶血性弧菌标准菌株在显色双层平板上结果如图1所示。

图1 副溶血性弧菌标准菌株在显色双层平板上的结果
Fig.1 Results of standard strains of Vibrio parahaemolyticus on the chromogenic bilayer plate
2.2 试验样品本底检测结果
试验样品培养结果显示3种样品均不含副溶血性弧菌。
2.3 人工染菌样品的显色双层平板法定量检测
人工染菌的调味杂色蛤肉、腌青虾和冰鲜八爪鱼样品中副溶血性弧菌定量检测结果见表1。同一人工染菌样品采用3种不同平板直接定量检测副溶血性弧菌结果如图2—图4所示。从图2可知,在人工染菌的调味杂色蛤肉样品中,采用3% NaCl NA平板和显色双层平板的计数结果之间无显著性差异(P = 0.1012,P≥0.05);采用显色双层平板和TCBS平板的计数结果之间存在极显著差异(P = 0.0014,P<0.01);采用3% NaCl NA平板和TCBS平板进行直接定量检测的计数结果之间存在极显著差异(P = 0.0021,P<0.01)。
从图3可知,在人工污染的腌青虾样品中,采用3% NaCl NA平板和显色双层平板进行直接定量检测的计数结果之间无显著性差异(P = 0.4918,P≥0.05);采用显色双层平板和TCBS平板进行直接定量检测的计数结果之间存在极显著差异(P = 0.0002,P<0.01);采用3% NaCl NA平板和TCBS平板进行直接定量检测的计数结果之间存在极显著差异(P = 0.0002,P<0.01)。
从图4可知,在人工污染的冰鲜八爪鱼样品中,采用3% NaCl NA平板和显色双层平板进行直接定量检测的计数结果之间无显著性差异(P = 0.2051,P≥0.05);采用显色双层平板和TCBS平板进行直接定量检测的计数结果之间存在极显著差异(P = 0.0013,P<0.01);采用3% NaCl NA平板和TCBS平板进行直接定量检测的计数结果之间存在极显著差异(P = 0.0022,P<0.01)。
以3% NaCl NA平板为对照,显色双层平板上菌落数量与其并无显著性差异,并且显色双层平板上的菌落均呈现特征性的淡紫色,易于识别,方便计数;而TCBS平板上的菌落数量与其比较明显减少,结果偏差较大。
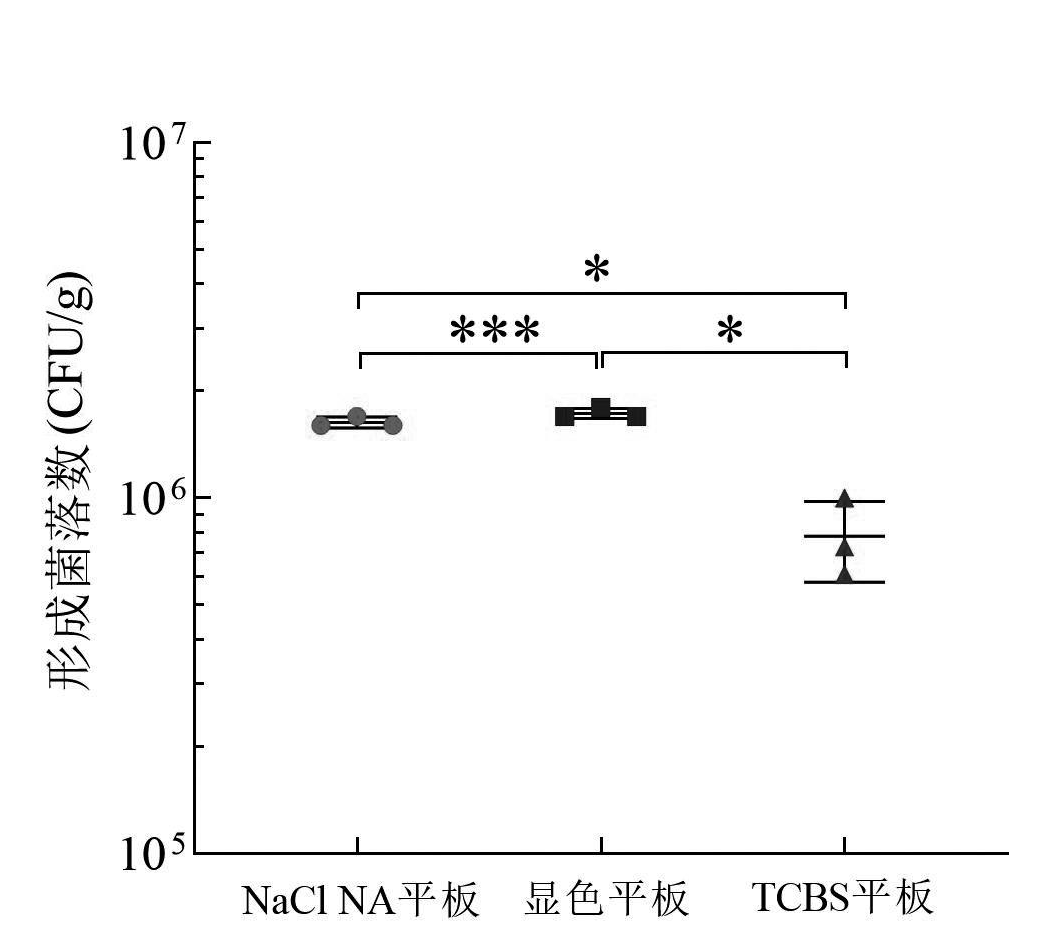
*表示P<0.01; ***表示P≥0.05
图2 调味杂色蛤肉样品采用3种不同平板计数的结果分析
Fig.2 Counting results of seasoned variegated clam meat samples on three types of plates

*表示P<0.01; ***表示P≥0.05
图3 腌青虾样品采用3种不同平板计数的结果分析
Fig.3 Counting results of pickled green shrimp samples on three types of plates
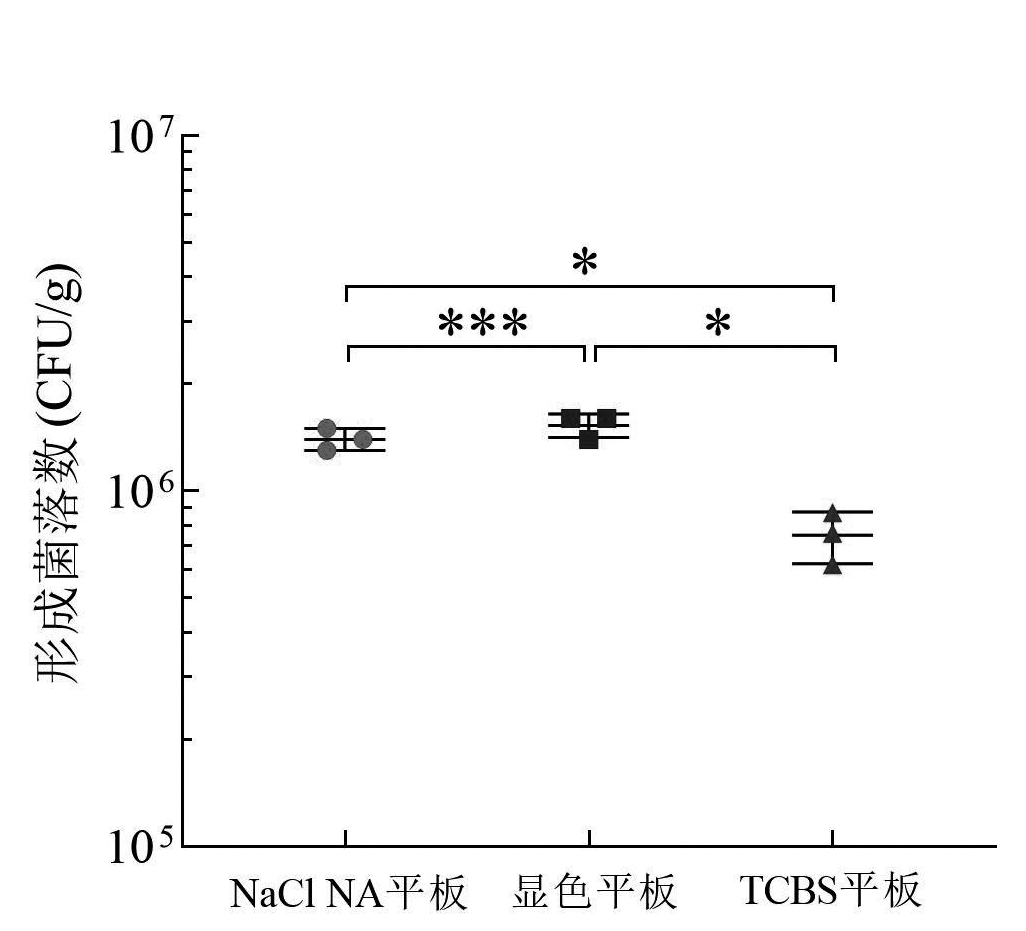
*表示P<0.01; ***表示P≥0.05
图4 冰鲜八爪鱼样品采用3种不同平板计数的结果分析
Fig.4 Counting results of iced octopus samples on three types of plates
综上所述,在3种不同的食品基质中,从检测结果的一致性和差异性进行分析,采用3% NaCl NA平板和显色双层平板直接定量检测副溶血性弧菌的结果均好于采用TCBS平板直接定量检测的结果,但副溶血性弧菌在3% NaCl NA平板上没有特征性的颜色菌落,显色双层平板直接定量检测结果则更接近于真实值。
3 结论和讨论
副溶血性弧菌是引起食源性疾病的重要病原菌之一,简便快速精确的检测方法对副溶血性弧菌的早期识别、提前防控及预警具有重要意义[28-30]。但现行采用的选择性培养基(如弧菌显色琼脂)对副溶血性弧菌进行培养的方法存在回收率低的问题。本研究采用双层平板计数法,使用3% NaCl NA琼脂和显色培养基对副溶血性弧菌进行平板计数,实现了副溶血性弧菌的直接定量检测。该方法与传统培养方法相比,直接定量结果灵敏度明显高于TCBS平板;与分子生物学等快速检测方法相比,无需高昂的仪器设备和复杂的技术要求及环境要求,具有选择性强、准确快速、操作简便的特点。本方法灵敏度高、方便快捷,可实现水产品中副溶血性弧菌的实时定量监控,从而减少副溶血性弧菌引起的食品安全风险,保障食品安全和人员饮食安全。该方法的广泛应用,可为针对水产制品中副溶血性弧菌的食品安全性检测研究提供简便稳定的技术支持和理论依据,方便企业自检自控,有利于出口水产品的快速检验和便利通关,促进水产品出口贸易发展。
参考文献
[1] RYU A R, MOK J S, LEE D E, et al. Occurrence, virulence, and antimicrobial resistance of Vibrio parahaemolyticus isolated from bivalve shellfish farms along the southern coast of Korea[J]. Environmental Science and Pollution Research, 2019, 26(20): 21034-21043.
[2] 吴斌, 胡元玮, 方琼楼, 等. 金华市淡水产品中副溶血性弧菌污染状况及PFGE分型研究[J]. 中国卫生检验杂志, 2022, 32(15): 1829-1831.
[3] 侯立杰. 重庆地区水产品中副溶血性弧菌的污染情况调查和分离株的毒力因素及药物敏感性研究[D]. 重庆: 西南大学, 2013.
[4] LEE K K, LIU P C, HUANG C Y. Vibrio parahaemolyticus infectious for both humans and edible mollusk abalone[J]. Microbes and Infection, 2003, 5(6): 481-485.
[5] 赵现锋, 王舒, 周晓屏, 等. 水产品中副溶血性弧菌快速检测技术研究进展[J]. 食品安全质量检测学报, 2018, 9(4): 884-889.
[6] ZHU P, GAO W, HUANG H, et al. Rapid Detection of Vibrio parahaemolyticus in Shellfish by Real-Time Recombinase Polymerase Amplification[J]. Food Analytical Methods, 2018, 11(8): 2076-2084.
[7] 杨珺. 鱼肉污染副溶血弧菌非预增菌快速检测方法的研究[D]. 江西: 江西农业大学, 2021.
[8] 梅玲玲, 潘雪霞, 朱敏, 等. 浙江省副溶血性弧菌污染水平及贝类海产品风险评估[J]. 中国人兽共患病学报, 2012, 28(7): 700-704+717.
[9] 郑雷军, 吕岩, 王李伟, 等. 上海地区婚宴食物中毒发生情况及预防措施[J]. 上海预防医学, 2012, 24(5): 262-263.
[10] 寇秀颖, 周宝青, 陈玲, 等. CRISPR/Cas系统在食源性致病菌快速检测新技术中的研究进展[J]. 食品科学, 2023, 44(7): 313-323.
[11] JEAMSRIPONG S, KHANT W, CHUANCHUEN R. Distribution of phenotypic and genotypic antimicrobial resistance and virulence genes in Vibrio parahaemolyticus isolated from cultivated oysters and estuarine water[J]. FEMS Microbiology Ecology, 2020, 96(8): fiaa081.
[12] 任淑敏, 张良军, 刘凡, 等. 一起由副溶血性弧菌引起的食源性疾病的病原学研究及溯源分析[J]. 食品安全质量检测学报, 2018, 9(4): 741-745.
[13] 刘旭. 海水养殖源弧菌耐药性调查及qnrVC基因在弧菌中的流行情况研究[D]. 上海: 上海海洋大学, 2016.
[14] 付萍, 王连森, 陈江, 等. 2015年中国大陆食源性疾病暴发事件监测资料分析[J]. 中国食品卫生杂志, 2019, 31(1): 64-70.
[15] 翁琴云. 厦门市水产品中副溶血性弧菌和溶藻弧菌的污染状况研究[J]. 现代食品, 2022, 28(8): 180-182+201.
[16] 马聪, 谭海玲, 刘礼平, 等. 副溶血性弧菌鉴定能力验证样品的制备[J].中国食品卫生杂志, 2011, 23(6): 515-519.
[17] 于纪棉, 倪晶晶, 陶冬英, 等. 进口水产品中副溶血性弧菌耐药性和毒力基因的调查[J]. 中国食品卫生杂志, 2014, 26(4): 320-323.
[18] 时晨, 于良, 王悦, 等. 秦皇岛市一起由副溶血性弧菌引起的食源性疾病暴发事件的检测和溯源分析[J]. 食品安全质量检测学报, 2021, 12(9): 3503-3507.
[19] 吴丽珠, 高红梅, 杨洋, 等. 一起副溶血性弧菌所致食源性疾病暴发的流行病学调查[J]. 上海预防医学, 2022, 34(6): 587-590+600.
[20] LI W W, PIRES S M, LIU Z, et al. Surveillance of foodborne disease outbreaks in China, 2003—2017[J]. Food Control, 2020, 118: 107359.
[21] 秦文彦, 王静, 姚素霞, 等. 太原市零售肉制品中食源性致病菌的污染现状和菌型特征[J]. 中华微生物学和免疫学杂志, 2019, 39(10): 731-736.
[22] 方瑛, 雷亚虹, 蓝红英, 等. 2017—2021年浙江省建德市腹泻人群副溶血性弧菌感染现状及病原学特征分析[J]. 中国公共卫生管理, 2023, 39(4): 570-572.
[23] GB 4789.7—2013 食品安全国家标准 食品微生物学检验 副溶血性弧菌检验[S]. 北京: 中国标准出版社, 2013.
[24] 张淑红, 吴清平, 张菊梅, 等. 副溶血性弧菌显色培养基检测效果初步评价[J]. 微生物学通报, 2008, 35(1): 145-148.
[25] 易青, 宁喜斌. 沙门菌、金黄色葡萄球菌、副溶血性弧菌的选择性共增菌培养基的研制[J]. 中国食品卫生杂志, 2023, 35(4): 510-516.
[26] GB 4789.10—2016 食品安全国家标准 食品微生物学检验 金黄色葡萄球菌检验[S]. 北京: 中国标准出版社, 2016.
[27] GB 4789.28—2013 食品安全国家标准 食品微生物学检验 培养基和试剂的质量要求[S]. 北京: 中国标准出版社, 2013.
[28] 吴晓芳, 陈莉萍, 沈月华, 等. 一起由副溶血性弧菌引起的聚集性腹泻事件的病原特征分析[J]. 中国食品卫生杂志, 2023, 35(5): 768-771.
[29] 黎梓怡, 施春雷. 泛基因组学在食源性致病菌检测及其耐药监测中的应用[J]. 食品安全质量检测学报, 2022, 13(14): 4472-4478.
[30] 杨铭锋, 徐新悟, 林文凭, 等. 慈溪市一起新血清型副溶血性弧菌引起的食源性疾病暴发分析[J]. 中国卫生检验杂志, 2023, 33(17): 2157-2159.
表1 3种平板计数结果
Table 1 Counting results of three types of plates
样品 | 计数结果 (×106 CFU/g) | ||
3% NaCl NA平板 | 科玛嘉弧菌显色双层平板 | TCBS平板 | |
调味杂色蛤肉 | 1.6、1.6、1.7 | 1.7、1.7、1.8 | 1.0、0.73、0.61 |
腌青虾 | 2.0、1.9、1.8 | 1.9、1.9、2.1 | 0.44、0.63、0.72 |
冰鲜八爪鱼 | 1.4、1.3、1.5 | 1.6、1.4、1.6 | 0.62、0.76、0.87 |







