CopyRight 2009-2020 © All Rights Reserved.版权所有: 中国海关未经授权禁止复制或建立镜像
粮谷中杀螺胺乙醇胺盐残留量的测定
作者:郭雨 施亚申 严静华 林桦
郭雨 施亚申 严静华 林桦
摘 要 本研究建立了一种液相色谱-串联质谱法测定粮谷中杀螺胺乙醇胺盐残留量的方法。采用改进的QuEChERS方法,样品经一定体积比的氨水乙腈超声提取,冷冻高速离心,N-丙基乙二胺(PSA)分散萃取净化材料净化,采用安捷伦Zorbax C18色谱柱分离,高效液相色谱串联质谱仪检测,通过外标法准确定量。杀螺胺乙醇胺盐在0.2~20.0 μg/L浓度范围内,7个空白基质标准曲线浓度点具有较好的线性关系,相关系数R2>0.995,杀螺胺乙醇胺盐的检出限为0.3 μg/kg,定量限为1.0 μg/kg;在1.0 μg/kg、5.0 μg/kg和10.0 μg/kg 3个不同浓度加标水平下,粮谷中杀螺胺乙醇胺盐6次平行试验结果的平均回收率为83.5%~122.7%,相对标准偏差在1.1%~9.4%之间。结果表明,该方法样品前处理操作简便、耗时短、检测耗材成本低、结果重复性佳,能够满足日常粮谷中杀螺胺乙醇胺盐残留的检测要求。
关键词 粮谷;杀螺胺乙醇胺盐;QuEChERS
Method for Determination of Niclosamide-Olamine Residues in Grains
GUO Yu 1 SHI Ya-Shen 2 YAN Jing-Hua 1 LIN Hua 3
Abstract A method was established to determine residue of niclosamide-olamine in grains by LC-MS/MS. Using the improved QuEChERS method, the samples were ultrasonically extracted by a certain volume ratio of ammonia acetonitrile, centrifuged at high speed in a refrigerated state, purified with PSA. They were separated by Agilent Zorbax C18 chromatographic column, detected by high-performance liquid chromatography tandem mass spectrometer, and accurately quantified by external standard method. In the concentration range of 0.2-20.0 μg/L, the concentration points of the 7 blank matrix standard curves had a good linear relationship, with the correlation coefficient (R²)>0.995, and the detection limit of niclosamide-olamine was 0.3 μg/kg and the limit of quantification was 1.0 μg/kg. The average recoveries of six parallel tests of niclosamide-olamine in grains were 83.5%-122.7%, and the relative standard deviations were 1.1%-9.4% under three different concentration spike levels of 1.0 μg/kg, 5.0 μg/kg and 10.0 μg/kg. This method has simple sample pre-treatment, short analysis time, low cost of detection consumables, and good reproducibility. It can meet the detection requirements for the residues of niclosamide-olamine in grains.
Keywords grain; niclosamide-olamine; QuEChERS
第一作者:郭雨(1988—),男,汉族,江苏昆山人,本科,工程师,主要从食品农产品中农药和兽药残留研究工作,E-mail: 294282 308@qq.com
1. 江苏安舜技术服务有限公司 苏州 215332
2. 苏州海关综合技术中心 苏州 215104
3. 早康枸杞股份有限公司 中卫 755100
1. Alex Stewart Agricultural Ltd, Suzhou 215332
2. Comprehensive Technology Center of Suzhou Customs, Suzhou 215104
3. ZaoKang Goji Berry INC, Zhongwei 755100
食品安全始终是广大人民群众最关心也是最关注的问题之一。为减少病虫害给粮食带来的危害,在实际生产过程中化学农药的使用必不可少,但与此同时,违规农药的使用也屡见不鲜。
杀螺胺乙醇胺盐,又称氯硝柳胺乙醇胺盐,主要用做灭钉螺药,对水稻福寿螺[1]的杀灭作用迅速,效果好,且对环境安全,因此被广泛应用于水稻种植业。GB 2763—2021《食品安全国家标准 食品中农药最大残留限量》[2]规定了在稻谷和糙米中杀螺胺乙醇胺盐(残留物以杀螺胺计)的最大残留限量,分别为稻谷2 mg/kg,糙米0.5 mg/kg。杀螺胺乙醇胺盐的测定方法主要有高效液相色谱串联质谱法和高效液相色谱法,其中高效液相色谱串联质谱法多应用于水产品[3-4]、底泥和环境水质[5-7]中杀螺胺乙醇胺盐的测定,GB 31656.7—2021《食品安全国家标准 水产品中氯硝柳胺残留量的测定 液相色谱-串联质谱法》[8]也规定了鱼、虾、鳖等水产品可食组织中氯硝柳胺残留量的测定;也有文献报道使用高效液相色谱法测定水稻[9]和水体[10]中杀螺胺乙醇胺盐残留量的分析方法,但大多数采用传统的提取和净化技术,不但耗时且步骤复杂,需要使用大量的提取溶剂,对环境不友好,检测结果相对不稳定,方法的检出限/定量限较高。
本研究基于改进的QuEChERS方法,采用高效液相色谱串联质谱仪检测技术,建立了一种快速、高效、稳定、灵敏度高的测定粮谷中杀螺胺乙醇胺盐残留量的方法。
1 材料与方法
1.1 设备与试剂耗材
高效液相色谱串联质谱仪:1260-6460(美国Agilent公司);Vortsx 3小型高速涡旋仪(德国IKA公司); 5000系列往复式振动摇床(美国Talboys公司);2400 TH超声波清洗仪(上海安谱公司);X3R高速离心机(美国Thermo Fisher Scientific公司) 。
杀螺胺乙醇胺盐标准品(1 mg/mL,A Chemtek Inc公司);乙腈(LC-MS级)、甲酸(LC-MS级)、乙酸铵(LC-MS级)、N-丙基乙二胺(PSA)、石墨化碳黑(GCB)、十八烷基硅烷(C18)、QuEChERS萃取盐包(含4 g无水硫酸镁,1.0 g氯化钠,1.0 g二水合柠檬酸三钠,0.5 g半水柠檬酸氢二钠)均采购自上海安谱公司;氨水(GR)采购自国药集团。实验用水:商品化蒸馏水经过美国密理博Millipore制备的一级水。
1.2 分析与方法
1.2.1 提取与净化
准确称取(5±0.05)g的样品于50 mL具螺纹塞的塑料离心管中,加入8 mL水,合盖,涡旋混匀1 min,放置10 min。加入10 mL乙腈、50 μL氨水,涡旋仪涡旋1 min,往复式摇床振荡15 min,超声波清洗仪超声10 min,加入QuEChERS萃取盐包,涡旋仪涡旋1 min,转移至冷冻冰箱,-5℃冷冻约30 min,4700 r/min冷冻(-4℃)离心5 min。小心移取上清液1 mL转移至10 mL带盖塑料圆底离心管中,加入50 mg PSA粉末,涡旋仪小心涡旋30 s,立即取上清液过0.22 μm有机相滤膜,高效液相色谱-串联质谱仪分析。
1.2.2 仪器分析条件
色谱条件。安捷伦Zorbax C18色谱柱(规格:2.1 mm×150 mm,粒径3.5 μm);柱温箱温度:40℃;流动相A为5 mmol/L乙酸铵水溶液(含0.1%甲酸),流动相B为乙腈。流动相洗脱梯度:0~1.5 min,50% A;2.1~6 min,A从50%~10%;6.2~8.0 min,50% A,保持3 min;流速0.4 mL/min;进样量5 μL。
质谱条件。离子源类型:AJS电喷雾离子源负离子扫描(ESI-),毛细管电压:3500 V,雾化器压力:35 psi;干燥气温度:325℃,干燥气流速:10 L/min;鞘气温度:350℃,鞘气流速:11 L/min,采集方式:多反应监测(MRM模式)。
1.2.3 溶液配置与标准曲线制备
将杀螺胺乙醇胺盐标准溶液(1 mg/mL)用乙腈逐级稀释到0.01 mg/mL作为中间储备液,有效期3个月。
使用合适的稻谷空白样品(不含任何相关的分析残留物),按照1.2.1所述进行样品提取和净化,得到空白基质溶液。在配置的标准工作溶液曲线中先分别加入100 μL空白基质溶液,然后配置成0.2 μg/L、 0.5 μg/L、1.0 μg/L、2.0 μg/L、5.0 μg/L、10 μg/L、20 μg/L共7个点的空白基质标准工作溶液曲线。
1.2.4 杀螺胺乙醇胺盐残留量计算
外标法计算出实际样品中杀螺胺乙醇胺盐残留量(以杀螺胺计)。
1.2.5 添加回收试验
在稻谷、小麦、玉米、燕麦空白样品中分别添加1倍、5倍和10倍定量限的杀螺胺乙醇胺标准溶液,即1.0 μg/kg,5.0 μg/kg和10.0 μg/kg 3个不同浓度的加标,样品按照1.2.1所述提取与净化方法每个浓度水平分别进行6次平行试验,结果统计分析,计算回收率和相对标准偏差。
2 结果与讨论
2.1 质谱条件优化
杀螺胺乙醇胺盐的分子结构式如图1所示。
图1 杀螺胺乙醇胺盐的分子结构式
Fig.1 Molecular structural formula of niclosamide-olamine
杀螺胺乙醇胺盐中因乙醇胺分子为游离态,在实际的质谱分析过程中不参与离子化,实际检测化合物为杀螺胺。将10 mg/L的杀螺胺标准溶液通过质谱自动优化软件,对其母离子进行扫描,因杀螺胺含有多个含氯原子和羟基基团,因此杀螺胺在负离子模式下能够产生更多的[M-H]-分子离子,优化的母离子为m/z 325。随后按照仪器自动优化软件,分别找出定量和定性子离子以及对应的碰撞能量,结果见表1。
表1 杀螺胺的质谱图条件
Table 1 Ion pairs information of niclosamide-olamine
化合物名称 | (m/z) | (m/z) | (V) | (eV) | 极性 |
杀螺胺 | 325 | 289* | 80 | 8 | 负离子 |
325 | 171 | 80 | 24 |
注: *代表定量离子.
2.2 色谱条件的改善
文献和国家标准中多以磷酸盐、甲醇-水或者乙腈-水作为流动相,但是在实际实验过程中发现,使用甲醇-水或者乙腈-水作为流动相时,杀螺胺在色谱图上会出现峰前舌的现象(图2)。因杀螺胺显示一定的酸性,并且pKa值约为5.6,当pH = 7.4时,杀螺胺分子以去质子化的形式存在,因此,色谱分析的流动相中应添加适当浓度的缓冲盐来调整合适的pH。通过不断地优化分析,当加入0.1%甲酸和5 mmol/L乙酸铵时,能够有效地改善峰形同时增加分析化合物的灵敏度。因此,最终选择含有0.1%甲酸和5 mmol/L乙酸铵水溶液和乙腈作为流动相。
2.3 提取
通常水稻、小麦等粮谷产品为了能够长久保存,在仓储前需要将其烘干,要求水分含量小于14.5%。因此,在粮谷样品检测过程中,加入适量的水一是能够避免乙腈与蛋白质直接接触,蛋白质变性会使样品表面区域结块,从而引起提取试剂与样品接触不充分;二是植物细胞在吸收水分后能够充分地舒展开,细胞间间隙增大,在有机试剂提取过程中能够与目标化合物充分接触,大大增加提取效率[11]。本实验考虑过甲醇、乙腈、乙酸乙酯、二氯甲烷提取,因乙腈的渗透性较强,基质离子化作用小,对粮谷中蛋白质有沉淀效果,杀螺胺显示一定的酸性,并且其pKa值约为5.6,加入一定量的氨水能够更好地提取目标化合物,因此加入50 μL氨水加大提取效率。
2.4 净化吸附剂的选择
常规的净化材料分别为N-丙基乙二胺(PSA)、石墨化碳黑(GCB)和十八烷基硅烷(C18),为考量净化材料是否对目标物质有吸附,以及不同使用量对于目标物质的吸附程度,分别配制3组,共9个10 μg/L的杀螺胺标准溶液1 mL,分别加入50 mg、 100 mg、 200 mg的N-丙基乙二胺(PSA)、石墨化碳黑(GCB)和十八烷基硅烷(C18),涡旋,混匀,过膜,进行液相色谱串联质谱仪分析。结果表明,石墨化碳黑(GCB)和十八烷基硅烷(C18)均对杀螺胺有极强的吸附性,而N-丙基乙二胺(PSA)对目标物的吸附程度较低,且随着用量的增加,吸附程度逐步加大(图3)。因此,选择N-丙基乙二胺(PSA)作为净化吸附剂,且添加量为50 mg。
2.5 空白基质溶液标准曲线确定
按照1.2.1中所述进行样品提取和净化,得到空白基质溶液。考虑到样品基质对于目标物质在提取过程中的影响,为抵消这部分基质对于目标物质的影响,分别配置添加了50 μL、100 μL、150 μL、200 μL、300 μL、400 μL和500 μL空白基质溶液的5.0 μg/L,体积为1 mL的标准溶液,液相色谱串联质谱仪分析结果见表4。结果表明,从添加100 μL空白基质溶液开始,基质对于目标物质几乎无影响,因此,综合考虑到样品基质对于仪器的污染和对结果的影响,在制作标准曲线时加入100 μL空白基质溶液比较合适。

图4 添加空白基质溶液的体积对杀螺胺标准溶液的影响
Fig.4 Effects of the volume of blank matrix solutions on the standard solution of niclosamide
2.6 不同空白基质对于结果定量的影响
考虑到不同空白基质标准溶液曲线可能对于定量结果的影响,因稻谷易获得且种植范围广,因此选用空白稻谷样品,按照1.2.1提取和净化,并按照1.2.3制作标准溶液曲线,对稻谷、小麦、玉米和燕麦样品分别加标10.0 μg/kg,做6次平行试验,计算回收率(图5)。结果表明,使用空白稻谷样品,对于小麦、玉米和燕麦样品加标10.0 μg/kg,回收率为98%~120%,选用空白稻谷样品制作的标准溶液曲线对于稻谷、小麦、玉米和燕麦样品中目标物质的分析基本无影响,具有普遍适用性,因此本研究采用稻谷作为空白基质样品。
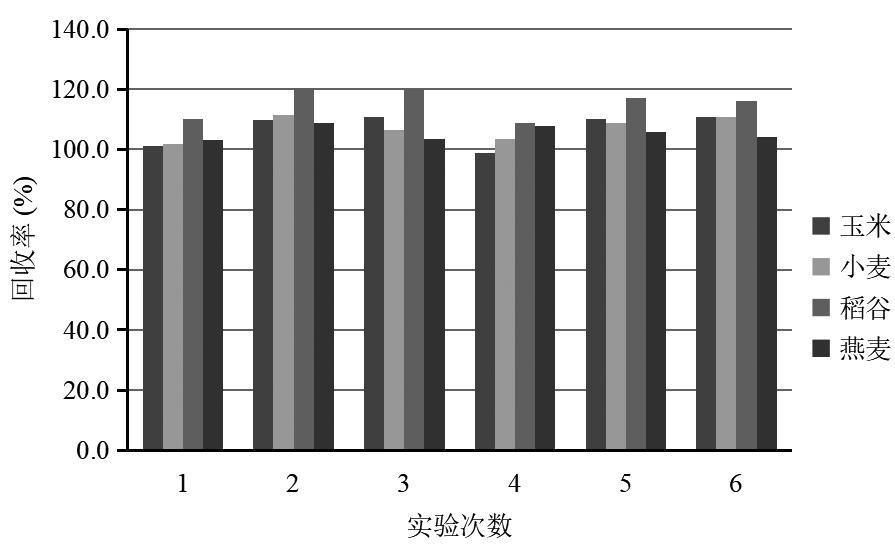
图5 稻谷基质标准溶液曲线对于小麦、玉米和燕麦样品的影响
Fig.5 Effects of rice matrix standard solution curves on wheat, corn and oat samples
2.7 方法的线性、检出限和定量限
杀螺胺在0.2~20.0 μg/L的浓度范围内,线性的相关系数R2>0.995(图6),杀螺胺的检出限为0.3 μg/kg,定量限为1.0 μg/kg,满足日常检测要求。
2.8 回收率和相对标准偏差
在1.0 μg/kg,5.0 μg/kg和10.0 μg/kg 3个不同浓度的添加水平下,稻谷、小麦、玉米和燕麦中杀螺胺的回收率和相对标准偏差结果见表2。
表2 添加浓度及其回收率和相对标准偏差(n = 6)
Table 2 Addition concentration, recovery rate and relative standard deviation(n = 6)
样品名称 | 添加浓度 (μg/kg) | 回收率 (%) | 相对标准偏差 (%) |
稻谷 | 10.0 | 98.9 ~ 110.9 | 4.3 |
小麦 | 10.0 | 102.0 ~ 111.4 | 3.0 |
玉米 | 10.0 | 108.8 ~ 120.4 | 3.4 |
燕麦 | 10.0 | 103.2 ~ 108.6 | 1.8 |
3 结论
本研究依据基质的特性,通过改良的QuEChERS方法,样品经水浸泡,5‰氨水乙腈超声提取,高速冷冻离心,50 mg N-丙基乙二胺(PSA)分散萃取净化材料净化,C18色谱柱色谱分离,液相色谱串联质谱仪分析,建立了一种高效液相色谱串联质谱法测定粮谷中杀螺胺乙醇胺盐残留量的定量分析方法。通过添加100 μL空白基质溶液,在0.2~20.0 μg/L的浓度范围内,杀螺胺的线性良好,方法的检出限为0.3 μg/kg,定量限为1.0 μg/kg,加标1.0 μg/kg、 5.0 μg/kg和10.0 μg/kg的稻谷、小麦、玉米和燕麦的加标回收率为83.5%~122.7%,相对标准偏差均<10%,该方法操作简便、耗时短,检测耗材成本低,结果重复性佳,具有较低的定量限,能够满足粮谷类产品中杀螺胺乙醇胺盐残留的限量要求,为粮谷中杀螺胺乙醇胺盐残留的调研和监测提供了有效的技术支撑。
参考文献
[1]肖汉祥, 张扬, 黄炳超, 等. 70%杀螺胺乙醇胺盐可湿性粉剂防治水稻福寿螺药效试验[J]. 植物医生, 2005, 18(2): 33-34.
[2] GB 2763—2021 食品安全国家标准 食品中农药最大残留限量[S]. 北京: 中国农业出版社, 2021.
[3]刘永涛, 沈丹怡, 等. 改良的QuEChERS与HPLC-HESI/MS/MS同时测定中华鳖组织中氯硝柳胺和酰胺醇类药物及其代谢物的残留量[J]. 分析测试学报, 2017, 36(8): 955-962.
[4]刘伶俐, 万译文, 伍远安, 等. QuEChERS/液相色谱串联质谱法测定水产品中氯硝柳胺[J]. 食品工业科技, 2016, 37(26): 316-318+323.
[5]和佳鸳, 王琳, 等. 土壤中氯硝柳胺残留的超高效液相色谱-串联质谱测定法[J]. 职业与健康, 2021, 37(4): 4.
[6]刘永涛, 沈丹怡, 等. 同位素稀释高效液相色谱-串联质谱法测定水体、底泥、鱼及虾中氯硝柳胺残留量[J]. 分析测试学报, 2020, 39(8): 980-985.
[7] Noor F, Hameed U H, Muhammad B, et al. Deep eutectic solvent based method for analysis of Niclosamide in pharmaceutical and wastewater samples-A green analytical chemistry approach[J]. Journal of Molecular Liquids, 2021, 335: 116142.
[8] GB 31656.7—2021食品安全国家标准 水产品中氯硝柳胺残留量的测定 液相色谱-串联质谱法[S]. 北京:中国农业出版社, 2021.
[9] C. Paghadar, N.H. Vadia. Development and validation of stability indicating RP-HPLC and HPTLC for determination of Niclosamide in bulk and in synthetic mixture[J]. Arabian Journal of Chemistry, 2019, 12, 1803-1814.
[10]伍一红,龚道新,彭筱,等. 高效液相色谱法分析水稻和稻田中的氯硝柳胺乙醇胺盐残留[J]. 色谱, 2011, 29(11): 1098-1102.
[11] 郭雨, 施亚申, 等. 花生和南瓜籽中三乙膦酸铝残留量的测定方法分析[J].中国口岸科学技术, 2023, 11 (5): 63-67.
图2 不同流动相对色谱峰的影响
Fig.2 Effects of different mobile phases on chromatographic peaks
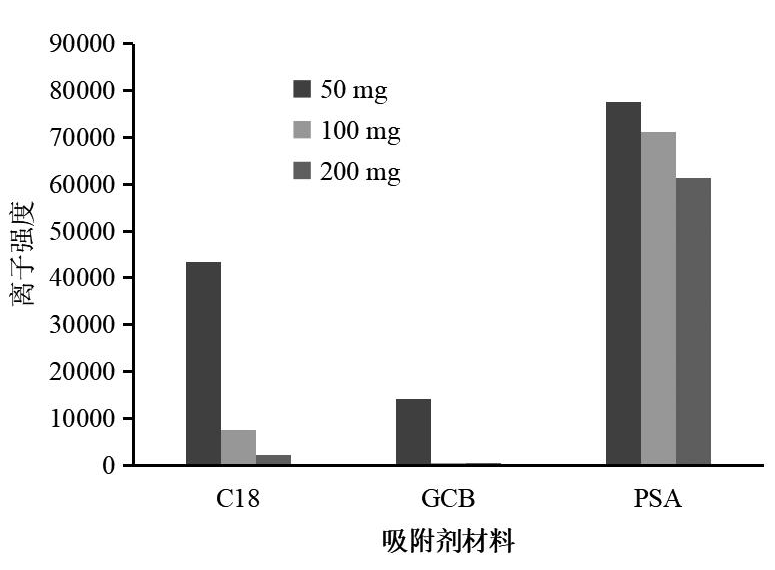 图3 不同吸附材料和使用量对杀螺胺的影响
图3 不同吸附材料和使用量对杀螺胺的影响
Fig.3 Effects of different adsorbent materials and dosages on niclosamide

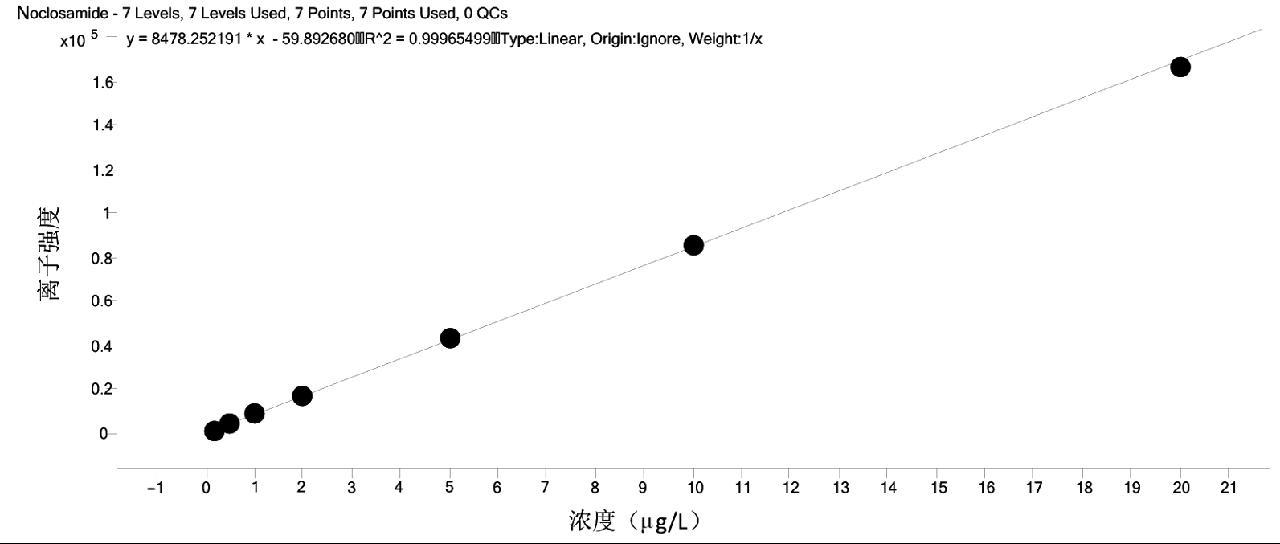
图6 杀螺胺的浓度范围和线性方程
Fig.6 Concentration range and linear equation of niclosamide







