CopyRight 2009-2020 © All Rights Reserved.版权所有: 中国海关未经授权禁止复制或建立镜像
MALDI-TOF MS验证与综合评价
作者:王艺凯 侯颖 杨帆 任宇捷 杨菲 李运涛 邱烨 刘鑫
王艺凯 侯颖 杨帆 任宇捷 杨菲 李运涛 邱烨 刘鑫
摘 要 基质辅助激光解吸电离飞行时间质谱(Matrix-Assisted Laser Desorption/Ionization Time-of-Flight Mass Spectrometry,MALDI-TOF MS)在微生物鉴定方面具有快速高通量分析和高灵敏度等优点,被广泛应用于医疗诊断、生物防御、环境监测和食品质量控制等相关领域。MALDI-TOF MS与PCR技术结合,能够实现高通量的核苷酸位点分析。为了确保其在应用中的可靠性和准确性,建立一套完善的验证与综合评价方案对其进行性能评价至关重要。本文通过参考现有MALDI-TOF MS标准并结合核酸检测的特殊性,建立了该类型设备的验评方案,提出了包含质量测定范围、准确性、分辨率、稳定性等基本性能验证指标和准确性、灵敏度、重复性、抗干扰性等应用性能验证技术指标。依据以上指标,对QuanNUA型MALDI-TOF MS进行验评,验评方案方便易行且无须专业的计量设备,普通的分子生物学实验室就能够对MALDI-TOF MS进行系统和全面验评。该验评方案可为MALDI-TOF MS用于核酸鉴定性能评价提供参考。
关键词 基质辅助激光解吸电离飞行时间质谱;性能评价;核酸检测
Validation and Comprehensive Evaluation
of MALDI-TOF MS
WANG Yi-Kai1 HOU Ying1 YANG Fan2 REN Yu-Jie1
YANG Fei1 LI Yun-Tao3 QIU Ye1 LIU Xin1*
Abstract Matrix-Assisted Laser Desorption/Ionization Time-of-Flight Mass Spectrometry (MALDI-TOF MS) is renowned for its rapid and high-throughput analysis capabilities, as well as high sensitivity in microbial identification, which has led to its widespread application in various fields such as medical diagnostics, biodefense, environmental monitoring, and food quality control. The combination of MALDI-TOF MS and PCR technology can achieve high-throughput nucleotide site analysis. To ensure its reliability and accuracy in these applications, establishing a comprehensive validation and evaluation scheme for performance assessment is crucial. This paper, by referencing existing MALDI-TOF MS standards and considering the particularities of nucleic acid detection, has developed a verification scheme for this type of equipment. It proposes basic performance verification indicators including mass measurement range, accuracy, resolution, and stability, as well as application performance verification technical indicators such as accuracy, sensitivity, repeatability, and interference resistance. Based on these indicators, the QuanNUA type MALDI-TOF MS was evaluated, and the evaluation scheme is convenient and practical without the need for specialized metrological equipment, allowing general laboratories to conduct systematic and comprehensive evaluation of MALDI⁃TOF MS. This validation and evaluation scheme can provide a reference for assessing the performance of MALDI-TOF MS in nucleic acid identification.
Keywords Matrix-Assisted Laser Desorption/Ionization Time-of-Flight Mass Spectrometry (MALDI-TOF MS); performance evaluation; nucleic acid detection
基金项目:海关总署科研项目(2023HK027)
第一作者:王艺凯(1982—),男,汉族,辽宁沈阳人,硕士,高级工程师,主要从事海关仪器研发与验证评价工作,E-mail: wangyikai_2001@163.com
通信作者:刘鑫(1981—),男,汉族,博士,陕西西安人,正高级工程师,主要从事海关仪器研发与验证评价工作,E-mail: liuxin_cn@qq.com
1. 中国海关科学技术研究中心 北京 100026
2. 二连海关技术中心 二连浩特 011100
3. 北京融智优普生物科技有限公司 北京 100026
1. China Customs Science and Technology Research Center, Beijing 100026
2. Erenhot Customs Technology Center, Erenhot 011100
3. Beijing Rongzhi Youpu Biotechnology Co., Ltd., Beijing 100026
基质辅助激光解吸电离飞行时间质谱(Matrix-Assisted Laser Desorption/Ionization Time-of-Flight Mass Spectrometry,MALDI-TOF MS)利用激光脉冲照射样品与基质的共结晶体,使样品分子与基质解吸并电离。在电场加速下,电离后的样品分子通过真空飞行管并按其质量/电荷比(m/z)的不同以不同速度飞行至检测器。检测器记录离子飞行时间并生成能够反映样品中微生物的特定分子指纹的质谱图,将其与数据库中已知微生物图谱进行比对,能够快速、准确地鉴定微生物的种或属[1]。这项技术在微生物鉴定中具有快速、准确、经济高效等特点[1-2],常被用于分析核糖体蛋白[3-4]。
1 MALDI-TOF MS 技术简介
近年来,MALDI-TOF MS与PCR技术结合发展而来的核酸质谱技术,能够实现常规PCR无法达到的通量[5-6]。其实验操作步骤为:先进行多重PCR,再进行单碱基延伸,最后使用设备完成检测并进行数据分析。相比传统的实时荧光定量聚合酶链式反应(Quantitative Real-time PCR)等分子诊断手段,这一技术拥有多重、准确、高通量的优势,这是由MALDI-TOF MS的检测原理和技术路线所决定的。首先,MALDI-TOF MS直接依据分子量的差异来进行检测,只要待测靶标扩增后的分子量不同,就可以相互区别开来[7-10],不会如传统qPCR一样受到荧光通道数的限制。因此,利用MALDI-TOF MS通常能够实现30~50重乃至更多靶标的分析,而传统的qPCR方法单次检测通常小于5重。其次,由于采用了两步扩增反应,再加上对质量直接进行检测,因此MALDI-TOF MS具有极强的准确性和特异性,抗干扰能力强,适合复杂背景下的低丰度[11-13]靶标分析。最后,MALDI-TOF MS检测速度极快,每个样本在质谱检测环节仅需数秒的时间,适合大批量的样本的分析[14]。
2 评价关键指标
MALDI-TOF MS应用操作流程相对复杂,专业要求高,作为一台专用设备,若其设计合理性、操作易用性、兼容性不足,可能会造成假阴性或假阳性结果的出现,对微生物检测产生一定影响。鉴于此,参考国家相关标准[15],结合实际应用与相关研究,本文旨在建立一套完整的评价方法,对MALDI-TOF MS的基本性能和应用功能进行综合测评,为该类设备的性能评价提供参考,进而系统全面地评价MALDI-TOF MS性能及应用特征。
为全面考核MALDI-TOF MS的基本性能,参考行业标准、专家共识、仪器生产企业要求,在基本性能验证中分别就质量检测范围、质量准确性、质量分辨率、质量重复性、质量稳定性、灵敏度等指标进行考核,其中质量检测范围设定为质荷比(m/z):1174.9~10459.0,满足大多数MALDI-TOF MS检测的应用检测需求。此外,在应用性能评价中,利用呼吸道病毒联检试剂盒(HRV/HMPV-B/HBoV1/RNaseP/ORF1ab/PIV1)作为验证材料分别对空白实验、检测下限、抗干扰性、准确性、重复性、批间稳定性等进行测定。
3 评价方案
3.1 基本性能评价要求
本次对MALDI-TOF MS基本性能验证评价的参数主要参考了医药行业标准YY/T 1740.2—2021《基质辅助激光解吸电离飞行时间质谱仪》中的参数内容,性能评价指标的具体要求结合了YY/T 1740.2—2021中对核酸检测质谱仪的指标要求,以及融智生物 QuanNUA 飞行时间质谱仪器的具体技术指标综合制定。具体技术指标如下:
(1)质量范围:可测定的最低到最高质荷比(m/z)范围1500~10000;(2)质量准确性:质荷比最大允许误差≤ 5×10-4;(3)质量分辨率:在最高质荷比(m/z)1500~10000内,质量分辨率≥700 FWHM;(4)信噪比:检测绝对量≤50 fmol的合成标准品,信噪比≥10;(5)质量重复性:质荷比的变异系数≤0.02%;(6)质量稳定性:8小时内质荷比的相对偏差不超过±3×10-4;(7)核酸检测准确度:采用载脂蛋白E(Apolipoprotein E,APOE)MALDI-TOF MS检测试剂盒及阴性、阳性参考品进行重复检测,对阴性、阳性参考品各重复检测10次,阴性参考品检测结果均应为阴性,阳性参考品检测结果均应为阳性。
3.2 应用性能验证评价
应用性能验证评价,依据呼吸道病毒联检成品试剂盒(HRV/HMPVB/HBoV1/RNaseP/ORF1ab/PIV1)作为应用案例分别对应用性能指标进行测定评价。
3.2.1 空白对照
取无酶水进行空白验证试验,空白对照目标位点无有效延伸峰(无识别峰)。
3.2.2 准确性
采用呼吸道病毒联检成品试剂盒阳性参考品进行准确性检测,每次测定3次,同时和目标序列(合成)进行对比,重复测试及测序对比结果一致率 100%。
3.2.3 检测下限
采用呼吸道病毒联检成品试剂盒阳性参考品进行重复检测,对参考品进行梯度稀释,使核酸模板浓度为7 fg/μL进行检测,验证仪器检测下限是否能达到7 fg/μL。
3.2.4 抗干扰能力
阳性对照样本中分别加入不同梯度潜在干扰物质(血红素10 μg/mL、20 μg/mL、甘油三酯500 ng/mL、1000 ng/mL和胆红素1 ng/mL、2 ng/mL),以无酶水作为对照进行检测,样本检测结果不受干扰物质加入的影响,检测结果与阳性对照组测定结果一致。
3.2.5 精密度试验
(1)日内重复性。利用呼吸道病毒联检成品试剂盒对企业阳性参考品进行10 次重复检测,试剂盒日内检测结果一致率100%。
(2)日间重复性。2个工作日内,分别利用呼吸道病毒联检成品试剂盒对企业阳性参考品进行10 次重复检测,试剂盒日间检测结果一致率100%。
(3)批间重复性。连续生产的3批呼吸道病毒联检成品试剂盒,对 3 份企业阳性参考品行 10 次重复检测,试剂盒批间检测结果一致率100%。
4 验评结果
4.1 基本性能参数
4.1.1 质量范围
利用验证标品进行检测,分析信噪比,在1174.9~10459.0范围点上,信噪比分别为179.64和92.79,满足核酸检测范围指定指标要求,结果见表1。
表1 质量范围
Table 1 Quality range
测试项目 | 质核比 | 信噪比 |
最小质荷比 | 1174.9 | 169.64 |
最大质荷比 | 9508.2 | 92.79 |
最大值外延10% | 10459 | |
质量范围 | 1174.9~10459.0 | |
4.1.2 质量准确性
使用序列ACCATG(m/z:1777.3)、序列CCATCTGAGCCAATTCCTGTT(m/z:6333.2)、序列TATAAGCACAAAGCACAGA GCGTTCCACGGC(m/z:9508.2) 的核酸标品进行检测,3条核酸标品最大允许误差分别为0.9×10-4、1.6×10-4、0.7×10-4,均满足缺≤5×10-4(仪器质核比通用技术要求),结果见表2。
4.1.3 质量分辨率
利用与4.1.2相同的核酸标准品测定MALDI-TOF MS分辨率,平均分辨率分别为980、1067、801,满足分辨率≥700要求,结果见表3。
4.1.4 信噪比
利用与4.1.2相同的标准物质绝对量50 fmol进行验证,3个核酸标品的信噪比分别为48.24、72.46、50.32,满足信噪比≥10要求,结果见表4。
4.1.5 质量重复性
利用与4.1.2相同的核酸标准品测定质量重复性,3组核酸标品的CV值分别为0.01%,0.00%、0.01%,满足质荷比的变异系数≤0.02%要求,结果见表5。
4.1.6 质量稳定性
利用与4.1.2相同的核酸标准品测定质量稳定性,3组核酸标品的偏差分别为-0.01%、0.00%、0.01%,结果见表6。
表6 质量稳定性
Table 6 Quality stability
时间 (h) | 质核比 | 偏差 | ||||
0 | 1777.0 | 6332.9 | 9508.7 | 0.00% | 0.00% | 0.00% |
1 | 1777.0 | 6333.0 | 9508.7 | 0.00% | 0.00% | 0.00% |
2 | 1777.2 | 6333.0 | 9508.4 | 0.01% | 0.00% | 0.00% |
3 | 1777.0 | 6333.0 | 9508.6 | 0.00% | 0.00% | 0.00% |
4 | 1777.1 | 6333.2 | 9508.4 | 0.00% | 0.00% | 0.00% |
5 | 1776.9 | 6332.7 | 9509.0 | -0.01% | 0.00% | 0.00% |
6 | 1776.9 | 6333.3 | 9508.1 | -0.01% | 0.01% | -0.01% |
7 | 1776.8 | 6333.0 | 9509.0 | -0.01% | 0.00% | 0.00% |
8 | 1776.8 | 6332.7 | 9509.2 | -0.01% | 0.00% | 0.01% |
4.1.7 核酸检测准确度
利用APOE核酸分型试剂盒验证检测准确性,阴性、阳性参考品均与预期位点一致,满足准确性符合率100%要求,结果见表7。
表7 核酸检测准确度
Table 7 Nucleic acid detection accuracy
样本 | SNP位点 | 位点碱基 | 测定结果 |
1 | rs429358 | T | T |
C | C | ||
2 | rs7412 | T | T |
C | C | ||
3 | 对照 | - | 无延伸峰 |
5 应用性能参数
5.1 空白对照
无酶水进行空白试验,各测试位点无延伸峰,满足空白无识别要求,结果见表8和图1。
5.2 准确性
利用呼吸道病毒联检成品试剂盒阳性参考品进行准确性检测并与目标序列(合成)进行对比,结果6位点与目标位点结果均符合,满足准确性要求,结果如图2所示。
5.3 检测下限
以终浓度为7 fg/μL的阳性参考品对MALDI-TOF MS的检测下限进行测定,与目标序列进行比对,结果显示7 fg/μL条件下能够对6个目标位点完成成功检测,满足7 fg/μL检测下限的要求,结果如图3所示。
5.4 抗干扰能力
以无酶水作为对照分别检测加入不同潜在干扰物质(血红素10 μg/mL、20 μg/mL、甘油三酯500 ng/mL、1000 ng/mL和胆红素1 ng/mL、2 ng/mL)的阳性参考品,评估MALDI-TOF MS抗干扰性,结果显示20 μg/mL血红素、1000 ng/mL甘油三酯及2 ng/mL胆红素等条件下对检测结果无影响,结果如图4所示。
5.5 精密度试验
5.5.1 日内重复性
利用呼吸道病毒联检成品试剂盒对阳性参考品进行日内重复检测,10次测定结果完全一致,符合日内重复性要求,结果如图5所示。
5.5.2 日间重复性
利用呼吸道病毒联检成品试剂盒对阳性参考品进行连续两天的重复检测,日间测定中连续两天10次测定结果与目标序列相符,且日间结果完全一致,满足日间重复性要求,结果如图6所示。
5.5.3 批间重复性
利用3个批次的呼吸道病毒联检成品试剂盒对批次内企业阳性参考品进行重复检测,比对批内及批间测定一致率。结果显示,3个批次测定结果一致且与目标位点相符,满足批间重复性要求,结果如图7 所示。
6 结论
本文使用核酸标品对QuanNUA型MALDI-TOF MS基本性能和应用性能中关键指标进行验证与综合评价,结果显示该设备对核酸标品的最高质荷比(m/z)验证范围为1174.9~10459.0,满足应用检测需求;其质量准确性、质量分辨率、质量重复性、质量稳定性、灵敏度等指标也均符合YY/T 1740.2—2021基质辅助激光解吸电离飞行时间质谱仪标准的要求。利用呼吸道病毒联检试剂盒对该设备应用功能进行测试,结果显示该设备对阳性模板的检测灵敏度可达到7 fg/μL,仪器的验证准确度为100%,检测结果与模板测序结果一致;各重复验证结果一致,日内、日间测定均成功检出,且测定一致;批次间稳定性较高;干扰性试验结果显示在规定浓度条件下血红素、甘油三酯、胆红素等干扰物质的加入对阳性样本检测无明显干扰。
本次验证报告客观地反映了QuanNUA飞行时间质谱的性能,相关材料准确记录了验评结果。QuanNUA飞行时间质谱在精密度、准确性、重复性、检出限等指标上满足病原微生物检测的要求,设备稳定性较高,可避免由血红素、甘油三酯、胆红素等干扰物质对样本中相关病原检测带来的干扰。因此,本文推测MALDI-TOF MS技术适用于海关口岸复杂样本中特定病原的检测,其可进行多靶标同时分析的能力,可实现“采集一份样本,检测多种病原”,提升海关实验室病原检测效率和准确率,有助于提高口岸“多病同防”检测能力。
参考文献
[1] Croxatto, A., G. Prod’hom, G. Greub. Applications of MALDI-TOF mass spectrometry in clinical diagnostic microbiology[J]. FEMS Microbiology Reviews, 2012, 36(2): 380-407.
[2] Ashfaq, M.Y., D.A. Da’na, and M.A. Al-Ghouti, Application of MALDI-TOF MS for identification of environmental bacteria: A review[J]. Journal of Environmental Management, 2022, 305: 114359.
[3] Torres-Sangiao, E., C. Leal Rodriguez, and C. Garcia-Riestra, Application and Perspectives of MALDI-TOF Mass Spectrometry in Clinical Microbiology Laboratories[J]. Microorganisms, 2021, 9(7): 1539.
[4] De Carolis. Application of MALDI-TOF mass spectrometry in clinical diagnostic microbiology[J]. Journal of Infection in Developing Countries, 2014, 8(9): 1081-1088.
[5] 中国核酸质谱应用专家共识协作组. 中国核酸质谱应用专家共识 [J] . 中华医学杂志, 2018, 98 (12): 895-900.
[6] Shuai. MALDI-TOF nucleic acid mass spectrometry for simultaneously detection of fourteen porcine viruses and its application[J]. Journal of Virological Methods, 2024. 329: 114990.
[7]刘宇, 张忠兵, 徐晓枫, 等. 基于MALDI-TOF MS技术快速鉴定奶牛乳腺炎奶样中疑似金黄色葡萄球菌[J]. 中国兽医学报, 2023, 43(9): 1941-1947.
[8] 孙伟, 许杰, 张薇, 等. 基于核糖体蛋白质标志物及MALDI-TOF MS技术快速鉴定糖丝菌属放线菌[J]. 微生物学报, 2023: 15(12): 4800-4813.
[9] 崔洁, 林吉恒, 孙瑛, 等. MALDI-TOF MS法快速鉴定散装即食食品中3种食源性致病菌[J]. 食品工业科技, 2024, 45(5): 253-270.
[10] 袁媛, 王欢, 修宁宁, 等. MALDI-TOF MS快速鉴定腹泻病原菌的评价[J]. 标记免疫分析与临床, 2023, 30(2): 338-342.
[11] 吴福平, 朱宏锴, 陈莹, 等. 应用MALDI-TOF-MS快速鉴定从鸡胴体中分离的一株空肠弯曲菌 [J]. 工业微生物, 2022, 52(2): 38-41.
[12] 韩伟, 庄绪会, 邹海杰, 等. MALDI-TOF MS技术在粮油与食品微生物快速鉴定领域的应用展望 [J]. 中国粮油学报, 2021, 36(8): 177-183.
[13] 谢海平, 喻佳俊, 黄清, 等. 基于MALDI-TOF MS技术对加州鲈病原弗氏柠檬酸杆菌的快速鉴定[J]. 淡水渔业, 2020, 50(6): 40-45.
[14]姜彦芬, 王金凤, 李睿文, 等. MALDI-TOF MS方法快速鉴定临床分离的肺炎克雷伯氏菌[J]. 中国动物检疫, 2020, 37(8): 101-105.
[15] YY/T1740.2—2021医用质谱仪 第2部分:基质辅助激光解吸电离MALDI TOF MS仪[S]. 北京: 中国标准出版社, 2021.
表2 质量准确性
Table 2 Quality accuracy
标准物质质核比 | 质核比 | 误差绝对值 | 误差平均值 | |||||
测试1 | 测试2 | 测试3 | 测试1 | 测试2 | 测试3 | |||
1777.30 | 1777.4 | 1777.3 | 1776.9 | 0.00005 | 0.00000 | 0.00023 | 0.00009 | |
6333.20 | 6332.4 | 6334.4 | 6334.3 | 0.00012 | 0.00020 | 0.00017 | 0.00016 | |
9508.20 | 9507.8 | 9508.8 | 9507.2 | 0.00004 | 0.00006 | 0.00010 | 0.00007 | |
表3 质量分辨率
Table 3 Quality resolution
测试号 | 质核比 | 半峰宽 | 分辨率 | |||||||
测试1 | 1777.3 | 6333.2 | 9507.6 | 2.14 | 5.94 | 13.09 | 829 | 1067 | 727 | |
测试2 | 1777.3 | 6334.0 | 9508.2 | 1.81 | 6.56 | 13.37 | 980 | 965 | 711 | |
测试3 | 1777.7 | 6333.8 | 9509.3 | 2.64 | 8.12 | 11.87 | 673 | 780 | 801 | |
质量分辨率 | - | - | - | - | - | - | 980 | 1067 | 801 | |
表4 信噪比
Table 4 Signal-to-noise ratio
质核比 | 信噪比 | |||
测试1 | 测试2 | 测试3 | 平均值 | |
1777.3 | 33.40 | 53.80 | 57.53 | 48.24 |
6333.2 | 50.40 | 87.78 | 79.20 | 72.46 |
9508.2 | 55.57 | 42.80 | 52.60 | 50.32 |
表5 质量重复性
Table 5 Quality repeatability
标准物质 | 测试1 | 测试2 | 测试3 | 测试4 | 测试5 | 测试6 | 测试7 | 测试8 | 测试9 | 测试10 | 平均值 | (SD) | (CV) |
1777.3 | 1777.1 | 1777.6 | 1777.0 | 1777.0 | 1777.0 | 1777.3 | 1777.1 | 1776.9 | 1777.3 | 1777.1 | 1777.2 | 0.2 | 0.01% |
6333.2 | 6333.4 | 6333.3 | 6333.0 | 6333.6 | 6333.6 | 6333.5 | 6333.7 | 6333.0 | 6333.3 | 6333.1 | 6333.34 | 0.26 | 0.00% |
9508.2 | 9508.9 | 9508.6 | 9508.2 | 9508.7 | 9509.1 | 9509.0 | 9508.8 | 9508.2 | 9509.1 | 9507.5 | 9508.61 | 0.52 | 0.01% |
表8 空白试验中核酸检测准确度
Table 8 Nucleic acid detection accuracy in blank test
测定 | 测试位点 | 测定结果 | 结论 | ||
1 | 2 | 3 | |||
无酶水 | HRV | 无延伸峰 | 无延伸峰 | 无延伸峰 | 空白无延伸 |
HMPV_B | 无延伸峰 | 无延伸峰 | 无延伸峰 | ||
HBoV1 | 无延伸峰 | 无延伸峰 | 无延伸峰 | ||
RNase P | 无延伸峰 | 无延伸峰 | 无延伸峰 | ||
SARS-CoV-2-ORF1ab | 无延伸峰 | 无延伸峰 | 无延伸峰 | ||
PIV1 | 无延伸峰 | 无延伸峰 | 无延伸峰 | ||
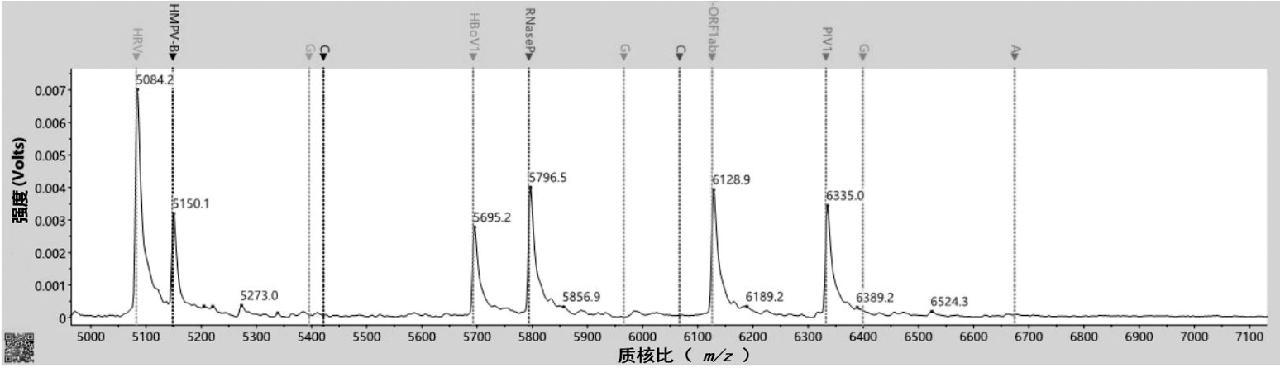
图1 空白实验
Fig.1 Blank experiments
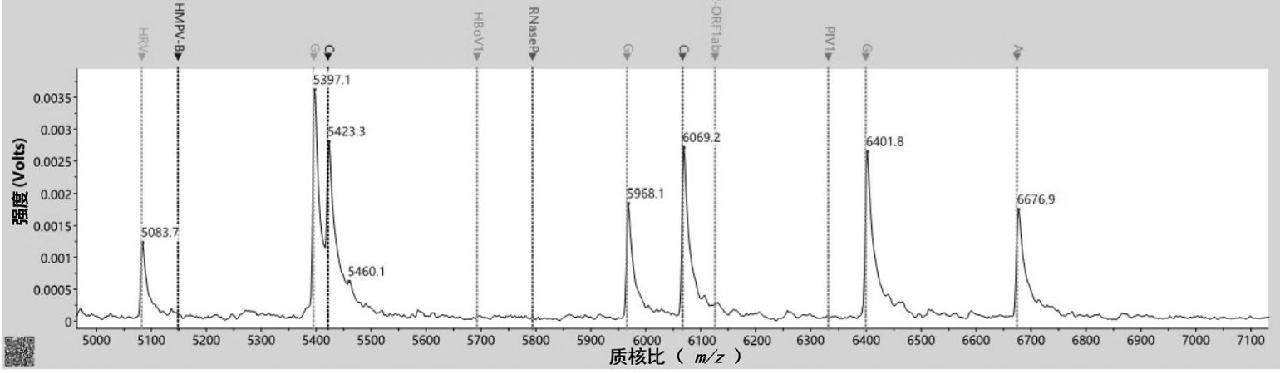
图2 准确性验证
Fig.2 Accuracy verification
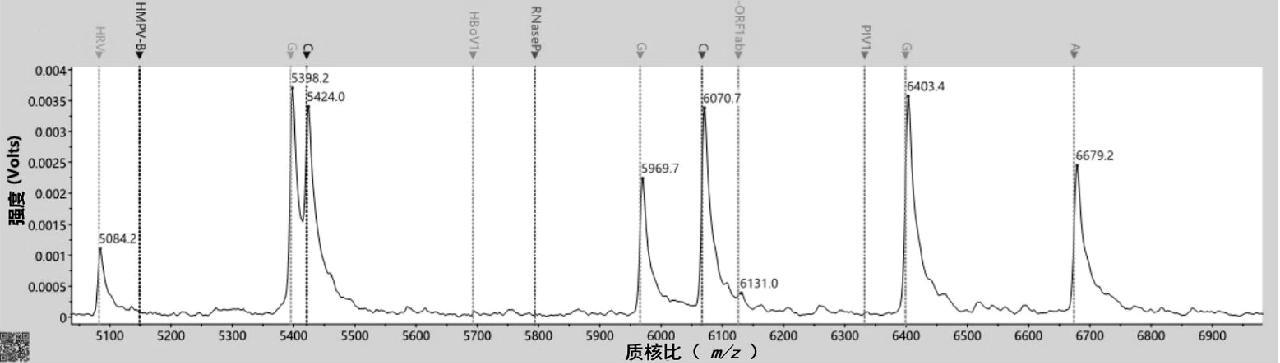
图3 检测下限
Fig.3 Lower detection limit

A: CK对照; B: 血红素 (20 μg/mL) ; C: 甘油三酯 (1000 ng/mL); D: 胆红素 (2 ng/mL)
图4 抗干扰性检测
Fig.4 Anti-interference detection

图5 日内重复性
Fig.5 Intra-day repeatability
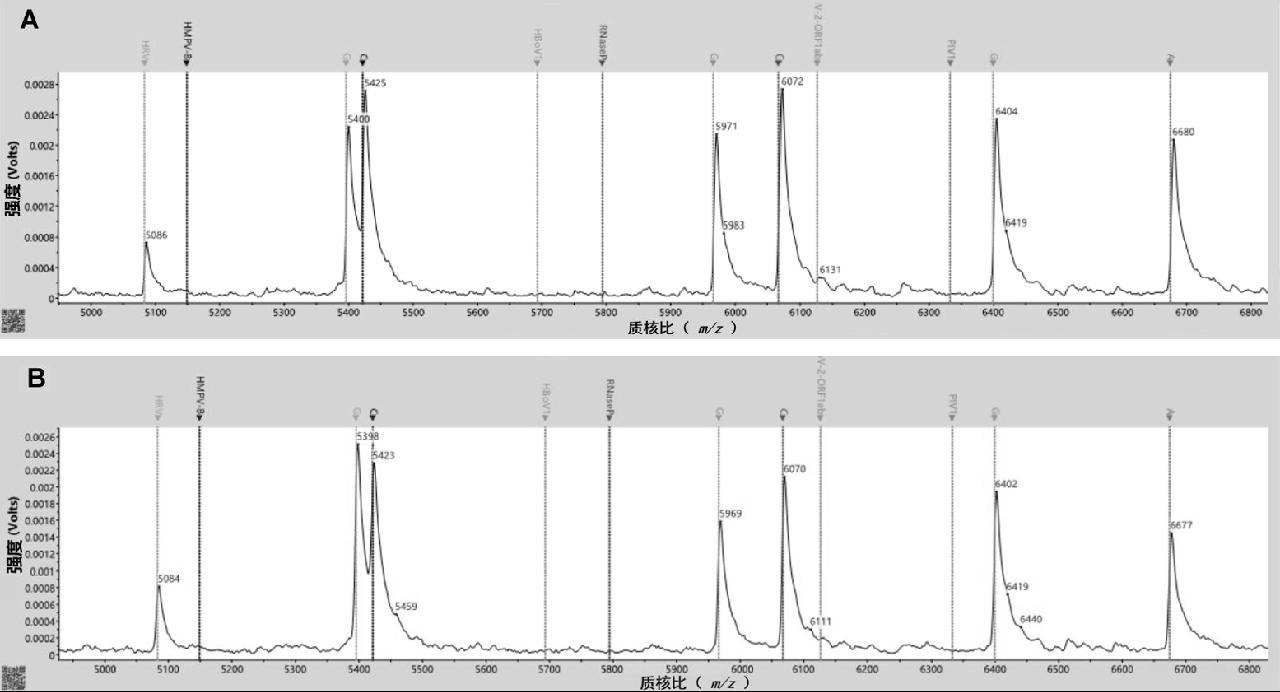
A: Day1; B: D: Day2
图6 日间重复性
Fig.6 Inter-day repeatability
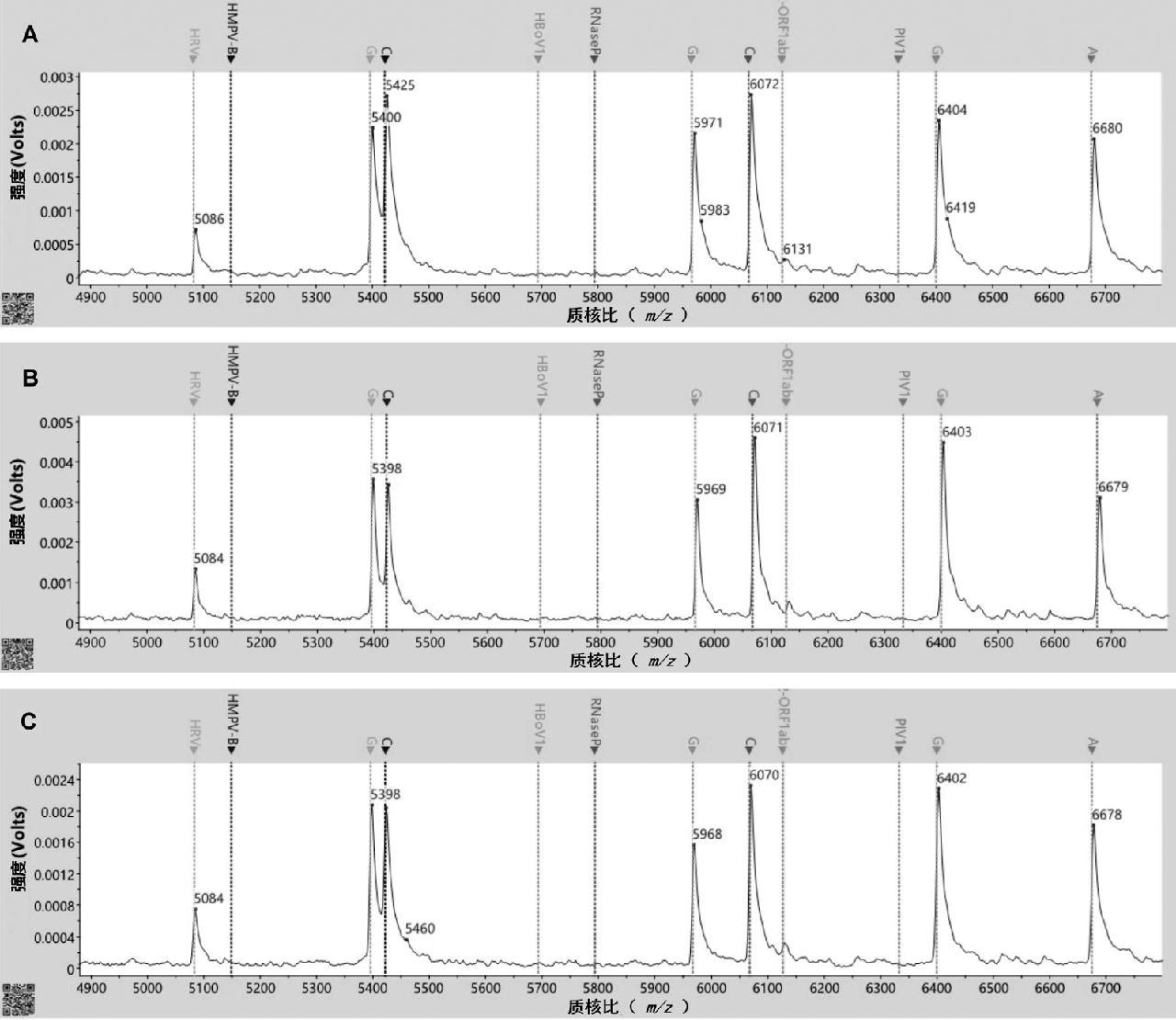
A: KIT1; B: KIT2; C: KIT
图7 批间重复性
Fig.7 Batch-to-batch repeatability







