CopyRight 2009-2020 © All Rights Reserved.版权所有: 中国海关未经授权禁止复制或建立镜像
全自动核酸提取及检测分析系统性能验证及评价
作者:王婕敏 杨铭 艾晓娟 郝玉通 文海燕 孙菲
王婕敏 杨铭 艾晓娟 郝玉通 文海燕 孙菲
王婕敏 1 杨 铭 1 艾晓娟 1 郝玉通 2 文海燕 2 孙 菲 1 *
摘 要 本文评估了移动P2+实验室中配置的全自动核酸提取及检测分析系统对咽拭子、血清和肛拭子3种类型临床样本核酸的提取效果。采用荧光定量PCR法,使用猴痘病毒核酸检测试剂盒、登革热病毒核酸检测试剂盒和诺如病毒检测试剂盒,对临床采集的血清样本、咽拭子样本、肛拭子样本3种类型各5例进行核酸提取、扩增及平行检测,并对内参循环阈值(Ct值)进行统计学分析。同时,选择35个临床咽拭子样本,采用不同的提取扩增系统进行核酸提取与扩增,比较内参扩增结果情况。结果显示,不同的样本类型重复检测的变异系数(CV值)均在5%以内,重复性较高,核酸Ct值结果一致性较好,每种类型样本提取效率均稳定。35个临床咽拭子分别使用全自动核酸提取及检测分析系统与常规实验室核酸提取检测分析系统进行交叉验证,两者检出率相同,结果一致。综上,移动P2+实验室中配置的全自动核酸提取及检测分析系统可用于提取咽拭子、血清和肛拭子样本核酸。
关键词 移动P2+实验室;核酸提取系统;核酸检测;性能验证
Performance Verification and Evaluation of Automated Nucleic Acid Extraction and Detection Analysis Systems
WANG Jie-Min 1 YANG Ming 1 AI Xiao-Juan 1 HAO Yu-Tong 2 WEN Hai-Yan 2 SUN Fei 1*
Abstract This study evaluated the efficiency of a nucleic acid extraction and detection system deployed in a mobile P2+ laboratory for the processing three types of clinical samples: throat swabs, serum, and rectal swabs. Using fluorescent quantitative PCR (FQPCR) assays with nucleic acid detection kits specific for monkeypox virus, dengue virus, and norovirus, we performed nucleic acid extraction, amplification, and parallel testing on 15 clinical samples (5 serum samples, 5 throat swab samples, and 5 anal swab samples). The cycle threshold (Ct) values of internal controls were statistically analyzed to evaluate the intra-assay reproducibility.A total of 35 clinical throat swab samples were selected and subjected to nucleic acid extraction and amplification using various extraction-amplification systems. The performance of internal reference amplification was evaluated and compared.The results demonstrated that the coefficient of variation (CV) values for repeated testing across the different sample types were all within 5%, indicating high reproducibility. Additionally, the Ct values showed good consistency, and the nucleic acid extraction efficiency was stable for each sample type. Furthermore, cross-validation was performed by testing the same 35 clinical throat swab samples using both an automated nucleic acid extraction and detection system and a conventional laboratory-based nucleic acid extraction and detection system. The detection rates were identical between the two systems.
Keywords mobile P2+ laboratory; nucleic acid extraction system; nucleic acid detection; performance validation
基金项目:海关总署科研项目(2024HK167);重庆市2022年度技术创新与应用发展专项面上项目(CSTB2022TIAD-GPX0073)
第一作者:王婕敏(1991—),女,汉族,湖南,硕士,兽医师,主要从事传染病检测究工作,E-mail: 271572051@qq.com
通信作者:孙菲(1969—),女,汉族,湖南,本科,主任技师,主要从事传染病检测和分子生物学研究工作,E-mail: sunfei0107@163.com
1. 湖南国际旅行卫生保健中心(长沙海关口岸门诊部) 长沙 410000
2. 重庆国际旅行卫生保健中心(重庆海关口岸门诊部) 重庆 401147
1. Hunan International Travel Healthcare Center (Changsha Customs Port Outpatient), Changsha 410000
2. Chongqing International Travel Healthcare Center (Chongqing Customs Port Outpatient), Chongqing 401147
核酸检测技术已成为口岸传染病诊断和防控的关键工具[1-2],尤其是在传染病的快速识别和处理中发挥着重要作用。相较于病毒分离培养的操作繁琐、环境和生物安全要求高,以及血清抗体检测的滞后性,在境外各种传染病不断出现的情况下,荧光定量PCR(Real-Time Fluorescent Quantitative PCR,qPCR)技术作为口岸重要检测技术手段,具有特异性高、灵敏度高、诊断迅速的特点,而移动P2+实验室为荧光定量PCR检测工作提供了生物安全环境条件,工作便利性作用凸显。核酸提取作为荧光定量PCR诊断的首要步骤,其效率和准确性直接影响后续实验的成败,本研究旨在通过移动P2+实验室配置的全自动核酸提取及检测分析系统对咽拭子、血清和肛拭子3种不同类型的样本进行核酸提取,比较分析该系统在移动P2+实验室环境条件下,对咽拭子、血清和肛拭子作为病原体常见的样本类型的核酸提取效率和可行性。
依据试剂中内参基因的扩增效果和稳定性,本研究对不同样本类型的扩增情况进行评估。内参基因作为核酸检测中的关键参照物,其稳定性直接影响到实验结果的可靠性[3-4]。选择表达稳定、特异性强的内参基因,可以更准确地评估目标基因的表达水平,采用人源性内参基因的扩增试剂,不仅可有效监控每个样本的采集质量,还能间接反映扩增效率[5-8]。
本研究通过验证在移动P2+实验室环境条件下,全自动核酸提取及检测分析系统在不同样本类型中的适用性和效率,并通过内参基因的分析,优化检测流程,为口岸传染病核酸检测提供更加稳定和准确的实验数据,以提高口岸传染病防控的时效性和准确性,在口岸公共卫生事件中快速预警具有实际应用意义。
1 材料与方法
1.1 材料与试剂
采集咽拭子、肛拭子、血液样本各5份,其中,促凝剂真空采血血管收集血液样本,离心后取上层血清。采购猴痘病毒核酸检测试剂盒(荧光PCR法),包括PCR反应液、猴痘病毒检测液、阳性对照、去RNA酶水(空白对照);诺如病毒GI病毒核酸检测试剂盒(荧光PCR法),包括RT-PCR反应混合液、酶混合液、诺如病毒GI检测液、阳性对照、去RNA酶水(空白对照);登革病毒通用型核酸检测试剂盒(PCR-荧光探针法),包括RT-PCR反应液、酶混合液、登革病毒通用型检测液、阳性对照、去RNA酶水(空白对照)。
1.2 仪器与设备
上海之江AutraMic mini4800型全自动核酸提取及检测分析系统(上海之江生物医药科技有限公司)及其配套纯化试剂包括预分装试剂;常规核酸提取及检测分析系统包括全自动核酸提取仪(硕世SMPE-960型)及其配套纯化试剂包括预分装试剂;荧光定量PCR仪(Quantstudio 7 flex)。
1.3 实验方法
1.3.1 核酸提取与扩增
使用全自动核酸提取及检测分析系统,并根据该仪器说明书要求进行核酸提取,根据猴痘病毒核酸检测试剂盒(荧光PCR法)、诺如病毒GI病毒核酸检测试剂盒(荧光PCR法)和登革病毒通用型核酸检测试剂盒(PCR-荧光探针法)试剂说明书配制反应体系,按照试剂说明书要求的扩增条件对5个咽拭子样本、5个血清样本和5个肛拭子(编号分别为Y1—Y5、X1—X5、G1—G5)样本进行检测,每份测定8个重复,共进行120项次的测定,记录结果及相应核酸循环阈(Cycle Threshold,Ct)值,以VIC通道检测的人源性内参基因的Ct值来反映其扩增效率。临床咽拭子35个,使用不同的核酸提取和扩增系统进行检测,记录结果及相应Ct值。
1.3.2 观察与评价指标扩增效率
以内参基因的Ct值作为指标,Ct值表示qPCR扩增过程中扩增产物的荧光信号达到设定的荧光阈值时所对应的不同样本的扩增循环数。
1.4 统计学方法
采用 Excel 软件建立数据库,对提取的不同类型样本中病毒RNA扩增后内参靶基因的Ct值进行结果比较,计量资料用( ±s)表示,精密度采用变异系数(Coefficient of Variation,CV)表示。
±s)表示,精密度采用变异系数(Coefficient of Variation,CV)表示。
2 结果
对由全自动核酸提取及检测分析系统提取的3种不同类型样本的核酸扩增效率加以比较,肛拭子样本选择5个样本检测8次内参基因Ct值分别为(31.94±0.22)(32.17±0.17)(34.48±0.37)(36.38±0.48)和(32.55±0.80);血液样本选择5个样本检测8次内参基因Ct值分别为(30.80±0.34)(31.22±0.44)(30.50±0.38)(31.68±0.45)和(31.47±0.38);咽拭子样本选择5个样本检测8次内参Ct值分别为(32.81±0.90)(32.64±0.67)(32.75±0.95)(32.55±0.84)和(32.20±0.96)。内参基因Ct值CV越小,内参基因的稳定性越好,即内参基因的提取效果越稳定。不同的样本类型,每个样本8次检测的重复性CV值均在5%以内,重复性较高,核酸Ct值结果一致性较好,每种类型样本均提取效率稳定。具体情况见表1—表3。
对临床35个咽拭子样本分别使用全自动核酸提取及检测分析系统和常规荧光定量PCR方法检测样本中的内参基因,检测结果见表4,检出率均为100%,两者的扩增曲线如图1—图2所示。
表1 核酸提取系统提取的肛拭子样本核酸内参基因
Ct值比较
Table 1 Comparison of Ct Values for Internal Reference Genes in Nucleic Acids Extracted from Anal Swab Samples Using the Automated Nucleic Acid Extraction System
样本 | Ct值 ( | CV (%) |
G1 | 31.94±0.22 | 0.70 |
G2 | 32.17±0.17 | 0.51 |
G3 | 34.48±0.37 | 1.08 |
G4 | 36.38±0.48 | 1.32 |
G5 | 32.55±0.80 | 2.47 |
表2 核酸提取系统提取的血液样本核酸内酯基因Ct值比较
Table 2 Comparison of Ct Values for Internal Reference Genes in Nucleic Acids Extracted from Blood Samples Using the Automated Nucleic Acid Extraction System
样本 | Ct值 ( | CV (%) |
X1 | 30.80±0.34 | 1.12 |
X2 | 31.22±0.44 | 1.42 |
X3 | 30.50±0.38 | 1.25 |
X4 | 31.68±0.45 | 1.42 |
X5 | 31.47±0.38 | 1.20 |
表3 核酸提取系统提取的咽拭子样本核酸内参基因
Ct值比较
Table 3 Comparison of Ct Values for Internal Reference Genes in Nucleic Acids Extracted from Throat Swab Samples Using the Automated Nucleic Acid Extraction System
样本 | Ct值 ( | CV (%) |
Y1 | 32.81±0.90 | 2.75 |
Y2 | 32.64±0.67 | 2.05 |
Y3 | 32.75±0.95 | 2.91 |
Y4 | 32.55±0.84 | 2.58 |
Y5 | 32.20±0.96 | 2.97 |
表4 不同提取系统提取的咽拭子样本核酸内参基因
Ct值比较
Table 4 Comparison of Ct Values for Internal Reference Genes in Nucleic Acids Extracted from Throat Swab Samples Using Different Nucleic Acid Extraction Systems
组别 | 样本数 | Ct值 ( | 检出率 (%) |
全自动核酸提取及检测分析系统 | 35 | 32.92±1.98 | 100 |
常规核酸提取及检测分析系统 | 35 | 31.86±2.20 | 100 |
3 结论
PCR技术在口岸传染病的检测中发挥着关键作用,通过特异性地扩增目标DNA序列,显著提高了病原检测的灵敏度和准确性,有效克服了传统免疫学检测的局限,尤其是在感染初期,能够快速及时地识别病原体,对于迅速筛查和诊断传染病具有重要意义[8-9]。在口岸疫情防控工作中,口岸传染病检测主要涉及咽拭子、血液和肛拭子等多种样本类型,其检测范围覆盖多种传染病,如呼吸道传染病、虫媒传染病和消化道传染病[10-12]。田峰等[8]仅使用新型冠状病毒核酸检测标准品对全自动核酸提取及检测分析系统进行重复性的检测分析,未说明该系统对不同人源性样本类型的检测情况。本研究使用猴痘病毒核酸检测试剂盒、登革热病毒核酸检测试剂盒和诺如病毒检测试剂盒,通过检测在组织和细胞中稳定表达的人源性内参基因的Ct值来反映不同样本类型的扩增效率。结果显示,人源性内参基因扩增结果稳定,表明全自动核酸提取及检测分析系统具有较好的核酸提取能力,且适用于多种临床样本。本研究在对咽拭子、血液和肛拭子3种样本的核酸提取效率进行比较时,发现血液样本的提取效率最高,而肛拭子的提取效率相对较低,可能与非血样本中细胞含量较少有关,但所有样本的核酸提取效率的变异系数均小于5%,显示出系统在不同人源性样本中提取效率的稳定性。同时,对临床35个咽拭子分别使用全自动核酸提取及检测分析系统与常规核酸提取及检测分析系统进行扩增,检出率均为100%,结果一致,表明全自动核酸提取及检测分析系统的核酸提取和扩增的检出方面与常规核酸提取及检测分析系统一致。总体而言,全自动核酸提取及检测分析系统在实验中显示出的性能指标符合使用要求,具备良好的核酸提取能力,扩增效率高,稳定性好,能够满足口岸多种传染病检测的需求,同时该系统为全程自动化设备,方便人员操作,设备体积较小,满足移动P2+实验室空间要求,有利于口岸一线检疫检测能力的提升。
参考文献
[1]叶颖, 李磊, 朱丽, 等. 国境口岸应对重大传染病疫情的措施与思考[J]. 中国公共卫生管理, 2023, 39(6): 774-777.
[2]阿尔蔼·塔拉哈提, 黄凯, 蒋晓玲, 等. PCR技术在口岸传染病检测中的应用[J]. 中国口岸科学技术, 2020(9): 26-30.
[3]何安娜, 张梦怡, 李逢钰, 等. 人乳头瘤病毒6型和11型通用型含内源性内参的重组酶介导的等温扩增技术检测方法的建立[J]. 新发传染病电子杂志, 2022, 7(2): 25-29.
[4]李俊慧, 裴倩倩, 赵晓转, 等. 不同人源性细胞中内参基因的筛选[J]. 中国医学工程, 2024, 32(6): 10-13.
[5]钟福春, 陈甜, 张抒彧, 等. 不同核酸提取程序及扩增仪组合检测呼吸道病毒的差异[J]. 中国卫生标准管理, 2023, 14(15): 128-132.
[6]彭雄俊, 彭一枝, 崔杨飞, 等. 三种核酸快速提取系统的病毒核酸提取效果评价[J]. 中国医学装备, 2022, 19(5): 48-53.
[7]何维芝, 许彬, 蒋立. 不同提取及扩增方法检测新型冠状病毒核酸的性能比较分析[J]. 华南预防医学, 2022, 48(1): 135-138.
[8]田锋, 党晓霞, 夏侯为民, 等. 全自动核酸提纯及实时荧光PCR系统的性能验证与评价[J]. 医学动物防制, 2024, 40(4): 410-413.
[9]綦佩妍, 李雪明, 戴俊, 等. 口岸输入性传染病风险识别的现状及优化[J]. 中国国境卫生检疫杂志, 2023, 46(5): 435-441.
[9]章钰莹, 刘雨婷, 李育平, 等. 我国境外输入性传染病研究热点和前沿的可视化分析[J]. 预防医学情报杂志, 2021, 37(10): 1428-1436+1442.
[10]李深伟, 陈磊琼, 张子龙, 等. 上海口岸一起韩国输入性霍乱病例的应急处置[J]. 中国国境卫生检疫杂志, 2019, 42(6): 393-394+406.
[11]卢玲敏, 黎湘娟. 2017—2022年广西口岸入境人员登革热监测结果分析[J]. 口岸卫生控制, 2024, 29(3): 38-40+54.
[12]曹冉冉, 刘晨霞, 罗灿, 等. 四川省首例猴痘病例病毒基因组特征分析[J]. 疾病监测, 2024, 39(8): 989-994.
1.247
0.860
0.282
图1 全自动核酸提取及检测分析系统扩增曲线
Fig.1 Amplification Curves of the Automated Nucleic Acid Extraction and Detection Analysis System
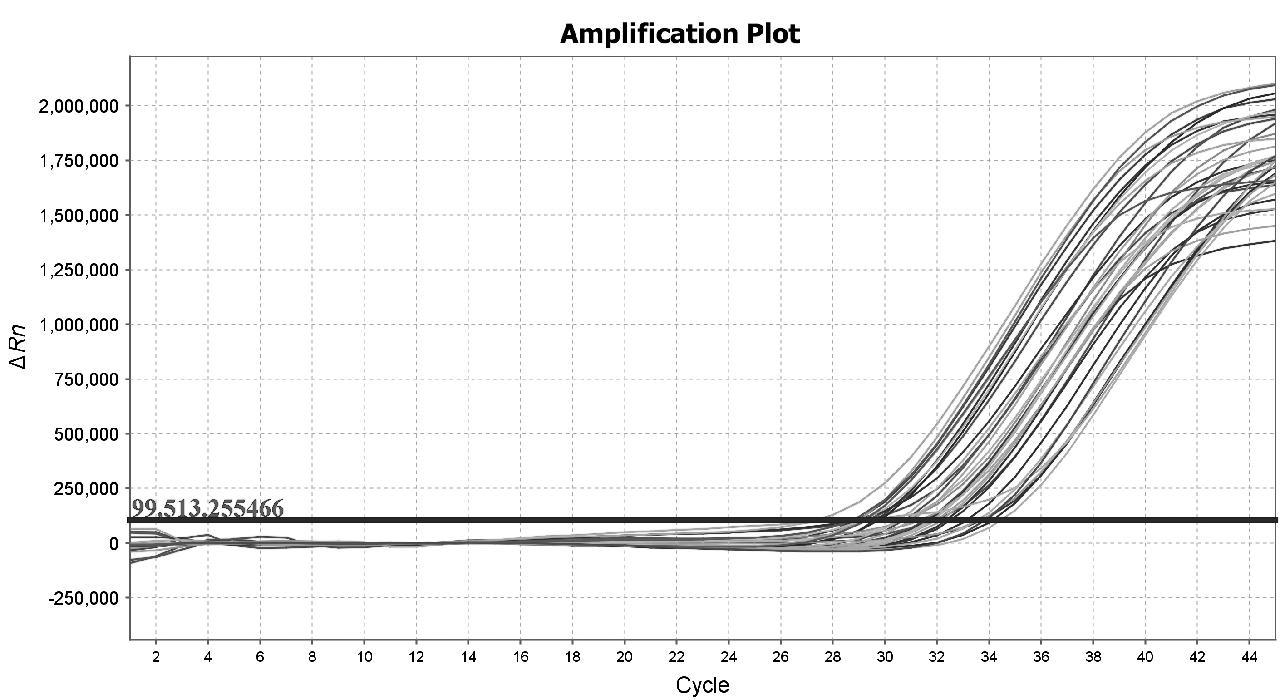
图2 常规核酸提取及检测分析系统扩增曲线
Fig.2 Amplification Curves of the Conventional Nucleic Acid Extraction and Detection Analysis System












