CopyRight 2009-2020 © All Rights Reserved.版权所有: 中国海关未经授权禁止复制或建立镜像
CP Select系统富集羽绒羽毛样品中禽流感病毒效率评估
作者:石文军 刘嘉静 辛学谦 邵迪 孙明君 常凯 徐彪 岳志芹
石文军 刘嘉静 辛学谦 邵迪 孙明君 常凯 徐彪 岳志芹
石文军 1 刘嘉静 2 辛学谦 1 邵 迪 1 孙明君 1 常 凯 1 徐 彪 1 岳志芹 1 *
摘 要 禽流感(Avian Influenza,AI)是由禽流感病毒(Avian Influenza Virus,AIV)引起的一种危害全球畜禽养殖业的重要呼吸道传染病之一。口岸检测是遏制病原跨境传播的第一道防线,进境羽绒羽毛样品中潜在病原及核酸载量低,PCR扩增和基因组测序难度大,不利于疫情信息的及时上报以及口岸一线的病原风险评估。本研究建立了进境羽绒羽毛样品病原富集技术,其中模拟样品PBS洗脱液最高可富集27.5倍,tris洗脱液最高可富集740倍;羽绒羽毛样品tris洗脱液最高可富集52倍。该病原富集技术可以为后续病原分离、核酸扩增及基因组测序研究提供重要支撑。
关键词 CP Select系统;富集;羽绒羽毛;禽流感病毒
Evaluation of the Efficiency of the CP Select System in Enriching Avian Influenza Virus from Down and Feather Samples
SHI Wen-Jun1 LIU Jia-Jing2 XIN Xue-Qian1 SHAO Di1
SUN Ming-Jun1 CHANG Kai1 XU Biao1 YUE Zhi-Qin1*
Abstract Avian influenza (AI), caused by the avian influenza virus (AIV), is a major respiratory infectious disease threatening global poultry farming industries, whose public health security and epidemic transmission risk warrant attention. Port-of-entry positive detection serves as the first line of defense against the cross-border spread of pathogens. However, imported down and feather samples typically contain low levels of potential pathogens and nucleic acid, making PCR amplification and genome sequencing challenging. This hinders timely epidemic information reporting and frontline pathogen risk assessment at the port. This study established an effective trace pathogen enrichment technique for imported down and feather samples. For simulated samples, the technique achieved up to 27.5-fold enrichment with PBS elution solution and up to 740-fold enrichment with Tris elution solution. For actual down and feather samples, the highest enrichment was 52-fold with tris elution solution. This pathogen enrichment technique provides crucial support for subsequent pathogen isolation, nucleic acid amplification, and genome sequencing studies.
Keywords CP select system; enrichment; down and feather; avian influenza virus
基金项目:海关总署科研项目(2024HK027;2023HK039);青岛海关科研项目(QK202503)
第一作者:石文军(1990—),男,汉族,博士,兽医师,主要从事进出境动物疫病检疫研究工作,E-mail: duoyanji@126.com
通信作者:岳志芹(1975—),女,汉族,博士,研究员,主要从事进出境动物疫病检疫研究工作,E-mail: yuezhiqin@126.com
1. 青岛海关技术中心 青岛 266000
2. 青岛农业大学 青岛 266109
1. Technology Center of Qindao Customs, Qingdao 266000
2. Qingdao Agricultural University, Qingdao 266109
禽流感病毒(Avian Influenza Virus,AIV)是一种单股负链RNA病毒,由8个节段组成。根据其血凝素(Hemagglutinin,HA)和神经氨酸酶(Neuraminidase,NA)的抗原性差异,分为18种HA亚型和11种NA亚型[1-3]。水禽是AIV的天然宿主[3]。高致病性AIV感染通常引起全身症状,而低致病性AIV感染一般局限于呼吸道和消化道[4]。近年来,AIV在全球范围内广泛传播,某些亚型如H5、H7、H9和H10发生重组或变异,并可导致人畜共患病,其中H5和H7型AIV通常会导致严重后果[5]。AIV的鉴定检测方法主要分为病原分离鉴定、分子生物学检测方法、血清学检测方法和其他方法,检测标准涉及国际标准、国家标准、行业标准和地方标准[6]。
口岸一线病原检测主要采用分子生物学检测法,而羽绒羽毛样品由于样品量大、病原含量低、样品杂质存留多等问题,病原浓度低。病原体富集技术就是将大体积羽绒羽毛样品中含量低的病原通过分离、浓缩等方法全部富集到可供检测的小体积样品中,从而增加单位体积样品中的病原数量,除去了某些干扰检测的成分,提高检测灵敏度和浓度。目前用于病原体富集的方法有很多,如选择性培养富集法、吸附洗脱法、膜过滤法、磁珠分离富集法、免疫捕捉聚合酶链式反应(Immunocapture-Polymerase Chain Reaction,IC-PCR)、荧光纳米微球法和芯片介电电泳等[7]。综合考虑羽绒羽毛样品特性以及富集效率、富集成本和便携性,需要开展新的思考与探索。
CP Select微生物富集系统作为液体样本前处理设备,可以从液体样品中快速富集微生物并形成小体积样液,可直接用于后续的培养、分析和鉴定,不需要离心、孵化、转移等传统操作。基于其特有的湿泡沫专利洗脱技术,可以使泡沫洗脱液迅速膨胀提供高达液体7倍以上的洗脱体积,极大地提高了生物样品的富集浓度和回收效率,使痕量生物样品的检测成为可能,同时大大减少时间和劳动力投入,目前已应用于环境、动物样本、废水、农产品等诸多领域的监测[8-12]。因此,为探究CP Select微生物富集系统在羽绒羽毛样品中的富集效率,本研究评估了CP Select系统富集羽绒羽毛样品中禽流感病毒的效率。研究结果表明,CP Select系统富集羽绒羽毛样品中禽流感病毒有效,其中模拟样品PBS洗脱液最高可富集27.5倍,tris洗脱液最高可富集740倍;羽绒羽毛样品tris洗脱液最高可富集52倍。本研究建立了进境羽绒羽毛样品有效痕量病原富集技术,利于后续可能的病原分离、核酸扩增及基因组测序研究。
1 材料与方法
1.1 仪器、试剂及样品
微生物富集系统(CP Select,InnovaPrep LLC);实时荧光定量PCR仪(QuantStudio™ 5,ThermoFisher);全自动核酸提取仪(GeneRotex 96,西安天隆科技有限公司);病毒DNA/RNA提取试剂盒(T800,西安天隆科技有限公司);330 M预过滤套筒(HC08016,InnovaPrep LLC);0.05 μM 浓缩移液器(CC08020-10,InnovaPrep LLC);PBS洗脱液(HC08000,InnovaPrep LLC);tris洗脱液(HC08001,InnovaPrep LLC);储存液(HC08558-5,InnovaPrep LLC);1×PBS缓冲液(BL302A,Biosharp);HiScript Ⅲ U+ One Step qRT-PCR Probe 5×Master Mix(Q611-01,Vazyme);荧光定量PCR引物为M-F:GACCRATCCTGTCACCTCTGAC,M-R:AGGGCATTYTGGACAAAKCGTCTA,M-Probe:TGCAGTCCTCGCTCACTGGGCACG(擎科生物);模拟样品为A/WSN/1933 (H1N1)病毒株,由本实验室利用反向遗传学构建而成;MDCK细胞由本实验室保存;荧光定量PCR阳性对照为禽流感病毒灭活尿囊液;羽绒羽毛样品为本实验室检测样品。
1.2 设施
模拟样品及羽绒羽毛样品处理过程均在生物安全二级实验室生物安全柜内进行。
1.3 方法
1.3.1 模拟样品浓缩后使用PBS洗脱液富集效率评估
本研究使用的模拟样品经MDCK细胞进行病毒滴定,嗜斑滴定数为5×108 pfu/mL。准备3个无菌1.5 mL EP管和3瓶1×PBS缓冲液,在每个EP管中加入200 μL 1×PBS缓冲液,然后在3个1.5 mL EP管和3瓶1×PBS缓冲液中分别加入0.1 μL、1 μL和10 μL模拟样品,震荡混匀,然后分别将3瓶1×PBS缓冲液利用微生物富集系统使用PBS洗脱液洗脱浓缩为200 μL浓缩液,提取RNA并进行荧光定量PCR实验,检测指标为禽流感病毒核酸(M基因)。
1.3.2 模拟样品浓缩后使用tris洗脱液富集效率评估
准备3个1.5 mL无菌EP管和3瓶1×PBS缓冲液,在每个EP管中加入200 μL 1×PBS缓冲液,然后在3个1.5 mL EP管和3瓶1×PBS缓冲液中分别加入0.1 μL、1 μL和10 μL模拟样品,震荡混匀,然后分别将3瓶1×PBS缓冲液利用微生物富集系统使用tris洗脱液洗脱浓缩为200 μL浓缩液,提取RNA并进行荧光定量PCR实验,检测指标为禽流感病毒核酸(M基因)。
1.3.3 羽绒羽毛样品浓缩后使用tris洗脱液富集效率评估
准备4份羽绒羽毛样品,分别使用1 L 1×PBS缓冲液浸泡处理。取浸泡后的液体,经330 M预过滤套筒初过滤和4℃沉淀后,吸取200 μL液体于1.5 mL EP管中,吸取500 mL液体于1×PBS缓冲液瓶中,分别将4瓶羽绒羽毛样品清洗液利用微生物富集系统使用tris洗脱液洗脱浓缩为200 μL浓缩液,提取RNA并进行荧光定量PCR实验,检测指标为禽流感病毒核酸(M基因)。
2 结果与分析
2.1 模拟样品浓缩后使用PBS洗脱液富集效率评估
为评估PBS洗脱液对流感病毒模拟样品富集效率,本研究将1.3.1中所取的9份液体各取200 μL提取RNA并进行荧光定量PCR实验,检测指标的具体数值统计如表1所示,可视化分析结果如图1所示。在200 μL PBS中分别加入0.1 μL、1 μL、10 μL模拟样品,Ct值分别是25.940、23.243和21.965;在500 mL PBS加入0.1 μL、1 μL、10 μL模拟样品,Ct值分别是39.048、35.802和30.848;将上述3份500 mL PBS依次利用微生物富集系统富集并使用PBS洗脱液洗脱浓缩为200 μL浓缩液,Ct值分别是34.267、31.921和28.573(表1),CP Select系统富集倍数分别是27.5倍、14.7倍和4.8倍(图1),表明使用CP Select系统能够有效富集PBS液体中的流感病毒。
表1 模拟样品浓缩后使用PBS洗脱液富集检测Ct值
Table 1 Ct values after concentration and enrichment with PBS elution buffer (simulated samples)
(μL) | 溶液浓度 | ||
200 μL (PBS) | 500 mL (PBS) | 200 μL (PBS浓缩) | |
0.1 | 25.940 | 39.048 | 34.267 |
1.0 | 23.243 | 35.802 | 31.921 |
10.0 | 21.965 | 30.848 | 28.573 |
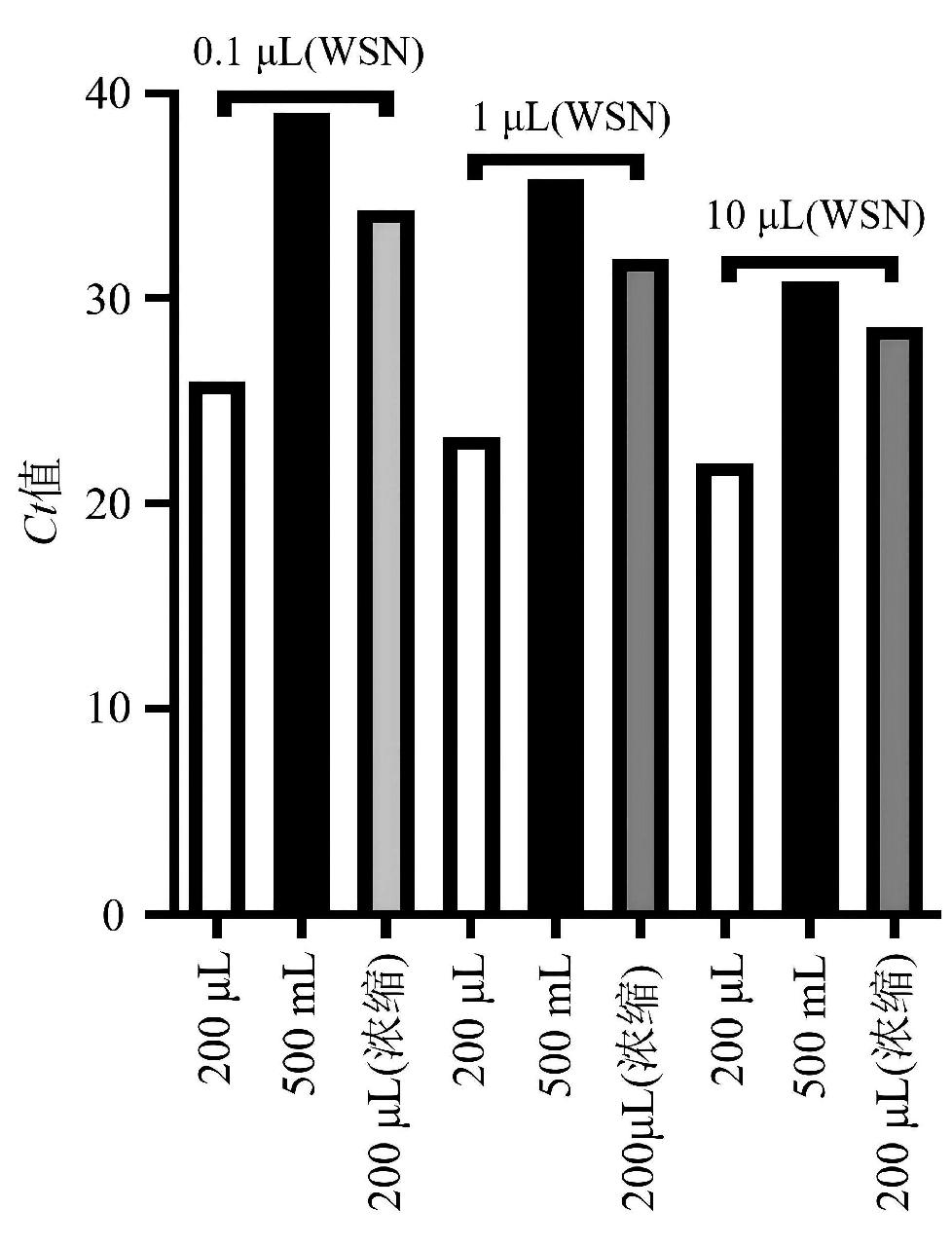
图1 模拟样品浓缩后使用PBS洗脱液富集效率评估
Fig.1 Enrichment efficiency evaluation using PBS elution buffer (simulated samples)
2.2 模拟样品浓缩后使用tris洗脱液富集效率评估
为评估不同洗脱液对于流感病毒模拟样品富集效率的影响,本研究将1.3.2中所取的9份液体各取200 μL提取RNA并进行荧光定量PCR实验,检测指标的具体数值统计见表2,可视化分析结果如图2所示。在200 μL PBS中加入0.1 μL、1 μL、10 μL模拟样品,Ct值分别是27.339、24.622和22.165;在500 mL PBS加入0.1 μL、1 μL、10 μL模拟样品,Ct值分别是40.017、36.010和32.760;将上述3份500 mL PBS依次利用CP Select系统使用tris洗脱液洗脱浓缩为200 μL浓缩液,Ct值分别是30.487、27.214和23.799(表2),CP Select系统富集倍数分别是740倍、444倍和498倍(图2),表明使用微生物富集系统tris洗脱液能够比PBS洗脱液更加有效富集PBS液体中的流感病毒,但是tris洗脱液富集的模拟样品将会失去病原体活性,而PBS洗脱液富集的病原可以保留病原体的生物学活性,可用于后续的病原体分离以分离样品中潜在的病原体,因此可以根据具体的需要选择合适的洗脱液。
表2 模拟样品浓缩后使用tris洗脱液富集检测Ct值
Table 2 Ct values after concentration and enrichment with Tris elution buffer (simulated samples)
(μL) | 溶液浓度 | ||
200 μL (PBS) | 500 mL (PBS) | 200 μL (tris浓缩) | |
0.1 | 27.339 | 40.017 | 30.487 |
1 | 24.622 | 36.010 | 27.214 |
10 | 22.165 | 32.760 | 23.799 |
2.3 羽绒羽毛样品浓缩后使用tris洗脱液富集效率评估
为评估CP Select系统使用tris洗脱液在实际样品中的富集效率,本探究将1.3.3中所取的8份液体各取200 μL提取RNA并进行荧光定量PCR实验,检测指标的具体数值统计见表3,可视化分析结果如图3所示。4份羽绒羽毛样品的洗脱液,Ct值分别是40.104、35.372、39.960、37.529;4份羽绒羽毛样品清洗液利用CP Select系统使用tris洗脱液洗脱浓缩为200 μL浓缩液,Ct值分别是34.399、32.801、36.123和32.530(表3);CP Select系统富集倍数分别是52倍、5.5倍、14倍和31倍(图3),表明使用微生物富集系统tris洗脱液能够有效富集羽绒羽毛清洗液中的流感病毒,可以作为候选的病原富集系统用于羽绒羽毛样品中病毒核酸的富集。
3 结语
微生物富集系统对进境羽绒羽毛样品中禽流感病毒的富集及后续潜在的病原分离和测序工作提供了可行性。从羽绒羽毛样品浸出液中浓缩病毒时需要权衡好成本、时间和病毒回收率等因素,这些取决于数据和样本的整体应用及后续用途。微生物富集系统在大量液体富集病原中存在天然的优势,但是羽绒羽毛样品区别于理想化的PBS缓冲液中的模拟样品,羽绒羽毛清洗液中的成分比较复杂,而微生物富集系统中过滤膜孔径很小,因此羽绒羽毛清洗液必须经过恰当的预处理和预过滤后才能继续富集,否则会发生滤膜堵塞导致富集终止的情况。因此需要配备适用化的预处理过滤膜或者其他装置以提高微生物富集系统在实际样品中的富集效果。
展望病毒体富集的相关方法,Liang C等[13]在研究中表明二氧化硅附着法和脱脂牛奶絮凝是腺病毒和肠道病毒等病毒有效的富集技术,Martínez-Puchol S等[9]发现靶向富集测序(Target Enrichment Sequencing,TES)可以通过序列特异性探针实现对病毒基因组的定向捕获与富集,诸如此类的研究为病毒体富集环节提供了不同的思路。Angga M S等[14]通过研究认为微生物富集系统具有很好的检测速度和检测效果,并对CP Select方法加以改进,提高了其灵敏度和通量。因此CP Select微生物富集系统的发展可以考虑提高其自动化程度、提升富集效率、降低耗材成本及开发便携式检测设备等,未来有望实现从病毒富集到检测的一体化流程,从而更好地应用于口岸一线检测。
参考文献
[1] 张爱琼, 刘江, 杨策勋, 等. 禽流感病毒检测方法及致病机理研究进展[J]. 中国畜禽种业, 2024, 20(3): 112-118.
[2] Verhagen J H, Lexmond P, Vuong O, et al. Discordant detection of avian influenza virus subtypes in time and space between poultry and wild birds; Towards improvement of surveillance programs[J]. PloS one, 2017, 12(3): e0173470. DOI: 10.1371/journal.pone.0173470.
[3] Fereidouni S, Starick E, Karamendin K, et al. Genetic characterization of a new candidate hemagglutinin subtype of influenza A viruses[J]. Emerging microbes & infections, 2023, 12(2): 2225645. DOI: 10.1080/22221751.2023.2225645.
[4] Pedersen J C. Hemagglutination-inhibition test for avian influenza virus subtype identification and the detection and quantitation of serum antibodies to the avian influenza virus[J]. Avian Influenza Virus, 2008: 53-66. DOI: 10.1007/978-1-59745-279-3_8.
[5] 祝福勇, 樊云荣, 孔园园. H5和H7禽流感病毒综述[J]. 中国畜牧业, 2023(15): 45-46.
[6] 刘嘉静, 徐彪, 王群, 等. 禽流感病毒检测方法和标准研究进展[J]. 中国口岸科学技术, 2025, 7(4): 24-31.
[7] 闵现华, 韩跃武, 刘箐. 微量病原富集技术研究进展[J]. 中国公共卫生, 2010, 26(8): 1066-1069.
[8] Timme RE, Woods J, Jones JL, et al. SARS-CoV-2 wastewater variant surveillance: pandemic response leveraging FDA’s GenomeTrakr network[J]. mSystems, 2024, 9(6): e0141523. DOI: 10.1128/msystems.01415-23.
[9] Martínez-Puchol S, Tarradas-Alemany M, Mejías-Molina C, et al. Target enrichment metaviromics enables comprehensive surveillance of coronaviruses in environmental and animal samples[J]. Heliyon, 2024, 10(11): e31556. DOI: 10.1016/j.heliyon.2024.e31556.
[10] Lancaster E, Winston R, Martin J, et al. Urban stormwater green infrastructure: Evaluating the public health service role of bioretention using microbial source tracking and bacterial community analyses[J]. Water Research, 2024, 259: 121818. DOI: 10.1016/j.watres.2024.121818.
[11] Trudel-Ferland M, Levasseur M, Goulet-Beaulieu V, et al. Concentration of foodborne viruses eluted from fresh and frozen produce: Applicability of ultrafiltration[J]. International Journal of Food Microbiology, 2024, 416: 110687. DOI: 10.1016/j.ijfoodmicro.2024.110687.
[12] Singh S, Aw TG, Rose JB. Evaluation of an Automated Ultrafiltration System for Concentrating a Range of Viruses from Saline Waters[J]. Food And Environmental Virology, 2024, 16(3): 422-431.
[13] Liang C, Wang J, Zhang Y, et al. Assessing the viral enrichment methods and their roles in indicating wastewater-associated pollution in aquatic environments[J]. Ecotoxicology and Environmental Safety, 2025, 292: 117951. DOI: 10.1016/j.ecoenv.2025.117951.
[14]Angga M S, Malla B, Raya S, et al. Optimization and performance evaluation of an automated filtration method for the recovery of SARS-CoV-2 and other viruses in wastewater[J]. Science of the Total Environment, 2023, 882: 163487. DOI: 10.1016/j.scitotenv.2023.163487.
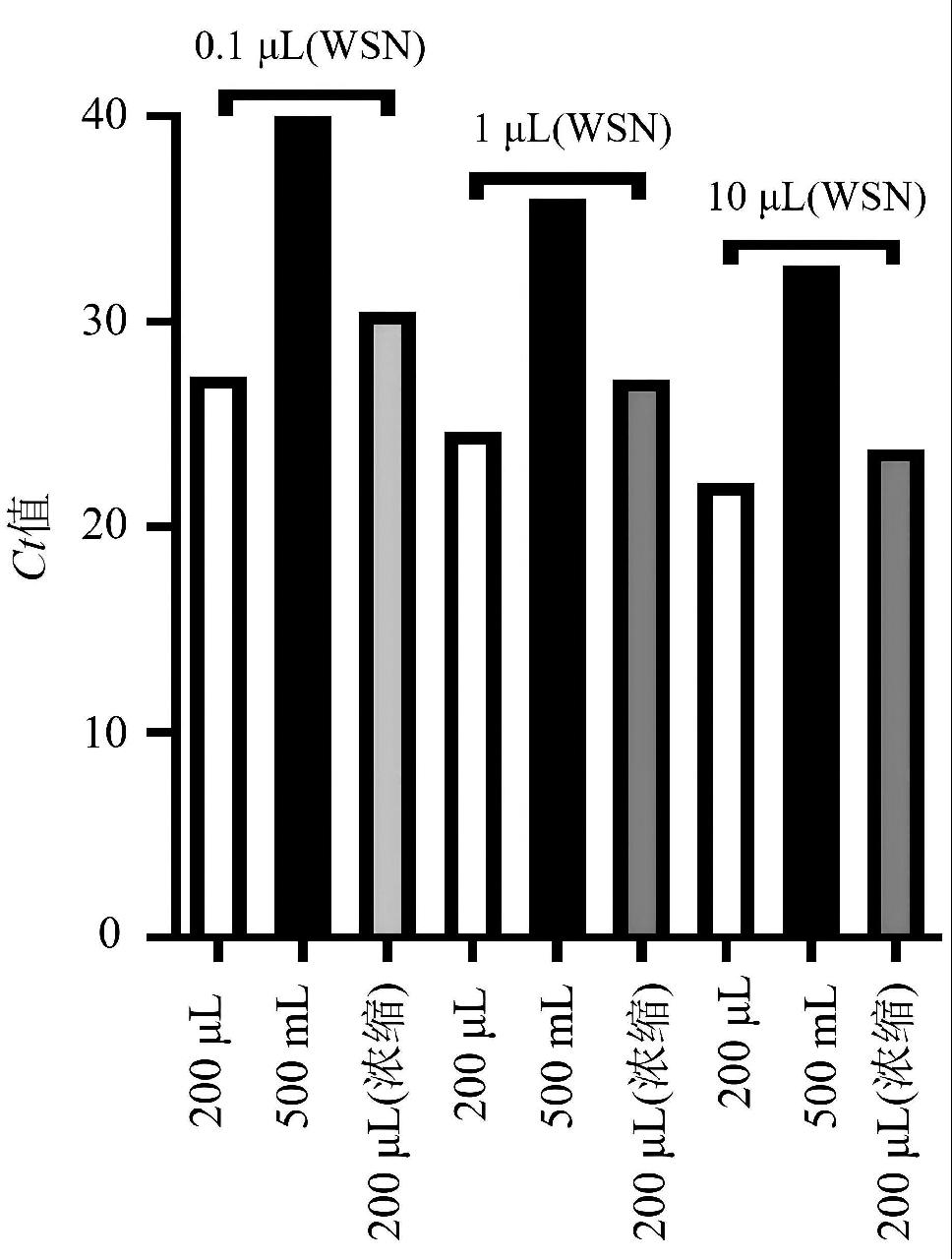
图2 模拟样品浓缩后使用tris洗脱液富集效率评估
Fig.2 Enrichment efficiency evaluation using tris elution buffer (simulated samples)
表3 羽绒羽毛样品浓缩后使用tris洗脱液富集检测Ct值
Table 3 Ct values after concentration and enrichment with Tris elution buffer (down and feather samples)
样品序号 | 溶液浓度 | |
500 mL (PBS) | 200 μL (tris浓缩) | |
样品1 | 40.104 | 34.399 |
样品2 | 35.372 | 32.801 |
样品3 | 39.960 | 36.123 |
样品4 | 37.529 | 32.530 |
图3 羽绒羽毛样品浓缩后使用tris洗脱液富集效率评估
Fig.3 Enrichment efficiency evaluationusing tris elution buffer (down and feather samples)







