CopyRight 2009-2020 © All Rights Reserved.版权所有: 中国海关未经授权禁止复制或建立镜像
小鼠源性成分实时荧光PCR检测方法的建立与应用
作者:杜思乐 张小寒 丁仰保 白子龙 徐子涵 刘朋朋 汪琳 蒲静
杜思乐 张小寒 丁仰保 白子龙 徐子涵 刘朋朋 汪琳 蒲静
杜思乐 1 张小寒 1 丁仰保 2 白子龙 1 徐子涵 1 刘朋朋 1 汪 琳 1 蒲 静 1 *
摘 要 本研究基于GenBank上已发布的小鼠线粒体基因序列进行多重比对,针对靶基因Atp6设计特异性引物和TaqMan探针,通过对反应体系和反应条件的优化,建立一种快速检测小鼠源性成分实时荧光聚合酶链式反应(Polymerase Chain Reaction,PCR)检测方法,并对其特异性、重复性、灵敏度进行测定。同时,将新建方法应用于口岸送检的鼠血等生物材料样品,并与现行标准检测方法进行对比。结果显示,建立的小鼠源性成分荧光PCR检测方法具有特异性强、灵敏度高、快速准确等优点,能够有效检出5.15 copies/μL的小鼠源性成分样本,适用于口岸、疾控、医疗等领域对小鼠源性成分特别是生物材料样本的快速检测。
关键词 小鼠;源性成分;实时荧光聚合酶链式反应;生物材料
Establishment and Application of a Real-Time Fluorescent PCR Detection Method for Mouse-Derived Components
DU Si-Le1 ZHANG Xiao-Han1 DING Yang-Bao2 BAI Zi-Long1
XU Zi-Han1 LIU Peng-Peng1 WANG Lin1 PU Jing1*
Abstract By retrieving and aligning murine mitochondrial gene sequences deposited in GenBank, species-specific primers and a TaqMan probe were designed targeting the Atp6 gene. After systematic optimization of reaction components and thermal-cycling parameters, a rapid real-time fluorescence polymerase chain reaction (PCR) assay for mouse-derived components was established. The specificity, repeatability and sensitivity of the newly developed method were comprehensively evaluated. Subsequently, the assay was applied to port-submitted biological samples such as rat blood and compared with the current standard protocol. The results demonstrated that the established real-time PCR method possesses high specificity, excellent sensitivity and rapidity, reliably detecting as few as 5.15 copies μL of murine DNA. The method is therefore suitable for the rapid detection of mouse-derived components, especially in biological specimens, at ports, centers for disease control and prevention, and clinical laboratories.
Keywords mouse; derived components; real-time fluorescent polymerase chain reaction (PCR); biomaterials
本论文由1+X合作单位资助
基金项目:国家重点研发计划课题(2023YFC3304001);中国海关科学技术研究中心自立课题(2023HZ12)
第一作者:杜思乐(1992—),女,汉族,北京人,博士,中级兽医师,主要从事动物源性成分及物种鉴定工作,E-mail: sile0228@163.com
通信作者:蒲静(1977—),女,汉族,河北唐山人,博士,正高级兽医师,主要从事物种鉴定和动物检疫工作,E-mail: pujing 1229@126.com
1. 中国海关科学技术研究中心 北京 100026
2. 南宁海关技术中心 南宁 530200
1. Science and Technology Research Center of China Customs, Beijing 100026
2. Technology Center of Nanning Customs District, Nanning 530200
实验小鼠(Mouse)在各类研究中发挥着不可替代的作用。小鼠属于啮齿目(Rodentia)鼠科(Muridae)动物,由小家鼠(Mus musculus)驯化而来,经长期人工培育,拥有大量的近交系、突变系和封闭系[1-2]。小鼠成熟早、繁殖力强,全年多发情,每胎产仔8~15只,年产6~9胎[3]。其身形娇小,饲养管理便捷,虽对环境适应能力弱,但这一特性使其对多种毒素、病原体以及致癌物质极为敏感。另外,小鼠的基因组与人类高度同源,约90%的基因与人类相似[4]。早在1913年,小鼠就已被用于实验,如今已成为使用量最大、研究最深入的哺乳类实验动物,广泛应用于药物研发、肿瘤学、免疫学、遗传学等众多领域[5-8]。
近年来,鼠血液、鼠血清作为口岸业务量最大的出口生物材料,为保证报关信息的准确性,需判定其源性成分来源,以便关税征收以及保护我国遗传资源安全。同时,为保障鼠血清等小鼠源性相关生物材料的快速通关,要求检测时长≤10个工作日。目前,我国鼠源性成分检测方法多为鼠源通用型检测方法或大鼠源性成分检测方法,尚无精准的小鼠源性成分快速检测方法。在现行有效的动物源性成分的检测标准中,应用最广泛的GB/T 38164—2019《常见畜禽动物源性成分检测方法 实时荧光PCR法》[9],仅能够检测大鼠源性成分;而GB/T 35918—2018《动物制品中动物源性检测基因条码技术 Sanger测序法》[10]等测序法的检测周期较长。为满足口岸快速通关的需求,保障合法贸易顺畅,维护我国生物资源安全,本研究建立了小鼠源性成分实时荧光聚合酶链式反应(Polymerase Chain Reaction,PCR)检测方法,为口岸进出口小鼠相关生物材料提供快速、灵敏、精准的分子鉴定方法。
1 材料和仪器
1.1 小鼠基因质粒的合成、鼠源性样本的收集
参照GenBank中小鼠的参考序列(GenBank:NC_005089.1),以线粒体基因Atp6基因全长(坐标7927—8607)为模板,委托生物公司合成小鼠Atp6基因全长序列(681 bp),并克隆入pUC57载体,得到含有小鼠线粒体基因的合成质粒MM-Atp6-pUC57。以该质粒作为阳性对照进行小鼠源性成分荧光PCR方法的建立。
本研究所使用的样品源自2022—2023年口岸送检的20份鼠源性生物材料(包括大鼠、小鼠的全血、血清、血浆等)及进境鼠血(来源于大鼠、小鼠等实验鼠),详细信息见表1,样本保存于-20℃冰箱。
表1 鼠源性样本信息
Table 1 Information of mouse-derived samples
样本编号 | 物种名 | 样本类型 | 样本来源 |
1 | 大鼠 (Rattus rattus) | 全血 | 出境 |
2 | 大鼠 (Rattus rattus) | 全血 | 出境 |
3 | 大鼠 (Rattus rattus) | 血清 | 出境 |
4 | 大鼠 (Rattus rattus) | 血清 | 出境 |
5 | 大鼠 (Rattus rattus) | 血浆 | 进境 |
6 | 大鼠 (Rattus rattus) | 血浆 | 进境 |
7 | 小鼠 (Mus musculus) | 全血 | 出境 |
8 | 小鼠 (Mus musculus) | 全血 | 出境 |
9 | 小鼠 (Mus musculus) | 血清 | 出境 |
10 | 小鼠 (Mus musculus) | 血清 | 出境 |
11 | 小鼠 (Mus musculus) | 血清 | 出境 |
12 | 小鼠 (Mus musculus) | 血清 | 出境 |
13 | 小鼠 (Mus musculus) | 血清 | 出境 |
14 | 小鼠 (Mus musculus) | 血清 | 出境 |
15 | 小鼠 (Mus musculus) | 血清 | 进境 |
16 | 小鼠 (Mus musculus) | 血浆 | 进境 |
17 | 小鼠 (Mus musculus) | 血浆 | 进境 |
18 | 小鼠 (Mus musculus) | 血浆 | 进境 |
19 | 小鼠 (Mus musculus) | 血浆 | 进境 |
20 | 小鼠 (Mus musculus) | 血浆 | 进境 |
21 | 豚鼠 (Cavia porcellus) | 血清 | 出境 |
22 | 仓鼠 (Mesocricetus auratus) | 血清 | 出境 |
23 | 褐家鼠 (Rattus norvegicus) | 活体 | 进境 |
1.2 引物探针设计合成
从GenBank下载多组小鼠的线粒体基因序列,使用DNAMAN 9.0软件进行多重序列比对后,选取Atp6基因作为靶基因,使用Oligo 7设计1对小鼠特异性引物和TaqMan探针(引物探针名称、序列及检测靶基因见表2)。Atp6基因探针的5'端标记荧光剂FAM,3'端标记淬灭剂BHQ1。引物和探针均由生工生物工程(上海)股份有限公司合成。
1.3 试剂
Prefilled Viral Total NA Kit-Duo试剂盒购自赛默飞世尔科技公司;HS Taq DNA 聚合酶、dNTP、10×PCR Buffer、MgCl2等,均购自TaKaRa公司。
1.4 仪器
冷冻离心机(Centrifuge 5415 R,Eppendorf公司);涡旋振荡器(MS2,Minishaker公司);加热制冷震荡金属浴(SCI-100HCM-Pro,Scilogex公司);全自动核酸提取仪(KINGFI-SHER-Duo,赛默飞世尔科技公司);实时荧光定量PCR仪(QuantStudio 5/7,赛默飞世尔科技公司)。
2 实验方法
2.1 小鼠源性成分实时荧光PCR方法的建立和优化
以含有小鼠线粒体基因的合成质粒MM-Atp6-pUC57为模板,使用实时荧光定量PCR仪QuantStudio对7对小鼠源性成分的引物、探针、Mg2+等各组分浓度进行优化。通过综合分析扩增曲线形状和循环阈值(Cycle Threshold,Ct),对反应参数进行筛选和验证,优化出最佳反应体系。
2.2 小鼠源性成分实时荧光PCR方法的特异性
应用建立的反应体系,以ddH2O为阴性对照,同时对大鼠、小鼠、豚鼠、仓鼠、褐家鼠(样本编号1、7、21、22、23)的样本进行检测,以验证方法的特异性。
2.3 小鼠源性成分实时荧光PCR方法的重复性
对重组质粒进行10倍梯度稀释3个浓度,选取浓度为5.15×105~5.15×103 copies/μL,每个浓度设置3个重复,ddH2O为阴性对照,按照优化的反应体系进行扩增,检测该方法的重复性,并测定组内变异系数(CV)。
2.4 小鼠源性成分实时荧光PCR方法的灵敏度
对重组质粒进行10倍梯度稀释,选取初始浓度为5.15×105copies/μL,对其进行连续6个浓度稀释,ddH2O为阴性对照,按照优化的反应体系进行扩增,确定建立方法的分析灵敏度。
2.5 标准曲线的建立
选取灵敏度试验中的6个浓度梯度的DNA模板,即5.15×105~5.15×100 copies/μL,ddH2O为阴性对照,按照已经优化的qPCR的反应条件扩增,以循环数为纵轴,拷贝数浓度的对数为横轴,建立标准曲线,计算相关系数(R2)和扩增效率。
2.6 对口岸送检的鼠源性产品的检测应用
2.6.1 对口岸送检的鼠源性样本的核酸提取
使用Fisher Scientific Prefilled Viral Total NA Kit-Duo试剂盒,按照说明书提取流程提取鼠源性样本的DNA。
2.6.2 对口岸送检的鼠源性产品的检测鉴定
使用本文建立的小鼠源性成分实时荧光PCR检测方法及国家标准GB/T 38164—2019对实验室收集的20份鼠源性成分样本(样本编号1—20)进行小鼠、大鼠源性成分检测;同时,使用现行国家标准GB/T 35918—2018对上述样本进行PCR,并将PCR扩增得到的片段进行测序分析,将测序结果与实时荧光PCR检测结果进行比对验证。
3 结果与分析
3.1 双重实时荧光PCR反应条件优化
经优化确立的小鼠源性成分实时荧光PCR反应体系体积为25 μL,体系组成见表3。反应参数:94℃ 3 min; 94℃ 15 s,60℃ 45 s,40个循环;每个循环在60℃时收集荧光信号。
3.2 特异性试验
使用建立的小鼠源性成分荧光PCR方法对小鼠、大鼠、豚鼠、仓鼠的血清进行检测。结果显示建立的检测方法能够有效检测出小鼠血清,与其余非小鼠源性成分基因组无交叉反应,表明该方法特异性良好,如图1所示。
表3 小鼠源性成分实时荧光PCR反应体系组成
Table 3 Composition of real-time fluorescent PCR reaction system for mouse-derived components
试剂名称 | 终浓度 | 体积 (μL) |
PCR Master Mix (2x) | 1× | 12.5 |
Mouse-1 (10 μmol/L) | 600 nmol/L | 1.5 |
Mouse-2 (10 μmol/L) | 600 nmol/L | 1.5 |
Mouse-Probe (10 μmol/L) | 200 nmol/L | 0.5 |
DNA 模板 (5~50 ng/μL) | — | 5 |
双蒸水 | — | 2.5 |
总体积 | — | 25 |
注: “—”表示对终浓度不作要求.
3.3 重复性试验
由表4的重复试验结果可知,不同浓度样本的检测结果变异系数最高为2.05%,各浓度的Ct变异系数均小于5%,表明本方法具有较好的重复性。
表4 实时荧光PCR检测方法的重复性测试结果
Table 4 Repeatability test results of the real-time fluorescence PCR detection method
目的基因 | (copies/μL) | (Ct值) | (Ct值) | (%) |
Atp6 | 5.15×105 | 19.143 | 19.13 | 0.12 |
19.105 | ||||
19.148 | ||||
5.15×104 | 23.414 | 22.88 | 2.03 | |
22.595 | ||||
22.626 | ||||
5.15×103 | 25.573 | 26.18 | 2.05 | |
26.400 | ||||
26.577 |
3.4 灵敏度试验
对重组质粒MM-Atp6-pUC57进行10倍系列稀释,选取初始浓度为5.15×105 copies/μL,对其进行连续6个浓度稀释,ddH2O为阴性对照,按照优化的反应体系进行扩增,最低可以稳定检出5.15 copies/μL 的小鼠源性成分DNA(图2),表明方法的灵敏度高,能够满足口岸检测要求。
3.5 标准曲线与荧光PCR效率计算
选取DNA模板浓度为5.15×105 ~5.15×100 copies/μL绘制qPCR标准曲线,具有良好的线性关系。由图3可知,该方法的标准曲线方程为y = -3.2777x + 38.119,相关系数R2为0.998,PCR反应效率为101.88%。荧光扩增效率正常范围内,Ct值与模板浓度对数的线性关系可靠,具有良好的稳定性和重复性,定量结果准确,实验误差控制在合理范围内。
3.6 对口岸送检鼠源性成分产品的检测应用
使用建立的小鼠源性成分实时荧光PCR检测方法及国家标准GB/T 38164—2019对实验室收集的20份鼠源性成分样本(样本编号1—20)进行小鼠、大鼠源性成分检测,样本编号1—6检出为大鼠源性成分(图4),样本编号7—20检出为小鼠源性成分(图5)。同时,用国家标准GB/T 35918—2018对20份小鼠、大鼠源性成分样本(样本编号1—20)进行PCR,并将PCR扩增得到的片段(图6)进行测序分析,测序结果经BLAST比对显示,样本编号1—6均为大鼠,样本编号7—20均为小鼠。上述检测结果表明建立的小鼠源性成分实时荧光PCR方法与标准方法的检测结果完全一致。
4 讨论
实验小鼠由于基因序列、生理结构和病理反应均与人类有诸多相似之处,因而作为实验动物已经广泛应用于生命科学和医疗等相关研究领域。小鼠作为生物材料的类型含了肝脏、肾脏、心脏、脑组织等器官组织材料,小鼠胚胎干细胞、小鼠巨噬细胞、淋巴细胞等免疫细胞,以及小鼠全血、小鼠血清等生物材料。近年来,我国实验小鼠、小鼠源性生物材料的进出口呈现快速增长趋势,2024年中国实验小鼠市场规模达52.4亿元,其中海外扩张速度超过国内市场增长,并且,基因修饰小鼠成为核心增长点[11]。因此,如何精准判定和区分小鼠与其他鼠类是完善实验动物监管体系、推动行业规范化发展,以及为出口提供技术保障的迫切需要。
由于小鼠生物材料样本类型多样,组织细胞、全血类型的样本基因组提取后的核酸浓度较高,检测相对容易;而鼠血清、鼠毛皮等样本,基因组含量较低,提取的核酸浓度低,对检测方法要求更高的灵敏度。线粒体基因组具有进化速度快、母系遗传等特点,其在细胞内的拷贝数远高于核基因组DNA,这种高拷贝特性使其在检测中具备显著优势。当样本量极少、DNA降解严重时,核基因组DNA会因拷贝数低易出现检测失败,而线粒体DNA凭借高拷贝数,能大幅提升扩增成功率,灵敏度远高于核DNA标记系统。因此,本研究选取小鼠的线粒体基因作为靶基因,建立小鼠成分实时荧光PCR检测方法。通过对小鼠线粒体基因组的特定保守区域设计特异性引物探针,能更高效、准确地判定是否为小鼠,便于与其他鼠类进行区分。通过建立方法的特异性、重复性、灵敏性测试,结果显示本研究建立的小鼠源性成分荧光PCR检测方法仅能特异性检出小鼠源性成分,与小鼠的其他近源种DNA均不发生交叉反应;重复试验结果显示不同浓度的小鼠样品变异系数最高为2.05%,Ct变异系数<5%,重复性好;灵敏度试验结果表明本方法可稳定检出5.15 copies/μL的目标DNA,PCR反应效率可达102.64%,表明建立方法灵敏度高,适合检测低核酸浓度的样本,能够满足口岸对小鼠源性成分的检测需求。
相较于国内已发布的鼠类源性成分的检测,我国现行标准有GB/T 35918—2018和BJS 201904《食品中多种动物源性成分检测实时荧光PCR法》[12],均为传统的Sanger测序法,虽然结果准确,但流程复杂,需要测序才能判定物种成分,单次检测需要3~5 d,单样成本高,不适合大批量样本的快速筛查和检测。现行有效的标准中使用实时荧光PCR检测方法检测鼠类源性成分的方法有 GB/T 38164—2019,但该标准仅能够准确检测肉类食品中的大鼠源性成分。在我国,周如华等[13]、王学政等[14]、王兴陇等[15]、苏佳等[16]先后建立了鼠源性成分实时荧光PCR快速检测技术,应用于肉类制品以及鼠源细胞等,但均为鼠源性成分的通用检测方法,而缺乏小鼠源性成分特异性检测方法。刘明明等[17]建立了双重实时荧光重组酶辅助扩增(Real-Time Recombinaseaided Amplification,Rt-RAA)方法,能够快速检测肉制品中的大鼠和小鼠[17],但此方法灵敏度略低、单样本成本高,适用于现场应急检测、基层筛查等即时性需求场景,无法满足口岸通关需要的精准检测依据和批量检测能力。因此,本研究建立的小鼠源性成分实时荧光PCR检测方法,不仅特异性强、灵敏度高、操作简便,全程仅需1~2 h,更适合高通量快速检测,极大地缩短了检测时长,能够有效加快口岸通关速度,以应对我国小鼠生物材料出口贸易需求,为我国进出口贸易安全提供了技术支撑。
此外,本研究建立的小鼠源性成分特异性实时荧光PCR检测方法还具有诸多应用场景。在生物安全监测方面,可利用小鼠特异性荧光PCR检测方法对实验环境、实验材料进行监测,检测是否存在其他鼠类成分的污染,确保实验结果的准确性和可靠性;同时也能防止实验小鼠逃逸后与野生鼠类杂交,对生态环境造成潜在风险。在食品安全领域,一些食品加工厂、仓储场所容易受到鼠类的污染,小鼠特异性荧光PCR检测方法可以快速检测食品及其原料中是否含有小鼠的成分,及时发现鼠类污染情况,保障食品安全。在疾病防控领域,某些鼠类是疾病的传播媒介,通过检测环境中是否存在小鼠以及小鼠的携带病原体情况,能够为疾病的预警和防控提供重要依据,有助于及时采取防控措施,防止疾病的传播和流行。
5 结论
本研究利用特异性位点荧光PCR技术,通过设计1对小鼠源性成分引物和1条特异性探针,建立了可以有效检测小鼠源性成分的实时荧光PCR检测方法。特异性试验结果显示不与其他近源种DNA发生交叉反应,重复试验Ct变异系数<5%,灵敏度试验显示该方法可稳定检出5.15 copies/μL的目标DNA。将建立的小鼠源性成分实时荧光PCR检测方法应用于进出境的鼠源性成分生物材料检测中,检测结果与现行标准方法结果一致。本研究建立的方法特异性强、灵敏度高、重复性好,可更好地适用于口岸、医疗、食品、疾控等领域实现对小鼠源性成分的快速检测。
参考文献
[1] 代小佩. 小鼠“常驻”实验室原因不只是性价比高[J]. 中国科技奖励, 2020, 3: 76-77.
[2] 孔琪. 小动物、大贡献之科学认识实验小鼠[J]. 中国比较医学杂志, 2015, 25(12): 87-88.
[3] 邵义祥. 实验动物学基础[M]. 东南大学出版社, 2018: 77.
[4] Waterston R H, Lindblad-Toh K, Birney E, et al. Initial sequencing and comparative analysis of the mouse genome[J]. Nature, 2002. 420: 520-562.
[5] 秦川, 张连峰. 小鼠基因工程与医学应用[M]. 中国协和医科大学出版社, 2010: 1-4.
[6] 秦川, 魏泓, 谭毅, 等. 实验动物学[M]. 人民卫生出版社,2010: 38.
[7] 杨斐, 胡樱. 实验动物学基础与技术[M]. 复旦大学出版社, 2019: 114-115.
[8] 孔繁瑶. 兽医大辞典[M]. 中国农业出版社, 1999: 446.
[9] GB/T 38164—2019 常见畜禽动物源性成分检测方法 实时荧光PCR法[S]. 北京: 中国标准出版社, 2019.
[10] GB/T 35918—2018 动物制品中动物源性检测基因条码技术 Sanger测序法[S]. 北京: 中国标准出版社, 2018.
[11]高毅. 南模生物: 基因修饰小鼠领域展现出高增长潜力[N]. 上海证券报, 2025-4-30.
[12]杨艳歌, 李莉, 王丹丹, 等. 多重real-time PCR技术快速鉴别特种乳中的乳源动物成分[J]. 食品科学, 2021(16): 192-194.
[13]周如华, 张玉红, 黄洪武, 等. 实时荧光定量PCR检测羊肉制品中鼠源性成分[J]. 中国法医学杂志, 2014, 29(6): 534-537.
[14]王学政, 季福玲, 刘志胜, 等. 一种用于实时荧光PCR法检测肉制品中鼠源性成分特异性引物的研发[J]. 中国生物制品学杂志, 2018, 31(7): 775-777+781.
[15]王兴陇, 包晓婧, 张海霞, 等. 鼠源VCAM-1基因TaqMan实时荧光定量PCR检测方法的建立[J]. 中国兽医科学, 2018, 48(1): 27-33.
[16]苏佳, 赵炜, 秦义娴, 等. 鼠源细胞TaqMan实时荧光定量PCR检测方法的建立[J]. 中国兽药杂志, 2023, 57(3): 10-16.
[17]刘明明, 周朝旭, 颜海燕, 等. 利用双重实时荧光重组酶辅助扩增技术快速检测肉制品中鼠源性成分[J]. 肉类研究, 2024, 38(9): 15-20.
表1(续)
表2 小鼠源性成分荧光PCR引物、探针
Table 2 Fluorescent primers and probes for mouse-derived components
引物、探针名称 | 序列 ( 5 '~3 ' ) | 靶基因 | 扩增片段 (bp) |
Mouse-1 | CTATTCCCATCCTCAAAACGC | Atp6 | 123 |
Mouse-2 | TTAGGGTTCATGTTCGTCCTT | ||
Mouse-Probe | AACCGWCTCCATTCTTTCCAACAC |
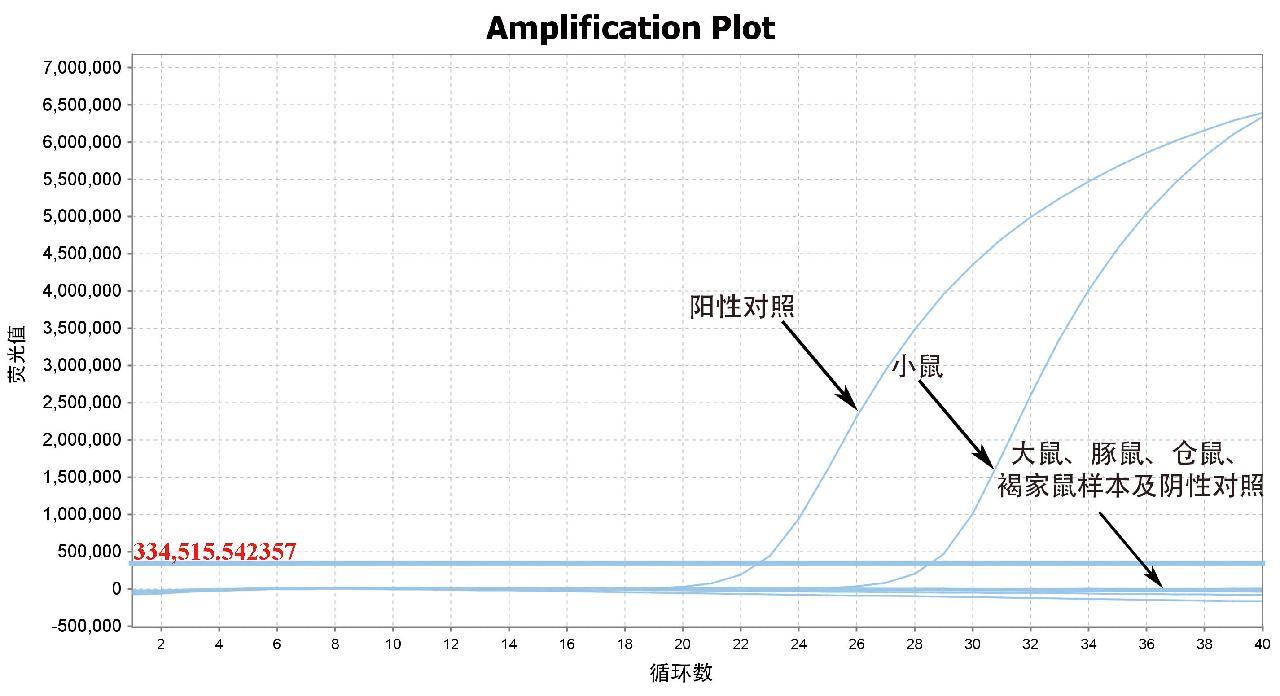
图1 实时荧光PCR特异性试验结果
Fig.1 Specificity test of real-time fluorescent PCR
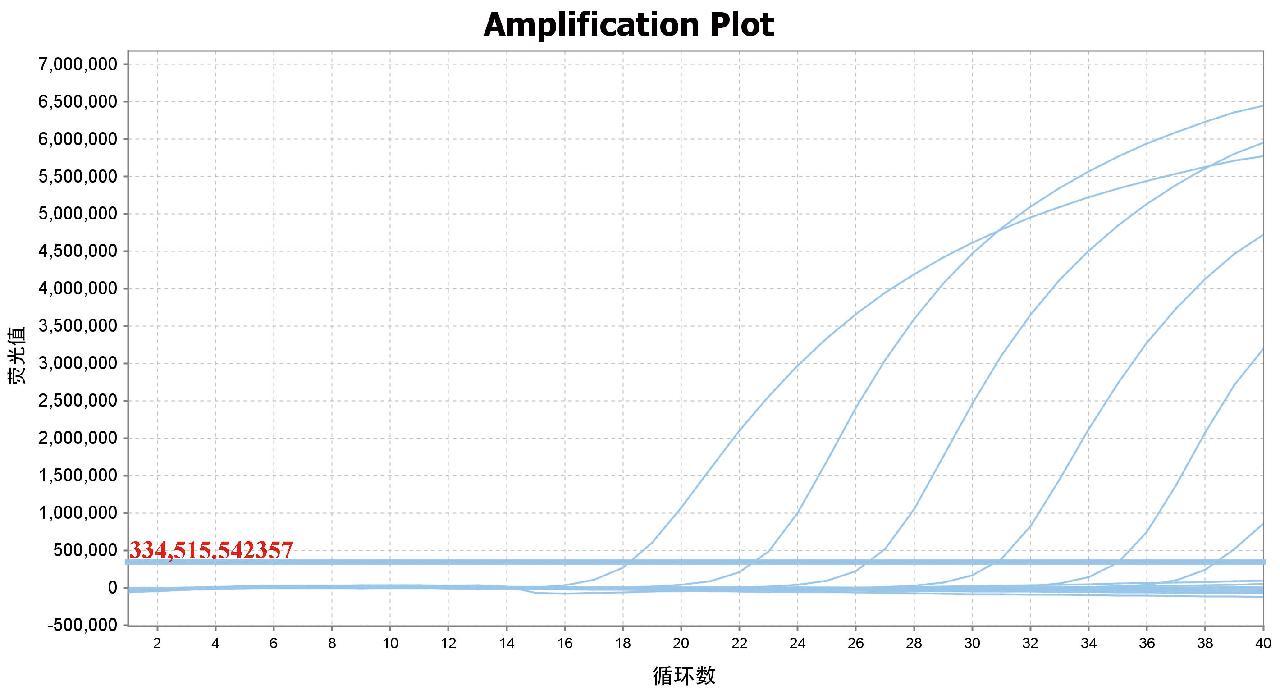
图2 实时荧光PCR灵敏度试验
Fig.2 Sensitivity test of real-time fluorescent PCR
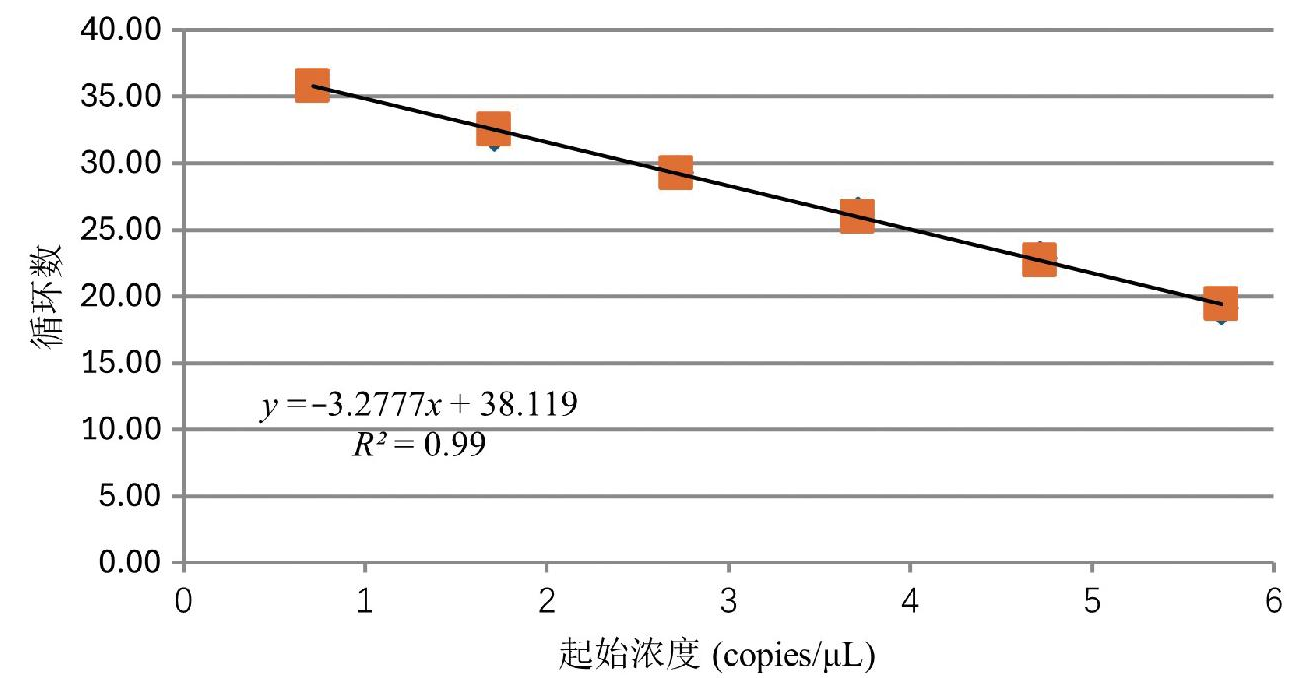
图3 实时荧光PCR标准回归曲线
Fig.3 Standard curve of real-time fluorescent PCR
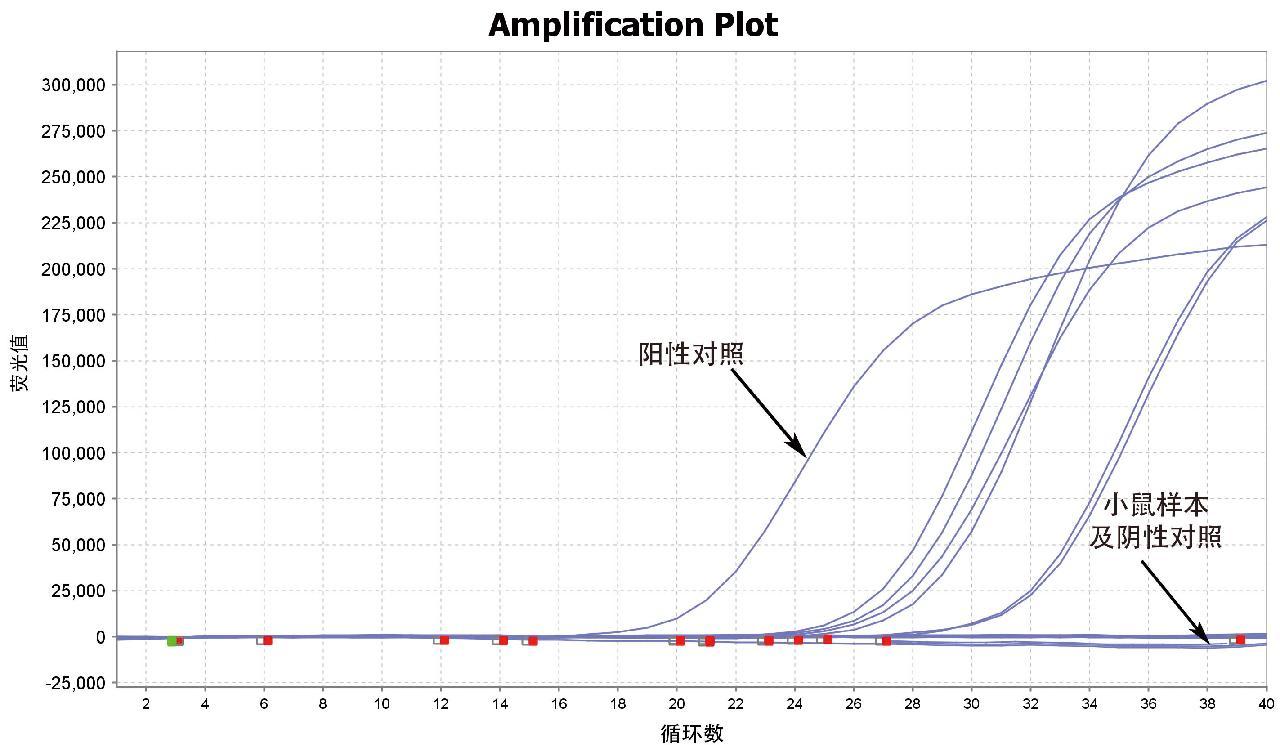
图4 实时荧光PCR检测6份大鼠源性成分样本
Fig.4 Real-time fluorescent PCR detection of 6 rat-derived components in samples
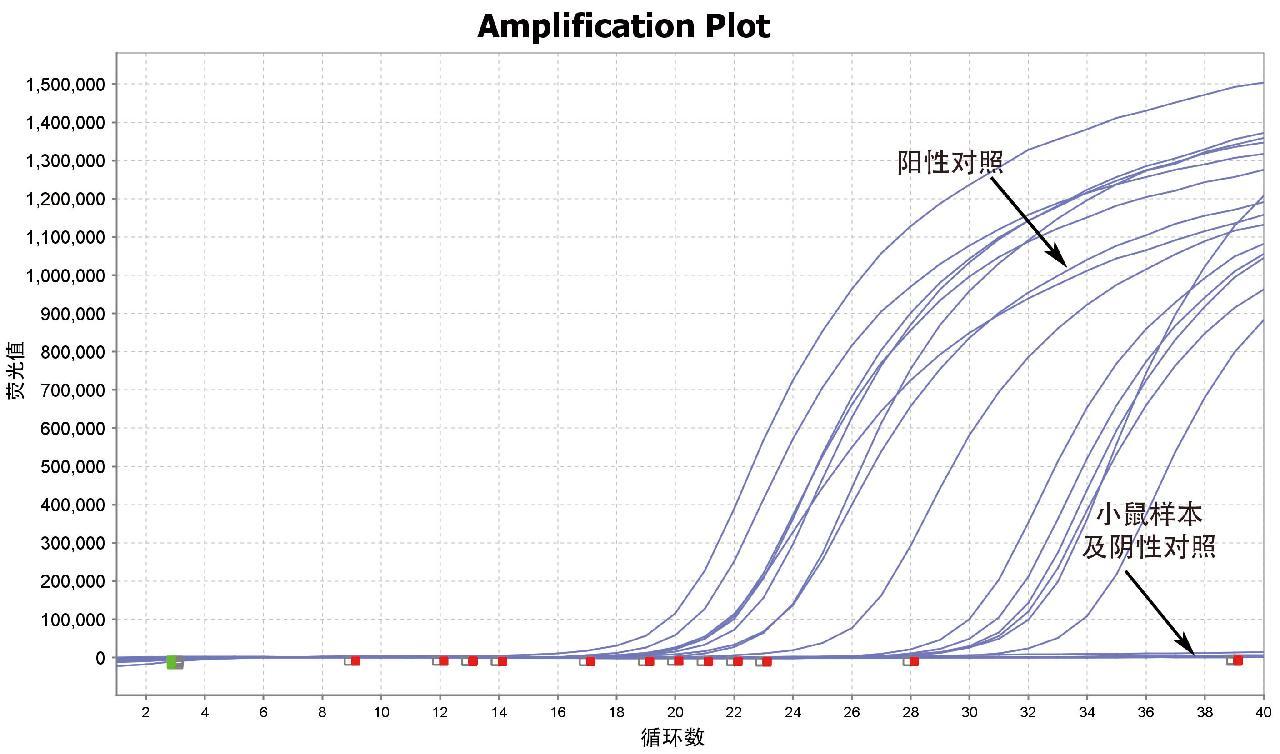
图5 实时荧光PCR检测14份小鼠源性成分样本
Fig.5 Real-time fluorescent PCR detection of 14 mouse-derived components in samples

M: DNA Marker (100~2000 bp); 1—6: 大鼠源性成分样本; 7—20: 大鼠源性成分生物材料; NTC: 空白对照; NEG: 阴性对照; POS: 阳性对照
图6 常规PCR检测大鼠、小鼠源性成分样本
Fig.6 Conventional PCR detection of rat- and mouse-derived components in samples







