CopyRight 2009-2020 © All Rights Reserved.版权所有: 中国海关未经授权禁止复制或建立镜像
莱氏无胆甾原体四川株的分离鉴定及Eno、 Gap、 pdhC因子生物信息分析
作者:杨俊 高源 刘启军 吴蕊 史梅梅 蒲静 王昱 聂福平
杨俊 高源 刘启军 吴蕊 史梅梅 蒲静 王昱 聂福平
杨 俊 1 高 源 1,2# 刘启军 1 吴 蕊 1 史梅梅 1 蒲 静 3 王 昱 1 聂福平 1 *
摘 要 为莱氏无胆甾原体的体外表达和基因工程疫苗的研究提供依据,本研究从四川某奶牛场患有乳房炎的奶牛上首次分离到1株莱氏无胆甾原体(命名为:WQ001),对编码Eno、Gap、pdhC蛋白基因进行体外扩增、测序并进行遗传进化分析、蛋白质的二级结构和B细胞抗原表位预测。结果表明,WQ001分离株与莱氏无胆甾原体PG-8 A株基因相似性高达99%,不同地区分离株Eno、Gap、pdhC基因差异不大,Eno、Gap、pdhC蛋白特性稳定,抗原表位结构明显。Eno、Gap、pdhC蛋白优势抗原表位较多,pdhC抗原性最为明显,可作为体外表达、免疫防控靶标蛋白候选基因。
关键词 莱氏无胆甾原体;分离鉴定;Eno、Gap、pdhC蛋白;生物信息学
Isolation and Identification of the Sichuan Strain of Acholeplasma Laidlawii and Bioinformatics Analysis of Eno , Gap and PdhC Factors
YANG Jun1 GAO Yuan1,2# LIU Qi-Jun1 WU Rui1 SHI Mei-Mei1
PU Jing3 WANG Yu1 NIE Fu-Ping1*
Abstract The aim is to provide a basis for the in vitro expression of Acholeplasma laidlawii and the development of genetic engineering vaccines, this study isolated a strain of Acholeplasma laidlawii (designated: WQ001) for the first time from a dairy cow with mastitis on a farm in Sichuan. The genes encoding the Eno, Gap, and pdhC proteins were subjected to in vitro amplification, sequencing, phylogenetic analysis, and predictions of protein secondary structure and B-cell antigenic epitopes. The result of genetic evolution analysis showed that WQ001 isolate shares 99% genetic similarity with the Acholeplasma laidlawii PG-8 A strain. The results showed that there was no significant difference in Eno、Gap、pdhC gene among different isolates. The characteristics of Eno, Gap and pdhC proteins remained stable,with distinct antigenic epitope structures. The Eno, Gap, and pdhC proteins contain numerous dominant antigenic epitopes, with pdhC demonstrating the most prominent antigenicity, making it a candidate gene for in vitro expression and as a target protein for immune prevention and control.
Keywords Acholeplasma laidlawii; isolation and identification; Eno, Gap, pdhC protein; bioinformatics analysis
本论文由牛结节性皮肤病1+X研究室资助
基金项目:重庆市科技局项目(cstc2019jscx-gksbX0132);重庆海关科研项目(2024CQKY01,2024CQKY02)
第一作者:杨俊(1983—),男,汉族,重庆綦江人,硕士,高级兽医师,主要从事动物疫病防控研究工作,E-mail: yy-qq@163.com
共同第一作者:高源(1994—),女,汉族,贵州盘县人,硕士,兽医师,主要从事传染病与寄生虫研究工作,E-mail: 1771340939@qq.com
通信作者:聂福平(1981—),女,汉族,重庆人,博士,正高级兽医师,主要从事动物传染病与病原微生物研究工作,E-mail: nie1626@163.com
1. 重庆海关技术中心/国家牛病检测重点实验室(重庆) 重庆 400020
2. 四川省达州市大竹县农产品质量安全监督检验检测站 达州 635100
3. 中国海关科学技术研究中心 北京 100000
1. Chongqing Customs Technology Center/State Key Laboratory of Cattle Diseases Detection (Chongqing) of Customs, Chongqing 400020
2. Dazhu County Agricultural Product Quality and Safety Supervision, Inspection and Testing Station, Dazhou 635100
3. Science and Technology Research Center of China Customs, Beijing 100000
莱氏无胆甾原体(Acholeplasma laidlawii,A. laidlawii),属支原体目(Orderl Myeoplasmatales),无胆甾原体科(Familyl Myeoplasmataeeae),无胆甾原体属(Acholeplasma)的一种无细胞壁的原核微生物[1],是细胞培养过程中常见的污染物之一,在临床上主要会引起牛乳房炎、生殖道炎症、流产或不孕等多种疾病,对养牛业的发展产生不利的影响[2-5]。该病原最早由Edward D G等[6-7]从污水中分离得到,并成为在培养基上成功培养的支原体之一,随后在多个国家被分离到。我国于2002年在陕北地区一患流行性阴道子宫内膜炎的驴生殖道分泌物中分离到一株莱氏无胆甾原体[8]。莱氏无胆甾原体基因组全长1496992 bp,GC含量 31.9%,有1491个基因序列,其中有1363个是假定编码序列(CDSs)[9]。据国外研究报道莱氏无胆甾原体具有烯醇化酶(Eno)、甘油醛-3-磷酸脱氢酶(Gap)、二氢硫辛酰基乙酰基转基酶(pdhC)等基因[10]。Eno、Gap基因存在于甾原体表面,具有加强黏附宿主的能力,是研究莱氏无胆甾原体致病性、基因工程疫苗、诊断试剂的重要靶蛋白[11]。pdhC基因存在于无胆甾原体的外膜上,是原发性胆汁性肝硬化抗线粒体抗体(Antimitochondrial Antibodies,AMA)的抗原,是重要的免疫抗原蛋白[12]。
本研究旨在对采自四川某牛场疑似支原体乳房炎奶牛的乳汁进行分离鉴定,并对分离株的Eno、Gap、pdhC蛋白基因进行扩增、测序、遗传进化分析及氨基酸序列推导,通过生物信息学分析,预测这3种蛋白的体外表达可行性、蛋白应用可行性及致病性等,为进一步研究奠定基础。
1 材料与方法
1.1 材料与试剂
患有乳房炎的奶牛乳汁,采自四川自贡市某奶牛场;精氨酸支原体培养基购自杭州百思生物技术有限公司;支原体液体培养基购自北京路桥技术股份有限公司;细菌基因组DNA提取试剂盒、DNA PCR Kit Ver 3.0 胶回收试剂盒、rTaq酶购自宝生生物工程(大连)有限公司;16S rRNA通用引物由生工生物工程(上海)股份有限公司合成;克林霉素、土霉素、卡那霉素等购自重庆色谱科技有限公司。
1.2 仪器与设备
ESCO AC2-4S1生物安全柜(新加坡艺思高科技有限公司);INB 500恒温培养箱(德国美墨尔特公司);高速冷冻离心机(Sigma公司);正置显微镜(奥林巴斯公司);普通PCR仪(ABI 公司);GelDoc-XR凝胶成像仪(美国BIO-Rad公司)。
1.3 分离培养
用0.45 μm滤器过滤乳样,取0.5 mL滤液接种于支原体液体培养基,37℃培养箱中培养5~7 d,待液体出现橙黄色时,取其液体划线接种支原体固体培养基,37℃培养,培养4 d后,在40倍显微镜下逐日观察菌落形态,出现典型“油煎蛋”样菌落时,染色镜检,挑单个菌落接种支原体液体培养基,将液体培养物存于-20℃备用。
1.4 生化特性试验
根据《伯杰氏鉴定细菌学手册》(第九版)中规定,选择以下项目进行生化特性观察实验:葡萄糖发酵、麦芽糖发酵、乳糖发酵等,将分离获得菌株分别接种于含葡萄糖、乳糖、麦芽糖、尿素等的各类生化鉴定管,每管加入100 μL菌液。石蜡封口后,置于37℃培养箱中培养,观察其颜色变化情况。
1.5 16S rRNA的检测
用试剂盒提取分离纯化菌株的基因组DNA,根据GenBank报道的细菌16S rRNA通用引物27F:5'-AGAGTTTGATCCTGGCTCAG-3' 1492R:5'-GGTTACCTTGTTACGACTT-3'进行PCR扩增。25 μL体系:rTaq酶12 μL,上、下游引物各1 μL,DNA模板1 μL,ddH2O 10 μL,反应条件:94℃预变性5 min;94℃变性50 s;54℃退火50 s;72℃延伸50 s,共35个循环;72℃延伸10 min;4℃保存。1%琼脂糖凝胶电泳检测PCR产物,胶回收目的条带,送生工生物工程(上海)股份有限公司进行测序。
1.6 药物敏感性试验
采用CCU计数法对莱氏无胆甾原体新鲜培养液进行计数,使菌液浓度为108~109 CCU/mL。将抗生素克林霉素、土霉素、庆大霉素、卡那霉素、左氧氟沙星、嗯诺沙星、氟苯尼考,配成2 mg/mL原液,置于4℃保存备用。挑取1环菌液加入药物最终浓度为512 μg/mL、128 μg/mL、64 μg/mL、32 μg/mL、16 μg/mL、8 μg/mL、4 μg/mL、2 μg/mL、1 μg/mL的肉汤培养基中,培养板水平放置于37℃培养箱中培养,每4 h观察一次,当1 μg/mL处理孔生长的颜色变得与空白对照组的颜色相同时,试验结束。
1.7 小鼠致病性试验
昆明小白鼠30只,随机分为6组,每组5只,腹腔注射分离支原体菌液,0.3 mL/只,空白对照组注射肉汤培养基,0.3 mL/只。连续观察20 d并记录。
1.8 生物信息学分析
根据GenBank已登录的Eno、Gap、phdC全基因序列,进行比对分析并分别设计引物,引物序列见表1。在25 μL体系中:rTaq酶12 μL,上、下游引物各1 μL,DNA模板1 μL,ddH2O 10 μL,按照94℃预变性5 min;94℃变性50 s;退火60 s;72℃延伸50 s,35个循环后72℃延伸10 min。1%琼脂糖凝胶电泳检测PCR产物,其胶回收产物送宝生生物工程(大连)有限公司进行测序。测序结果采用DNAStar、MEGA5.0、ProtParam等软件进行分析。
2 结果与分析
2.1 病原分离与形态观察
经过液体和固体培养基上连续2次分离培养,从患病奶牛乳汁中获得一株甾原体纯培养物,命名为WQ001。WQ001纯化菌落在显微镜100×视野下呈现典型的“煎蛋样”菌落,核心较厚,有棕黄色中心突起,边缘为一层薄薄的透明区(图1)。莱氏无胆甾原体革兰氏染色时均不易着色(图2);用吉姆萨染色法着色良好,显微镜下观察呈蓝紫色,形态特征为小球状,其直径为200~400 nm,如图3所示。
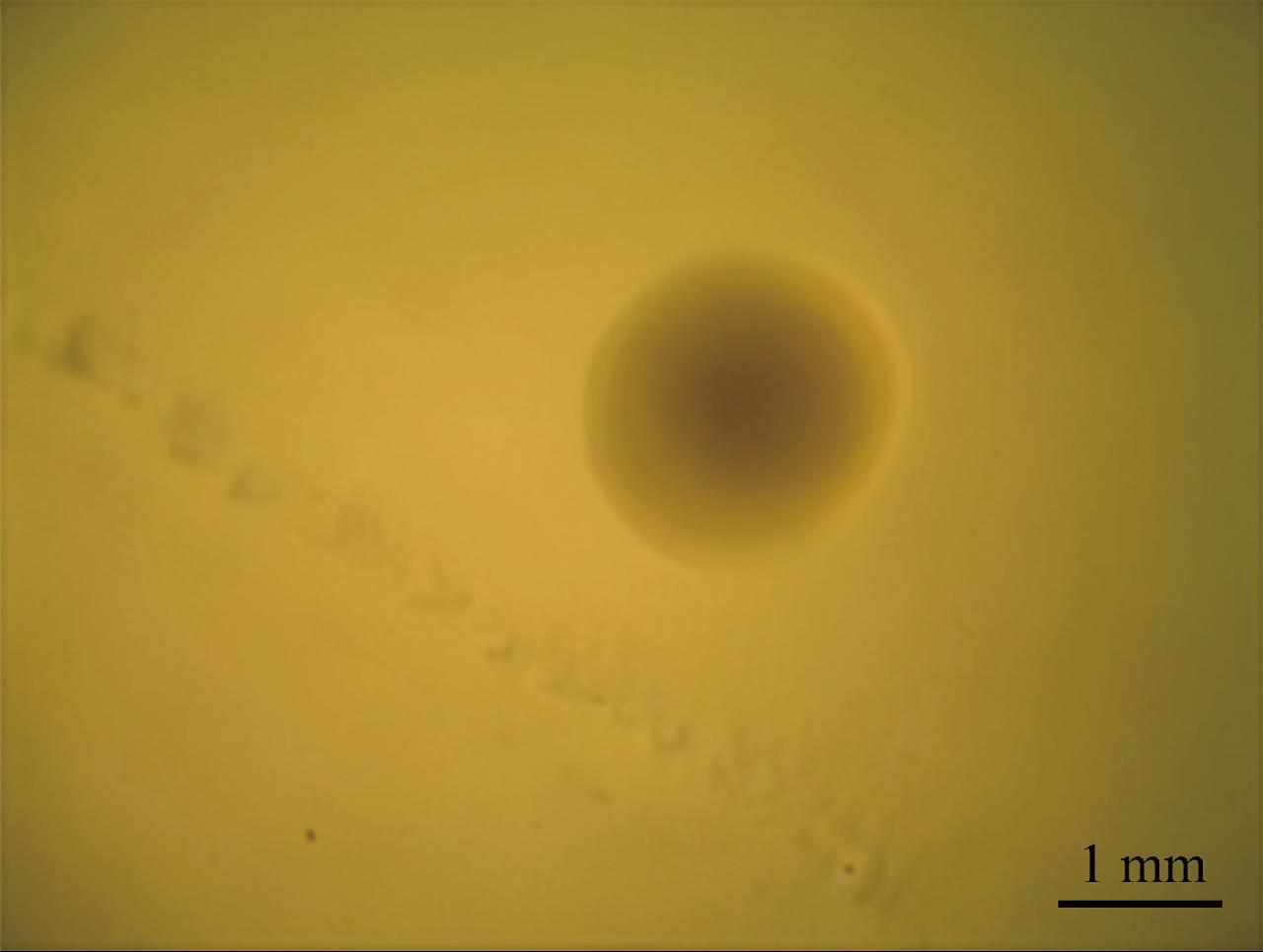
图1 固体培养基上的菌落形态
Fig.1 Colony morphology on solid medium
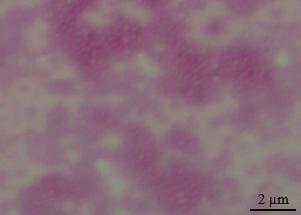
图2 革兰氏染色
Fig.2 Gram staining
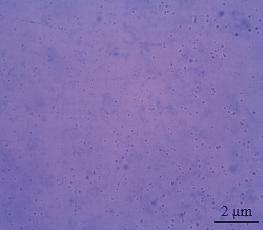
图3 吉姆萨染色
Fig.3 Giemsa staining
2.2 生化试验结果
WQ001培养物能发酵葡萄糖、精氨酸、麦芽糖、尿素等,不能发酵蔗糖、乳糖和枸橼酸盐,见表2。
表2 WQ001菌株生化试验结果
Table 2 Biochemical test results of WQ001
菌株 | 葡萄糖 | 麦芽糖 | 甘糖 | 蔗糖 | 乳糖 | 枸橼酸盐 | 精氨酸 | 尿素 |
WQ001 | + | + | + | - | - | - | + | + |
注: “+”表示阳性; “-”表示阴性.
2.3 16S rRNA基因序列的同源性比较和进化树分析
用16S rRNA引物从WQ001株基因组中扩增得到1413 bp片段,经BLAST比对发现该分离株与莱氏无胆甾原体PG-8A株(登录号:NR_074448.1)的16S基因片段相似性最高,达99.0%,与 pleciae无胆甾原体相似性达98%,与颗粒无胆甾原体和油棕植原体的相似性为97%,采用MEGA5.0软件,用N.J法建立系统发育树。该分离株与莱氏无胆甾原体PG-8A株聚在同一分枝上(图4)。
2.4 药敏试验结果
经测定,WQ001在37℃培养箱中静置培养2~3 d的菌液,浓度为109 CCU/mL。药敏试验结果显示,该分离株对左氧氟沙星、恩诺沙星、克林霉素、庆大霉素敏感性较高,对土霉素、卡那霉素、林可霉素有较低敏感性,结果见表3。
2.5 动物实验结果
实验组小鼠在通过腹腔攻毒莱氏无胆甾原体后,未出现异常。进行剖检之后,各组织器官也未出现眼观病变。
2.6 Eno、Gap、pdhC基因生物信息学分析结果
2.6.1 目的基因扩增结果
将WQ001基因组DNA,分别进行Eno、Gap、pdhC基因的PCR扩增,PCR产物经1%琼脂糖凝胶电泳,分别出现了长度约2200 bp、1123 bp、1649 bp大小的目的条带,如图5所示,与预期结果一致。
2.6.2 同源分析和系统进化分析
(1)Eno基因的同源分析。将PCR产物胶回收后测序全长2185 bp,其中包括一个长度为472个核苷酸的5'非编码区序列,一个编码432个氨基酸的开放阅读框、终止密码子和一个长度为457个核苷酸的3'非编码区,编码区核苷酸长度为1296 bp;Eno基因序列与PG-8A株莱氏无胆甾原体Eno基因的同源性高达99%,有6个突变位点(图6);将序列翻译为氨基酸再与PG-8A菌株Eno基因编码的蛋白进行比对,存在3个氨基酸突变位点(图7)。利用编码的氨基酸与在NCBI上执行BLAST(Nucleotide-protein)搜索基因同源序列,摘录同源基因编码的氨基酸序列有:莱氏无胆甾原体Acholeplasma laidlawii(WP-012242354.1)、颗粒无胆甾原体Acholeplasma granularum(WP-025724591.1)、目无胆甾原体Acholeplasma oculi(WP_045749564.1)、马无胆甾原体Acholeplasma hippikon(WP_035369272.1)、马胎无胆甾原体Acholeplasma equifetale(WP_026400137.1)、不黄无胆甾原体Acholeplasma axanthum(WP_026389947.1)、棕榈无胆甾原体Acholeplasma palmae(WP_026660709.1)、甘蓝无胆甾原体Acholeplasma brassicae(WP_030004922.1)。试验所得Eno基因所编码的蛋白与其他旁氏同源Eno所编码的蛋白进行比较,与莱氏无胆甾原体相似性高达99%,与颗粒无胆甾原体相似性为96%,与目无胆甾原体、马无胆甾原体、马胎无胆甾原体、不黄无胆甾原体、棕榈无胆甾原体和甘蓝无胆甾原体的相似性分别为89%、88%、84%、86%、84%和77%。利用DNAman软件构建进化树,如图8所示。由图8可知,分离菌株与莱氏无胆甾原体(Acholeplasma laidlawii)同属进化树的同一分支,亲缘关系最近,与其他标准菌株的亲缘关系较远。
(2)Gap基因的同源分析和系统进化分析。将PCR产物胶回收测序全长1123 bp,其中包括一个长度为89个核苷酸的5'非编码区序列,一个编码337个氨基酸的开放阅读框、终止密码子和一个长度为20个核苷酸的3'非编码区,编码区核苷酸长度为1014 bp;Gap基因序列与PG-8A株莱氏无胆甾原体Gap基因的同源性高达99%以上,有5个突变位点(图9);将序列翻译为氨基酸再与PG-8A菌株GAP基因编码的蛋白进行比对,存在1个氨基酸突变位点(图10)。利用编码的氨基酸与在NCBI上执行BLAST搜索基因同源序列,摘录同源基因编码的氨基酸序列有:莱氏无胆甾原体Acholeplasma laidlawii PG-8A(ABX81775.1)、颗粒无胆甾原体Acholeplasma granularum(WP_025725461.1)、目无胆甾原体Acholeplasma oculi(WP_045748945.1)、马无胆甾原体Acholeplasma hippikon(WP_035369990.1)、马胎无胆甾原体Acholeplasma equifetale(WP_026399917.1)、不黄无胆甾原体Acholeplasma axanthum(WP_026390926.1)、棕榈无胆甾原体Acholeplasma palmae(WP_026655613.1)、中度无胆甾原体Acholeplasma modicum(WP_026392140.1)、甘蓝无胆甾原体Acholeplasma brassicae(WP_030005226.1)。实验所得Gap基因所编码的蛋白与其他旁系同源Gap所编码的蛋白进行比较,与莱氏无胆甾原体PG-8A株的相似性高达99%以上,与颗粒无胆甾原体相似性为94%,与目无胆甾原体、马无胆甾原体、马胎无胆甾原体、棕榈无胆甾原体、中度无胆甾原体、不黄无胆甾原体和甘蓝无胆甾原体的相似性分别为91%、84%、82%、77%、76%和71%。利用DNAman软件构建进化树如图11所示。由图11可知,分离菌株与莱氏无胆甾原体PG-8A株同属进化树的同一分支,亲缘关系最近,与其他标准菌株的亲缘关系较远。
(3)pdhC基因的同源分析和系统进化分析。将PCR产物胶回收测序全长1649 bp,其中包括一个长度为14个核苷酸的5'非编码区序列,一个编码544个氨基酸的开放阅读框和终止密码子,编码区核苷酸长度为1635 bp;PdhC基因与PG-8A株莱氏无胆甾原体的同源性高达99%,有14个突变位点(图12);将序列翻译为氨基酸再与PG-8A株PdhC基因编码的蛋白比对,有4个氨基酸突变位点(图13)。利用编码的氨基酸与在NCBI上执行BLAST搜索基因同源序列,摘录同源基因编码的氨基酸序列分别来自:莱氏无胆甾原体Acholeplasma laidlawiiPG-8A(ABX81905.1)、颗粒无胆甾原体Acholeplasma granularum(WP_035357623.1)、目无胆甾原体Acholeplasma oculi丙酮酸的(CDR30165.1),目无胆甾原体Acholeplasma oculi(WP_045749958.1)、马无胆甾原体Acholeplasma hippikon(WP_035370119.1)、马胎无胆甾原体Acholeplasma equifetale(WP_026400236.1)、不黄无胆甾原体Acholeplasma axanthum(WP_052590007.1)、中度无胆甾原体Acholeplasma modicum(WP_026391537.1)、棕榈无胆甾原体Acholeplasma palmae(WP_045959892.1)。实验所得pdhC基因所编码的蛋白与其它旁氏同源pdhC所编码的蛋白进行比较,与莱氏无胆甾原体PG-8A株相似性高达99%,与颗粒无胆甾原体相似性为88%,与目无胆甾原体、马无胆甾原体、马胎无胆甾原体、棕榈无胆甾原体、不黄无胆甾原体和中度无胆甾原体的相似性分别为76%、74%、67%、60%和58%。利用DNAman软件构建进化树见图14。由图14可知,分离菌株与莱氏无胆甾原体PG-8A株同属进化树的同一分支,亲缘关系最近,与其他标准菌株的亲缘关系较远。
2.6.3 蛋白二级结构和抗原表位预测
(1)Eno蛋白二级结构和抗原表位预测。利用在线软件PPOPEN等预测Eno蛋白二级结构,其多肽链二级结构的3种类型分别是α-螺旋、β-折叠和无规则卷曲,比例分别是40.84%、12.99%和46.17%,以无规则卷曲为主,β-折叠较少;而其溶剂可及性分别是暴露37.12%、埋藏54.99%以及中间7.89%,因此,Eno氨基酸残基主要是埋藏的,也证明其具有疏水性。分析Eno蛋白的三级结构可知,其主要以无规则卷曲和转角散在存在,充分与周围的极性环境相接触,为抗原表位的形成提供有利条件(图15)。预测Eno蛋白共有14个表面可及性程度高的肽段,其中有4个肽段的表面可及性程度最高;24个具有抗原性的肽段,且抗原性的强弱不同,其中有6个肽段的抗原性最强;19条线性B细胞表位,其中2号、3号、6号、8号、11号、14号、15号、18号和19号肽段的氨基酸均小于7个,不符合B细胞表位的要求(图16)。综合上述预测结果,经Eno蛋白的B细胞表位预测,提示WQ001株的Eno蛋白优势抗原表位结构较少,预测其抗原性可能较低。
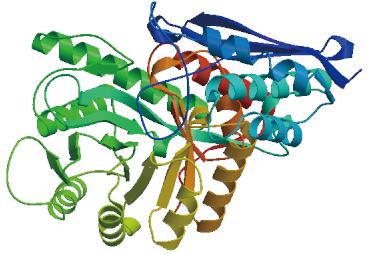
图15 Eno三级结构模型预测
Fig.15 Tertiary structure prediction model of Eno
(2)Gap蛋白二级结和抗原表位预测。预测Gap蛋白多肽链二级结构的3种类型分别是α-螺旋、β-折叠和无规则卷曲,比例分别是26.41%、 24.33%和49.26%,以无规则卷曲为主,β-折叠较少;而其溶剂可及性分别是暴露31.75%、埋藏60.83%以及中间7.42%,因此,Gap氨基酸残基主要是埋藏的,提示其具有疏水性。分析Gap蛋白的三级结构可知,其主要以无规则卷曲和转角散在存在,充分与周围的极性环境相接触,为抗原表位的形成提供有利条件(图17)共有12个表面可及性程度高的肽段,其中有9个肽段的表面可及性程度最高;22个具有抗原性的肽段,且抗原性的强弱不同,其中有10个肽段的抗原性最强;21条线性B细胞表位,其中1号、4号、5号、6号、8号、9号、10号、12号、14号、15号、16号,17号、19号、20号和21号肽段的氨基酸均小于7个,不符合B细胞表位的要求(图18)。综合上述预测结果,最终确定Gap蛋白的B细胞表位,说明,WQ001株的Gap蛋白优势抗原表位结构并不多,预测其抗原性不明显。
(3)pdhC蛋白二级结和抗原表位预测。预测pdhC蛋白多肽链二级结构的3种类型分别是α-螺旋、β-折叠和无规则卷曲,比例分别是20.77%、19.30%和59.93%,以无规则卷曲为主,β-折叠较少;而其溶剂可及性分别是暴露41.73%、埋藏48.35%以及中间9.93%,因此,pdhC氨基酸残基主要是埋藏的,也证明其具有疏水性。分析pdhC蛋白的三级结构可知,其主要以无规则卷曲和转角散在存在,充分与周围的极性环境相接触,为抗原表位的形成提供有利条件(图19)。共有29个表面可及性程度高的肽段,其中有16个肽段的表面可及性程度最高;30个具有抗原性的肽段,且抗原性的强弱不同,其中有17个肽段的抗原性最强;29条线性B细胞表位,其中3号、4号、5号、8号、13号、15号、20号和23号肽段的氨基酸大于7个,符合B细胞表位的要求(图20)。综合上述预测结果,最终确定pdhC蛋白的B细胞表位,说明WQ001株的pdhC蛋白优势抗原表位结构较多,其抗原性较明显,可作为体外表达、免疫防控靶标蛋白的候选基因。
3 讨论
莱氏无胆甾原体要发挥其致病作用,必须能够在宿主体内进行繁殖,而要进入宿主体内,黏附宿主是前提,如果支原体失去黏附素,则其致病作用也将消失[13-15]。而黏附素是一种暴露在支原体膜上的蛋白质,也具有重要的免疫原性[16]。支原体在黏附宿主后也能产生许多有毒的物质如超氧自由基、代谢产物、溶细胞酶等[17]。杜海霞等[18]发现猪肺炎支原体可以通过p97蛋白黏附于宿主呼吸道纤毛表面,然后通过蚕食纤毛使其大面积脱落无法排出异物,同时在气管黏膜上产生大量的分泌物质,分泌物质的长期积累而逐渐形成肺部实质性病变,最后导致动物出现呼吸系统疾病的症状。莱氏无胆甾原体中的膜结合磷脂酶可催化宿主细胞磷脂的水解,从而干扰宿主细胞的信号级联途径,并产生溶血磷脂破坏细胞膜的完整性[19-20]。
Eno、Gap基因存在于甾原体表面,具有增强黏附宿主的能力。pdhC基因存在于无胆甾原体的外膜上,是原发性胆汁性肝硬化抗线粒体抗体(AMA)的抗原,是重要的抗原蛋白。据国外报道莱氏无胆甾原体的Eno、Gap、pdhC为毒力基因,且Eno、Gap还是黏附因子。因此,本研究对分离株莱氏无胆甾原体进行Eno、Gap、pdhC基因检测,结果表明存在Eno、Gap、pdhC基因,提示分离得到的莱氏无胆甾原体具有致病性。对Eno、Gap、pdhC基因的重复序列、相似性、跨膜结构、信号肤、抗原表位进行预测,Eno蛋白、Gap蛋白、pdhC蛋白在哺乳动物、酵母细胞和埃希氏大肠杆菌中有较长的半衰期,蛋白质特性稳定,包含了螺旋、折叠和无规则卷曲,且以无规则卷曲为主,同时包含了β-折叠和α-螺旋,其中Eno蛋白分子质量约为46.5 ku,属弱疏水性酸性蛋白,有14个表面可及性程度高的肽段,24个具有抗原性的肽段和19条线性B细胞表位;Gap蛋白分子质量约为35.6 ku,属于弱亲水性碱性蛋白,12个表面可及性程度高的肽段,22个具有抗原性的肽段和21条线性B细胞表位;pdhC蛋白分子质量约为57.2 ku,属于弱亲水性碱性蛋白,有29个表面可及性程度高的肽段,30个具有抗原性的肽段和29条线性B细胞表位。研究结果表明:Eno、Gap、pdhC蛋白优势抗原表位结构较多的,预测其抗原性明显,其中pdhC蛋白优势抗原表位结构最多的,预测其抗原性最明显,可作为最优的体外表达、免疫防控靶标蛋白的优先候选基因,其体外表达产物可应用于诊断、检测方法建立,试验结果将为莱氏无胆甾原体pdhC基因工程疫苗和体外表达的应用研究提供依据。
4 结论
本研究从患乳房炎的奶牛乳汁中分离到一株疑似莱氏无胆甾原体,经菌落形态观察、生化鉴定、16S rRNA基因扩增并测序分析鉴定,结果显示,该分离株为莱氏无胆甾原体,且与莱氏无胆甾原体PG-8A株属同一分支。并对Eno、Gap、pdhC基因进行蛋白结构和抗原表位预测,为进一步研究莱氏无胆甾原体及其对奶牛致病性关系奠定了基础。
参考文献
[1] Daniel P, Nucifora, Nidhi D, et al. An Expanded Genetic Toolbox to Accelerate the Creation of Acholeplasma laidlawii Driven by Synthetic Genomes[J]. ACS Synthetic Biology, 2023, 13: 45-53.
[2] E S Medvedeva, A A Mouzykantov, V V Kostenko, et al. Adaptation to Antimicrobials and Pathogenicity in Mycoplasmas: Development of Ciprofloxacin-Resistance and Evolution of Virulence in Acholeplasma laidlawii[J]. Dokl Biochem Biophys, 2021, 501: 444-448.
[3] Gelgie A E, Desai S E, Gelalcha B D, et al. Mycoplasma bovis mastitis in dairy cattle[J]. Frontiers in Veterinary Science, 2024, 11.
[4] Pôrto R N G, Junqueira-Kipnis A P, De Oliveira Viu M A, et al. Evaluation of in vitro Activation of Bovine Endometrial and Vaginal Epithelial and Blood Mononuclear Cells to Produce Nitric Oxide in Response to Mycoplasma bovis, Mycoplasma bovigenitalium and Ureaplasma Diversum[J]. Acta Veterinaria, 2021, 71(2): 137-146.
[5] Spergser J, DeSoye P, Ruppitsch W, et al. Mycoplasma tauri sp. nov. isolated from the bovine genital Tract[J]. Systematic and Applied Microbiology, 2022, 45(1): 126292.
[6] Edward D G, Freundt E A. Proposal for Classifying Organisms Related to Mycoplasma laidlawii in a Family Sapromycetaceae, Genus Sapromyces, within the Mycoplasmatales[J]. Journal of General Microbiology, 1969, 57(3): 391-395.
[7] Low I E. Isolation of Acholeplasma laidlawii from Commercial, Serum-Free Tissue Culture Medium and Studies on Its Survival and Detection[J]. Applied Microbiology, 1974, 27(6): 1046-1052.
[8]权忠会, 张百祥, 王文科. 驴生殖道支原体的研究 I. 莱氏无胆固醇支原体的分离与鉴定[J]. 甘肃农业大学学报, 2002(3): 338-341.
[9] Lazarev V N, Levitskii S A, Basovskii Y I, et al. Complete genome and proteome of Acholeplasma laidlawii[J]. Journal of bacteriology, 2011, 193(18): 4943-53.
[10] KRAUSE D C, LEITH D K,BASEMAN J B. Reacquisition of specific proteins confers virulence in Mycoplasma pneumoniae[J]. Infect Immun, 1983, 39(2): 830-836.
[11] Barbosa M S, Sampaio B A, Spergser J, et al. Mycoplasma agalactiae Vaccines: Current Status, Hurdles, and Opportunities Due to Advances in Pathogenicity Studies[J]. Vaccines, 2024, 12(2): 156.
[12] Yang J, Aikins A O, Punzalan R, et al. S72 Diagnostic Value of Anti-Mitochondrial Antibodies (AMA), Anti-M2, Anti-sp100, and Anti-gp210 in Primary Biliary Cholangitis (PBC)[J]. American Journal of Gastroenterology, 2024, 119(10S): S54-S54.
[13] Yiwen C, Yueyue W, Lianmei Q, et al. Infection strategies of mycoplasmas: Unraveling the panoply of virulence Factors[J]. Virulence, 2021, 12(1): 788-817.
[14] Yueyue W, Feichen X, Yixuan X, et al. Pathogenicity and virulence of Mycoplasma genitalium: Unraveling Ariadne’s Thread J]. Virulence, 2022, 13(1): 1161-1183.
[15] Kuhnert P, Jores J. Mycoplasma hyopneumoniae pathogenicity: The known and the Unknown[M]. //Mycoplasmas in Swine. CABI, 2021: 73-86.
[16] Hegde S, Zimmermann M, Rosengarten R, et al. Novel role of Vpmas as major adhesins of Mycoplasma agalactiae mediating differential cell adhesion and invasion of Vpma expression Variants[J]. International Journal of Medical Microbiology, 2018, 308(2): 263-270.
[17] Yi X, Huang Y, Li X, et al. Decoding Mycoplasma Nucleases: Biological Functions and Pathogenesis[J]. Toxins, 2025, 17(5): 215.
[18] 杜海霞,刘茂军,冯志新,等.猪肺炎支原体及其他支原体黏附因子的研究进展[J].现代生物医学进展, 2012, m12(5): 984-987.
[19] Liu T, Zhang Y, Zhao H, et al. Mycoplasma hyopneumoniae inhibits the unfolded protein response to prevent host macrophage apoptosis and M2 Polarization[J]. Infection and Immunity, 2024, 92(10)92(10): e0005124.
[20] Rottem S. Interaction of Mycoplasmas With Host Cells[J]. Physiological Reviews, 2003, 83(2): 417-432.
表1 引物序列
Table 1 Primer sequence
引物名称 | 引物序列 | 产物长度 (bp) | 退火温度 (℃) |
Eno -R | 5 ' -GGAACATCATAAACATCACAAAGT-3 ' | 2200 | 52 |
Gap -R | 5 ' -TGGGGATTATGGTAAGTAAACG-3 ' | 1123 | 53 |
phdC -R | 5 ' - GACCAGTCAAAGCCAAC-3 ' | 1649 | 53 |
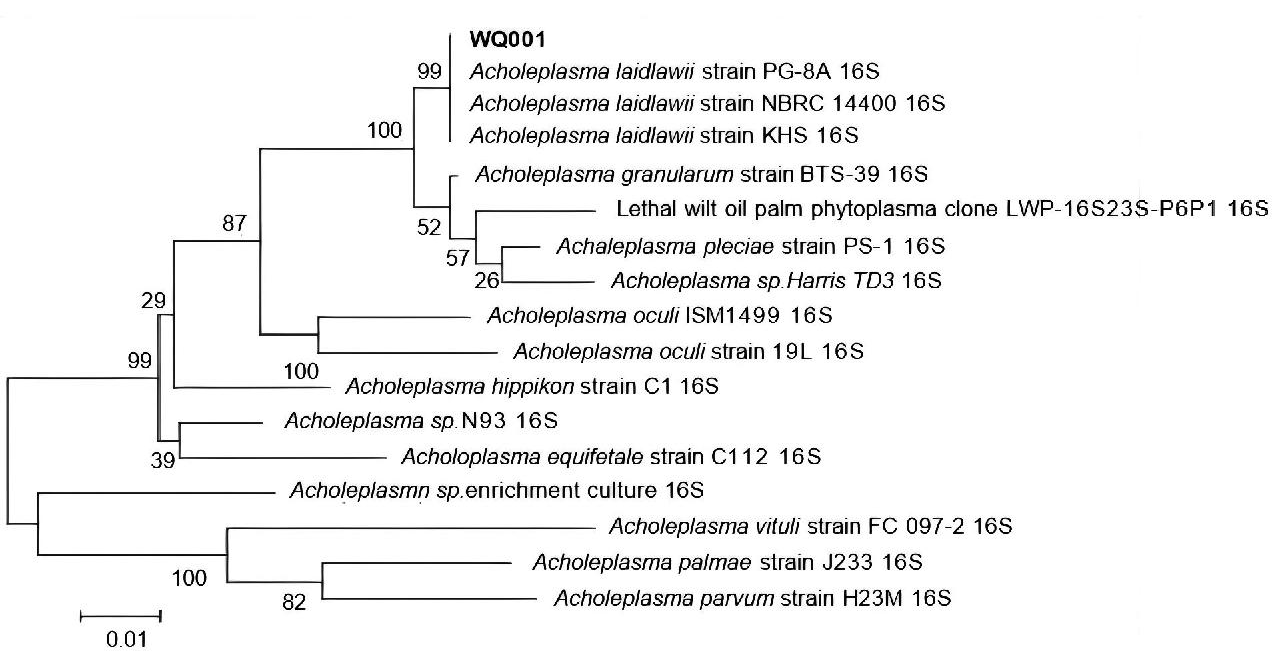
图4 WQ001菌株16SrRNA系统发育树
Fig.4 16SrRNA evolutionary tree of WQ001
表3 WQ001菌株药敏试验结果
Table 3 Susceptibility test results of WQ001
抗生素 | MIC (μg/mL) |
克林霉素 | 1 |
土霉素 | 4 |
庆大霉素 | 2 |
左氧氟沙星 | <1 |
恩诺沙星 | <1 |
卡那霉素 | 4 |
林可霉素 | 8 |
M: DL 2000 Marker; 1: Eno基因的PCR产物; 2: Gap基因的PCR产物; 3: pdhC基因的PCR产物
图5 PCR扩增产物
Fig.5 The PCR amplification product

图6 Eno目的基因ORF编码区域与PG-8A菌株
比对的突变位点
Fig.6 ORF gene coding region and PG-8A strain of mutations of Eno

图7 Eno基因编码氨基酸序列与PG-8A菌株比对的突变位点
Fig.7 Gene encoding amino acid sequence and PG-8A strain of mutations of Eno
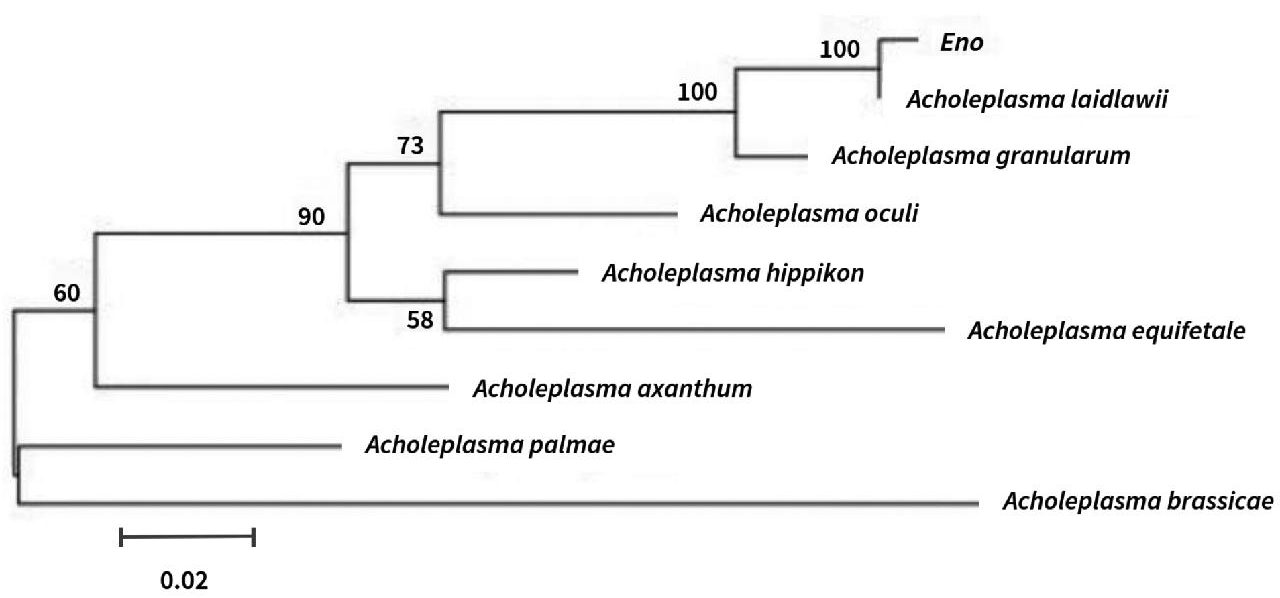
图8 Eno基因进化树
Fig.8 Genetic evolutionary tree of Eno

图9 Gap目的基因ORF编码区域与PG-8A菌株比对的突变位点
Fig.9 ORF gene coding region and PG-8A strain of mutations of Gap

图10 Gap基因编码氨基酸序列与PG-8A菌株比对的突变位点
Fig.10 Gene encoding amino acid sequence and PG-8A strain of mutations of Gap
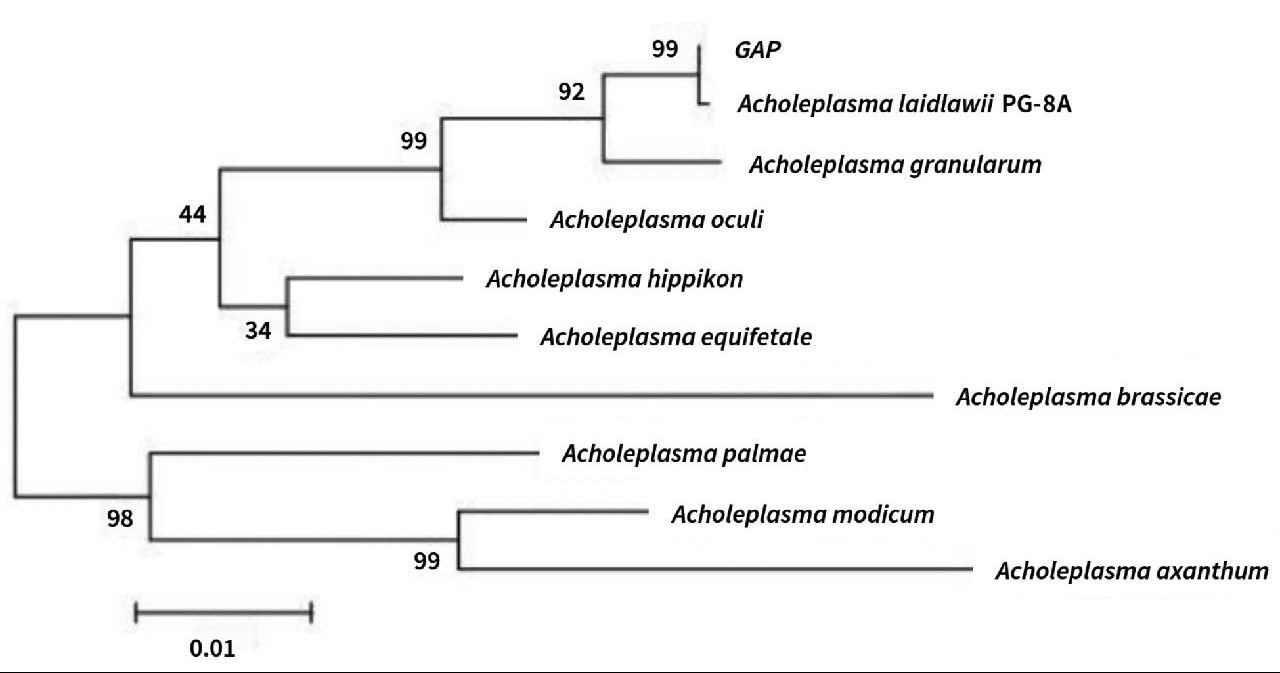
图11 Gap基因进化树
Fig.11 Genetic evolutionary tree of Gap

图12 pdhC目的基因ORF编码区域与PG-8A菌株
比对的突变位点
Fig.12 ORF gene coding region and PG-8A strain of mutations of pdhC

图13 pdhC基因编码氨基酸序列与PG-8A菌株
比对的突变位点
Fig.13 Gene encoding amino acid sequence and PG-8A strain of mutations of pdhC
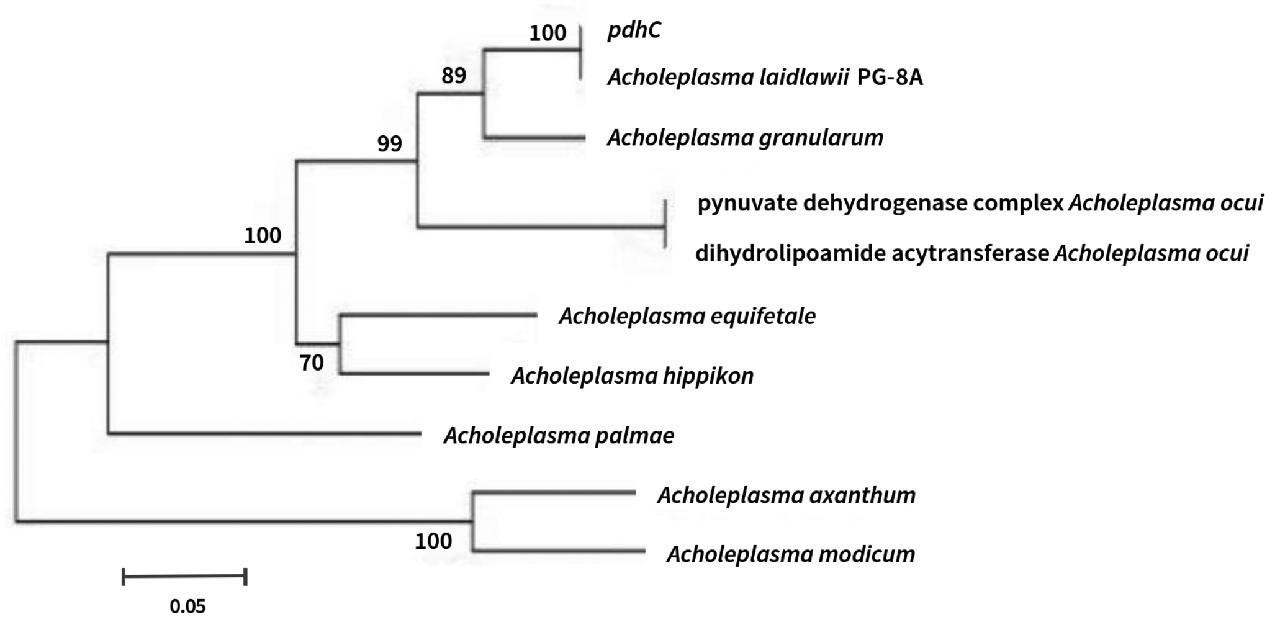
图14 pdhC基因进化树
Fig.14 Genetic evolutionary tree of pdhC
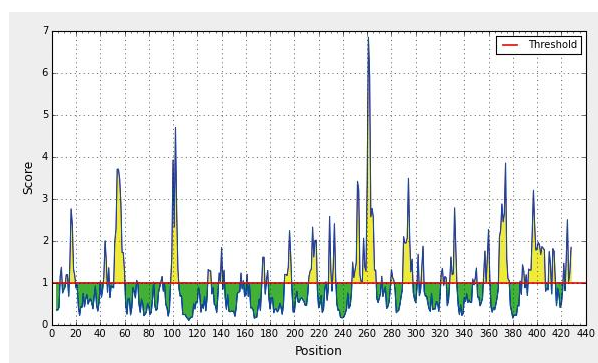
图16 Eno表面可及性预测图
Fig.16 Emini surface accessibility prediction of Eno
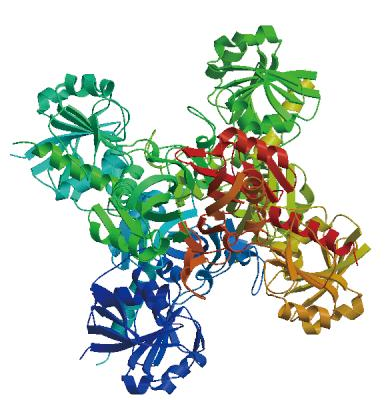
图17 Gap三级结构模型预测
Fig.17 Tertiary structure prediction model of Gap
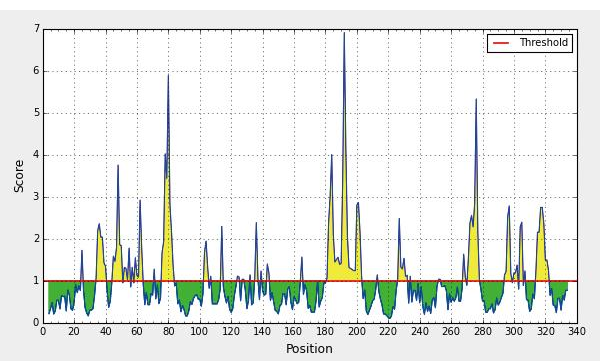
图18 Gap表面可及性预测图
Fig.18 Emini surface accessibility prediction of Gap
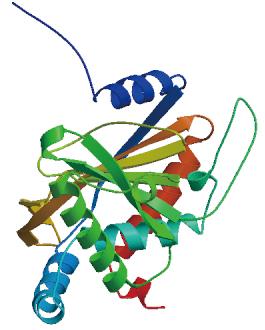
图19 pdhC三级结构模型预测
Fig.19 Tertiary structure prediction model of pdhC
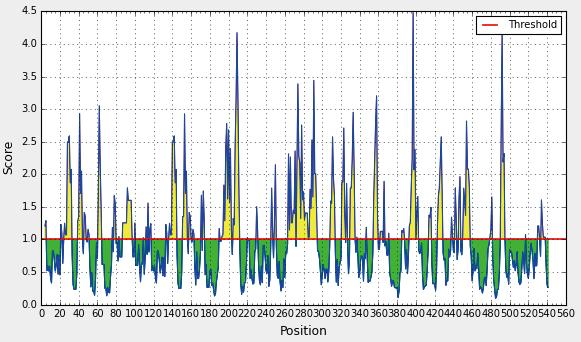
图20 pdhC表面可及性预测图
Fig.20 Emini surface accessibility prediction of pdhC







