CopyRight 2009-2020 © All Rights Reserved.版权所有: 中国海关未经授权禁止复制或建立镜像
手持式实时荧光PCR一体机快速检测猴痘病毒的应用研究
作者:任彤 赵相鹏 蒋鹏翀 韩佃刚 别玮 李小林 汪琳 邓丛良
任彤 赵相鹏 蒋鹏翀 韩佃刚 别玮 李小林 汪琳 邓丛良
任 彤 1 赵相鹏 1 蒋鹏翀 2 韩佃刚 3 别 玮 1 李小林 1 汪 琳 1 * 邓丛良 1 *
摘 要 为建立一种快速诊断猴痘病毒(Monkeypox Virus,MPXV)的检测方法,本研究制备了猴痘病毒一体化集成微流控芯片检测试剂盒,并将其与手持式实时荧光PCR一体机相结合用于猴痘病毒检测。该方法可实现样本裂解、核酸提取、核酸扩增及荧光检测的全自动操作,由此构建起基于微流控芯片平台的MPXV一体化自动检测方法。结果表明,该方法仅能对MPXV进行有效检测,与天花病毒、正痘病毒属均无交叉反应;对重组质粒标准品100 拷贝进行多次重复实验,检测结果稳定,灵敏度较高。同时,应用微流控芯片检测携带猴痘病毒标准品拭子溶液,检测结果与依据猴痘病毒检测标准的检测结果一致。本研究建立的MPXV微流控芯片一体化自动检测方法具有特异性强、灵敏度高、重复性好的优势,且操作简便、检测快速,不受实验场地限制,可广泛应用于猴痘病毒的现场即时检测。
关键词 猴痘病毒;微流控芯片;荧光RT-PCR;快速检测
Application of Portable Integrated Real-Time Fluorescent PCR Instrument in Rapid Detection of Monkeypox Virus
REN Tong1 ZHAO Xiang-Peng1 JIANG Peng-Chong2 HAN Dian-Gang3
BIE Wei1 LI Xiao-Lin1 WANG Lin1* DENG Cong-Liang1*
Abstract To establish a rapid detection method for diagnosing monkeypox virus (MPXV), an integrated microfluidic chip detection kit was established. Coupled with a handheld real-time fluorescent PCR system, the chip automatically performs sample lysis, nucleic acid extraction, amplification and detection within one closed cartridge. The assay exclusively detected MPXV without cross-reactivity to variola virus or other orthopox viruses. The limit of detection was 100 copies per reaction for recombinant plasmid standards, indicating high sensitivity. In addition, the microfluidic chip successfully identified one MPXV-positive clinical sample, and the result was concordant with that obtained using the standard MPXV detection protocol. The integrated, fully automated MPXV microfluidic-chip assay established in this study offers high specificity, sensitivity, and repeatability, while being simple to operate and rapid. Not restricted to specialized laboratories, it is ideally suited for on-site rapid detection of monkeypox virus.
Keywords Monkeypox virus (MPXV); microfluidic chip; real-time RT-PCR; rapid detection
本论文由蓝舌病1+X研究室资助
基金项目:国家重点研发计划课题(2021YFC2401005);中国海关科学技术研究中心自立课题(2024HZ11)
第一作者:任彤(1985—),女,蒙古族,山东聊城人,硕士,高级兽医师,主要从事进出口动物检验工作, E-mail: 179305203@qq.com
通信作者:邓丛良(1969—),男,汉族,山东海阳人,博士,研究员,主要从事进出口动植物检验工作, E-mail: Smile299@sohu.com
共同通信作者:汪琳(1974—),女,汉族,湖北随州人,博士,研究员,主要从事进出口动物检验工作, E-mail: 15301090661@189.cn
1. 中国海关科学技术研究中心 北京 100026
2. 北京中科生仪科技有限公司 北京 100029
3. 昆明海关技术中心 昆明 650228
1. Science and Technology Research Center of China Customs, Beijing 100026
2. Beijing Integrated BioSystems Co.,Ltd, Beijing 100029
3. Kunming Customs Technical Center, Kunming 650228
猴痘是由猴痘病毒(Monkeypox Virus,MPXV)引起的一种罕见、散发、天花样表现的人畜共患急性传染病[1-2]。1958年科学家首次在实验室发现猴子体内存在猴痘病毒[3]。这种病毒还可以感染多种鼠和兔,地松鼠是MPXV的重要宿主。1970年,在刚果民主共和国首次发现人感染MPXV的病例[4]。21世纪以来,全球多次暴发猴痘疫情。2023年9月我国宣布将猴痘纳入乙类传染病进行管理,采取乙类传染病的预防控制措施。目前,海关按规定程序对发生猴痘疫情的国家(地区)出入境人员开展采样检测并采取相应的医学措施。
猴痘病毒是正痘病毒属的一种双链DNA病毒,其外层由管状物质构成,内部为哑铃样芯髓,包含病毒DNA及若干蛋白质。病毒大小为200~250 nm,具有复杂的对称性,外观呈砖形或卵圆形。MPXV约有19万碱基对,在其基因组中检测到190余个开放阅读框(Open Reading, ORF),与其他正痘病毒核苷酸相似性超过90%,其特异性核酸序列位于5'—和3'—末端[5-6]。目前猴痘病毒诊断方法包括酶联免疫吸附法(Enzyme Linked Immuno Sorbent Assay,ELISA)、病毒分离培养、聚合酶链反应(Polymerase Chain Reaction,PCR)和基因测序技术等,在实际应用中分别具有不同的优缺点。ELISA[7-8]技术操作简便易行,结果容易判别,尤其是试纸条检测方法[9-10],操作方便快速,15 min内即可完成检测,便于基层和现场检测。但是ELISA特异性不强,和其他痘病毒容易产生交叉反应,而且其灵敏度也有待商榷,不能用于检测初感染猴痘病毒患者。猴痘病毒分离培养作为病毒鉴定检测的传统“金标准”[11],需经验丰富的技术人员在生物安全Ⅲ级实验室进行操作,对实验室生物安全要求极高,检测周期较长。高通量测序技术以其通量大、检测限低、准确性高、信息丰富等优势,广泛应用于猴痘病毒检测和研究[12-13],但其昂贵的仪器和检测成本以及对场地和技术要求较高,限制其在检测领域中的广泛应用。PCR技术作为病毒检测的常规技术,同样广泛应用于猴痘病毒检测[14-16],目前基于PCR技术陆续研发出实时荧光定量PCR技术[17-18]、液滴式数字PCR技术[19]、环介导等温扩增技术[20]、重组酶介导等温扩增-CRISPR/Cas13a结合侧流层析技术[21]检测猴痘病毒。其中,实时荧光PCR方法具有灵敏度高、特异性强的优点,是世界卫生组织(WHO)推荐的MPXV感染常规确证方法,但实时荧光PCR对检测人员、实验室环境和检测设备要求均较高,需要在专业的分子实验室内完成,在疫情突发现场、国境口岸等应急处置场景中往往难以满足快速检测要求。本研究应用手持式一体化实时荧光PCR仪及配套MPXV微流控芯片检测试剂盒,用于MPXV的检测,建立了MPXV全流程一体化全自动核酸快速检测方法,可为口岸一线和相关研究人员野外样品MPXV现场检测提供技术支撑。
1 材料与方法
1.1 材料
1.1.1 猴痘病毒阳性质控
猴痘病毒脱氧核糖核酸液体标准品(货号:BDS-IQC-373)购自广州邦德盛生物科技有限公司。
1.1.2 主要设备
手持式一体化实时荧光PCR仪(P1000,北京中科生仪科技有限公司);荧光PCR仪(ABI 7500,Thermo Fisher)。
1.2 方法
1.2.1 微流控芯片的制备及检测
手持式一体化实时荧光PCR仪及配套微流控芯片试剂盒如图1、图2所示。其中,图1为手持式一体化实时荧光PCR仪,该仪器设备为集样本处理、核酸提取纯化、实时荧光PCR检测功能于一体的全自动封闭式核酸扩增分析系统。以步进电机为试剂驱动单元,正、负压配合驱动芯片内试剂(图2)定向流动,依次实现样本裂解、核酸吸附、杂质洗涤、目的核酸洗脱、扩增试剂复溶等分子生物学过程。随后,再以半导体制冷片为核心的温度控制单元对PCR反应仓内的试剂进行温度控制循环,以实现PCR扩增反应;同时,配备5通道荧光检测单元,实时记录每个循环产生的荧光数据。最后,数据处理单元对采集到的数据进行分析并展示结果判断。
检测猴痘病毒时取患者50 μL 血液样品或拭子溶液加入微流控芯片样品通道进行检测。现场检测用3D打印拭子(图3)擦拭患者疱疹液,将拭子端部折断放进样品通道进行检测,如果是组织样品取1~2 g加入搓揉管中(图4),用手反复搓揉10~20 s后加入2滴溶液于样品通道,将芯片插入一体化实时荧光PCR检测仪内,运行反应35 min即可直接读取结果。
1.2.2 猴痘病毒检测试剂盒线性度测试
配置双重扩增体系,应用ABI 7500实时荧光PCR仪验证MPXV引物探针扩增效果。制备猴痘病毒微流控芯片检测试剂盒,将MPXV质粒标准品进行系列稀释后,直接加入微流控芯片中进行检测;同时按常规荧光RT-PCR流程进行扩增检测,评价2种方法的扩增线性度。
1.2.3 检测特异性
分别用MPXV标准样品、天花病毒、正痘病毒属病毒进行微流控芯片检测,分析检测方法的特异性。
1.2.4 检测重复性
以100拷贝的MPXV标准品加入微流控芯片中进行检测,独立重复8次,分析检测结果的重复性。
1.2.5 MPXV检测
取健康咽拭子液1000 μL,加入200 μL MPXV脱氧核糖核酸液体标准品,以不含有MPXV标准样品的健康咽拭子液作为健康对照,应用猴痘病毒微流控芯片检测试剂盒,对含有MPXV标准品拭子溶液和健康咽拭子溶液进行检测。同步依据行业标准SN/T 3487—2013《猴痘检疫技术规范》,分别取200 μL MPXV标准品拭子溶液和健康咽拭子溶液提取核酸进行实时荧光PCR检测。
2 结果与分析
2.1 MPXV引物探针扩增效果
配置双重扩增体系,验证MPXV引物探针扩增效果。将制备的MPXV阳性质粒参考品稀释至5拷贝、5×101拷贝、5×102拷贝、5×103拷贝、5×104拷贝、5×105拷贝,为横坐标;Ct值为纵坐标,绘制标准曲线。结果如图5所示,MPXV标准曲线的扩增效率为108.31%,间距为-3.14,R2 = 0.99;模板5拷贝时,ABI 7500 ΔRn≈60万。结果明确MPXV PCR扩增效率在正常范围,表明反应体系内的MPXV扩增是有效的。
2.2 MPXV微流控芯片的检测线性度
配制双重扩增体系,并制作成微流控芯片,验证手持式设备的检测线性度。将制备的MPXV阳性质粒参考品稀释至5×102 拷贝、5×103 拷贝、5×104 拷贝、5×105 拷贝、5×106 拷贝,用手持式一体化实时荧光PCR仪(图6)进行标准曲线实验。
结果显示,MPXV的检测出现典型的荧光曲线,Ct值介于17.37~31.86之间(图A),数值呈梯度递减。内标基因(Internal Positive Control,IPC)均出现典型的荧光曲线(图B),判断实验结果有效。MPXV微流控芯片的检测线性度好,R2 = 0.9960。
2.3 MPXV微流控芯片的检测特异性
在手持设备上进行试剂盒检测特异性实验,分别用1 μg人基因组、1 μg大肠杆菌基因组、1×104拷贝近缘病毒的质粒和100拷贝的MPXV质粒来进行特异性检测。图7表明4次反应IPC基因均出现典型的荧光曲线,实验结果有效。猴痘病毒阳性质粒检测出现典型的荧光曲线,检测结果显示为猴痘病毒阳性(图A);而天花病毒的质粒(图B)、人基因组(图C)和大肠杆菌基因组(图D)进行检测,均未见到扩增信号,检测结果显示为猴痘病毒阴性。
2.4 MPXV微流控芯片检测的重复性
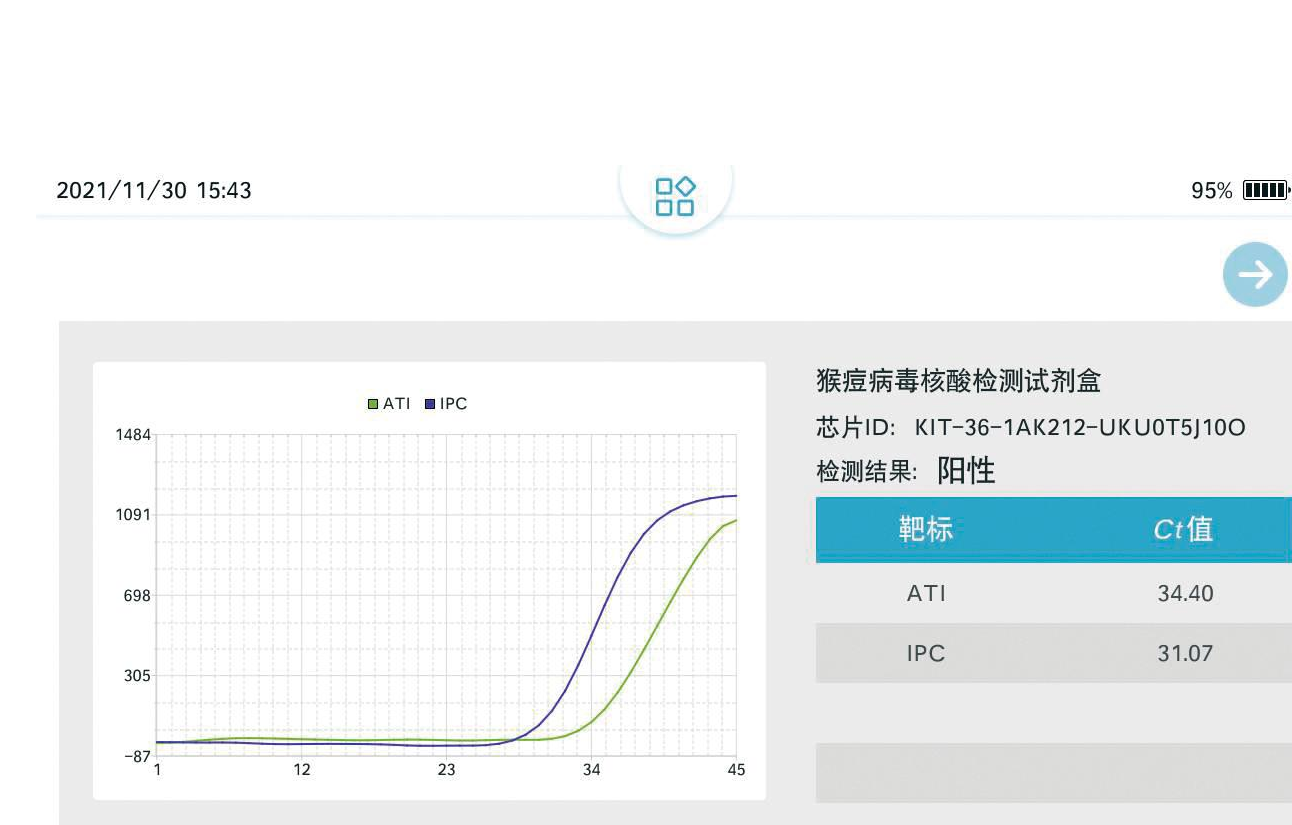
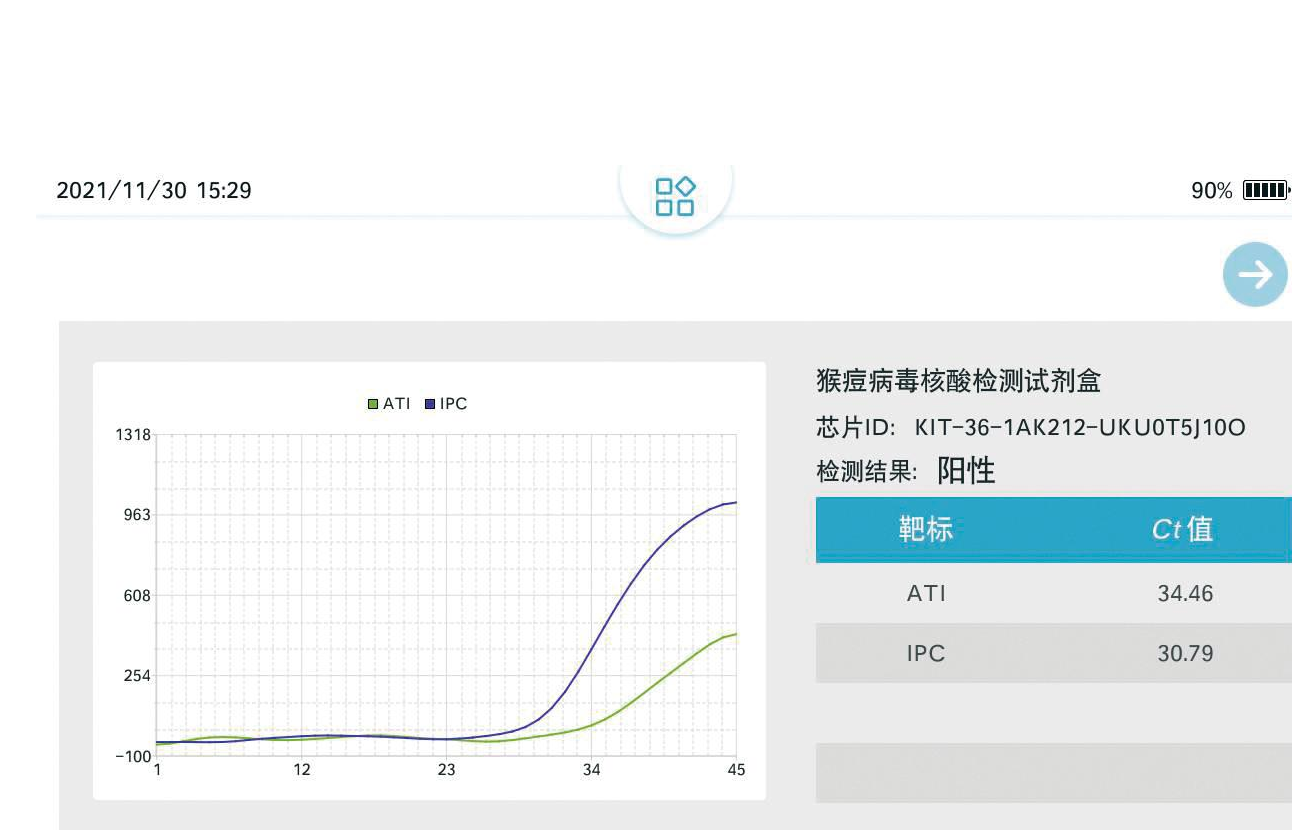
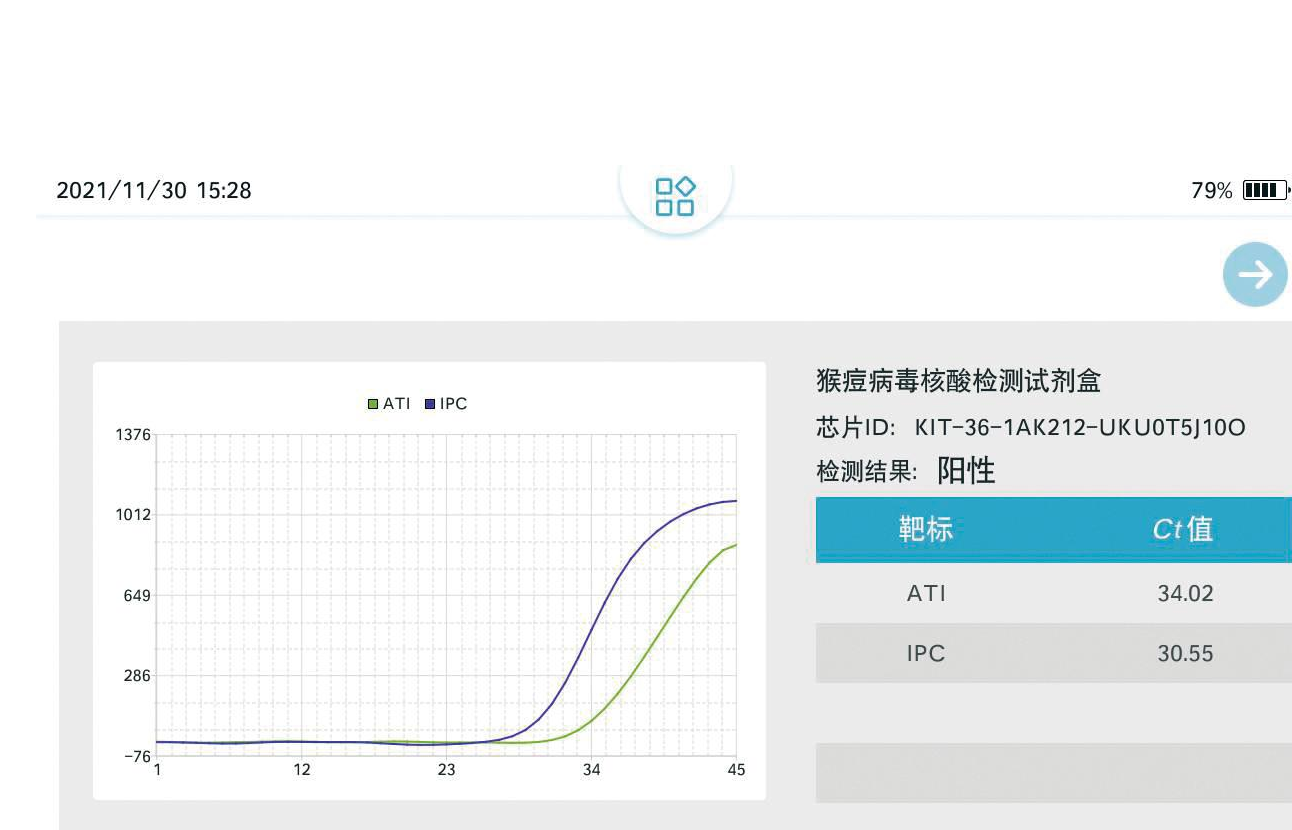
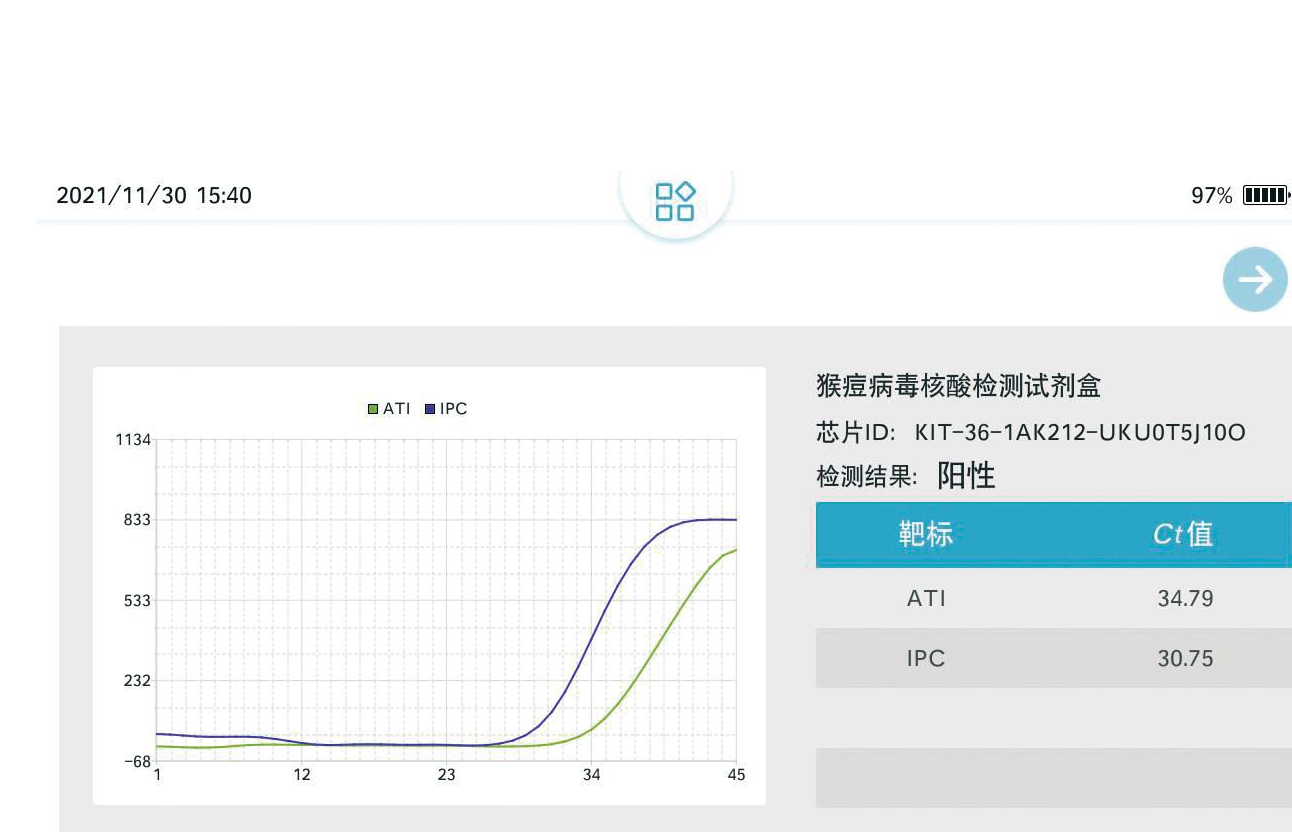
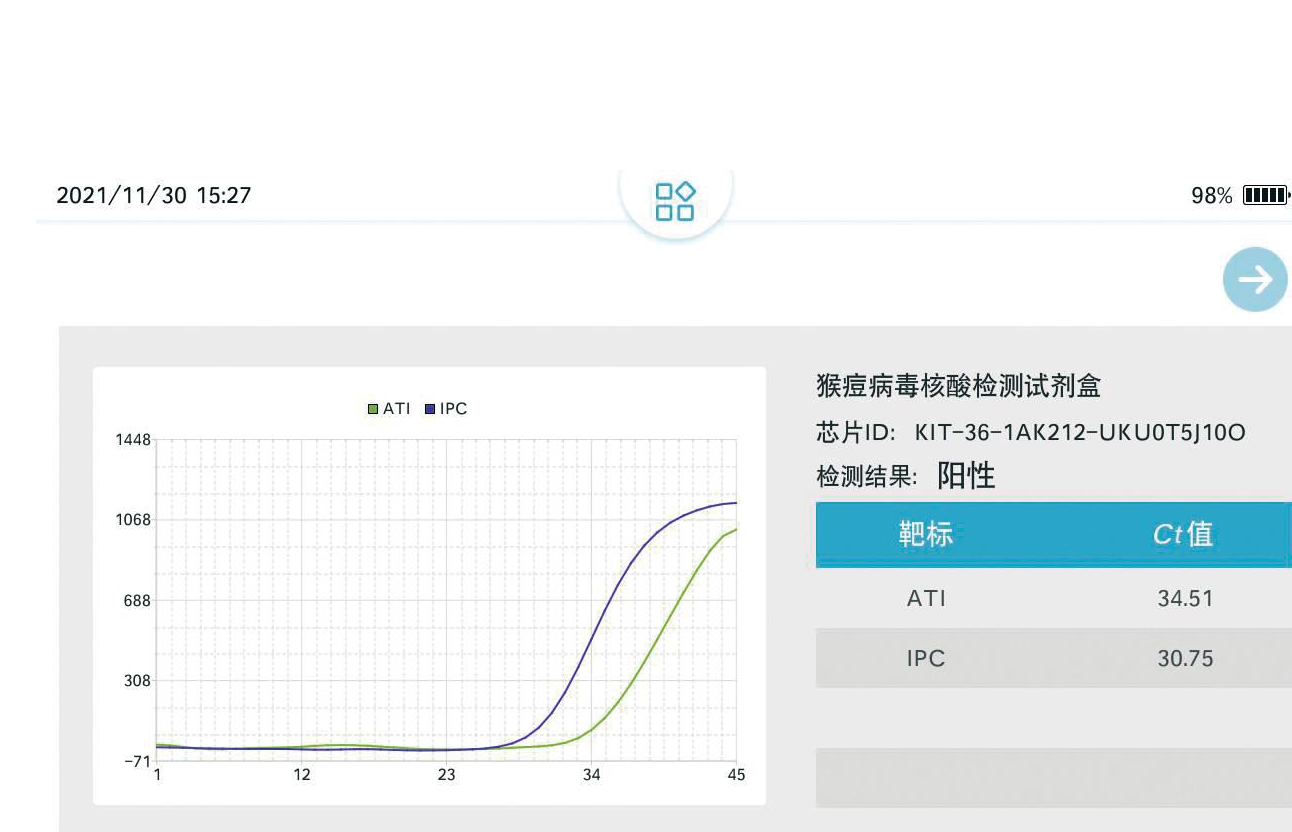
在手持设备上进行检测限测试,模板用100拷贝质粒作为检测限,在8台手持式实时荧光PCR仪器上进行8个重复(图8)。结果显示,不同批次检测之间的IPC基因和阳性质粒均有典型S型荧光曲线,表明实验结果有效。IPC基因的Ct值介于30.37~31.86之间,阳性质粒Ct值介于33.53~35.02之间,变异系数为1.30%。检测结果重复性稳定可靠。
2.5 应用微流控芯片试剂盒检测MPXV
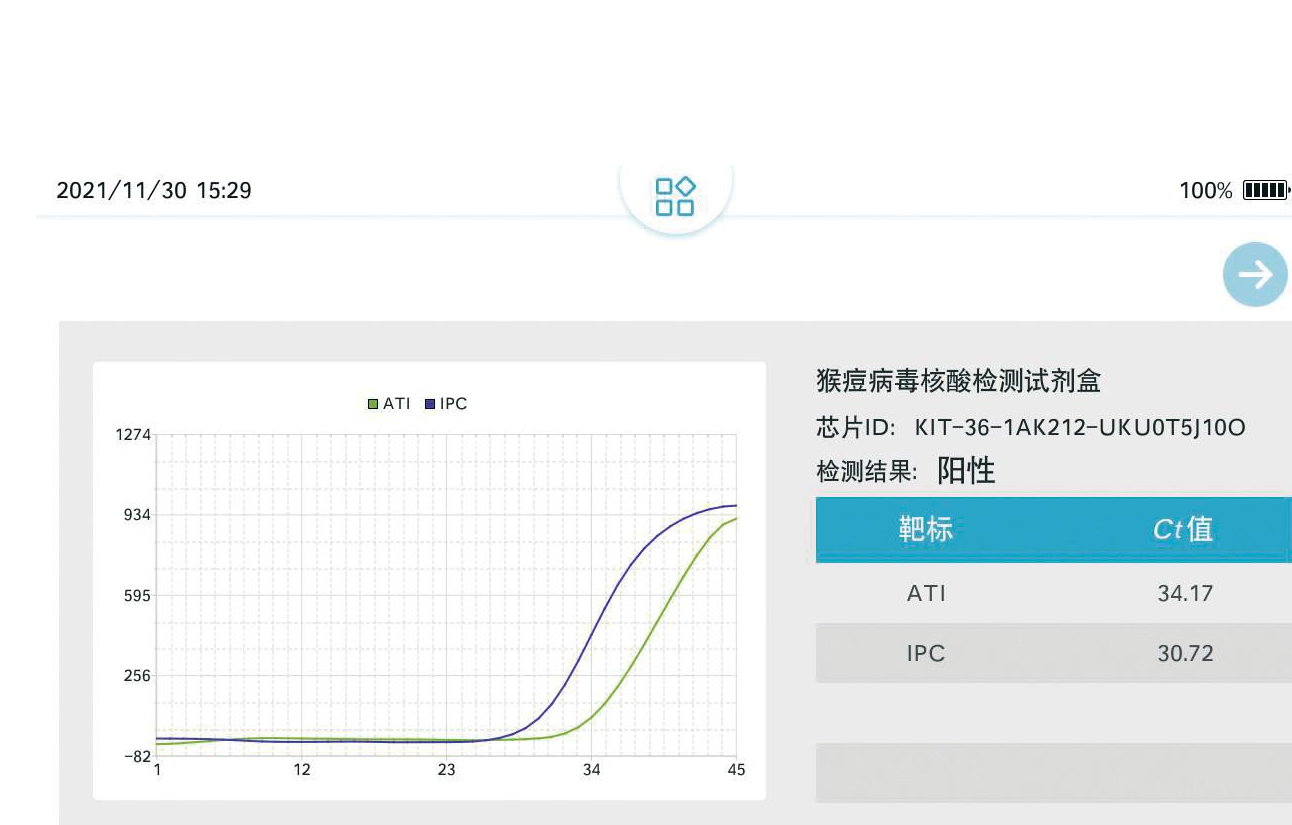
应用MPXV微流控芯片检测试剂盒,对含有MPXV标准品咽拭子溶液和健康咽拭子溶液进行检测。检测结果显示如图9所示,MPXV标准品咽拭子溶液IPC荧光Ct值为32.24,表明检测结果有效;正痘病毒属病毒Ct值为19.94,猴痘病毒Ct值为20.87,表明咽拭子溶液携带猴痘病毒(图A),检测结果与预期一致。健康咽拭子溶液(图B)IPC基因检测Ct值为29.79,实验检测结果有效;而正痘病毒属病毒核酸和猴痘病毒核酸检测均为阴性,表明健康咽拭子溶液不携带MPXV。
依据行业标准SN/T 3487—2013合成猴痘病毒检测引物和探针,检测含有MPXV标准品咽拭子溶液和健康咽拭子溶液。荧光PCR检测结果如图10所示,阳性对照出现典型的荧光曲线,而阴性对照没有出现荧光曲线,阴阳性对照成立,检测结果有效。图A咽拭子溶液MPXV没有出现荧光曲线,表明猴痘病毒核酸检测为阴性,咽拭子溶液不含猴痘病毒;而图B检测结果MPXV出现明显的荧光曲线,表明咽拭子溶液含有猴痘病毒,检测结果与应用手持式一体化实时荧光PCR一体机检测结果一致。
3 讨论
传染病的早期快速诊断,并针对传染病发生的地理环境因素和流行性风险进行及时统计和预警处置,是传染病检疫和防控工作的关键手段之一,这给传染病病原检测技术提出了精准性、即时性、现场化、信息智能化等要求。现有分子检测技术虽然可以满足精准需求,但对检测设备、环境、操作人员专业水平要求很高,难以实现现场快速检测分析。
一体化微流控芯片是一种新型技术平台,它利用微加工和注塑工艺,将不同功能单元集成在聚合物芯片上,实现独立的样品处理及核酸分离过程,同时与PCR和光学检测系统相配合,完成荧光定量PCR扩增功能[22]。一体化芯片包括微流控通道、样品处理、温度循环和光学检测等主要功能模块,对应于系统主机的微量注射泵、超声发生器、半导体加热制冷器和热电偶、LD激发光源和光学检测器件等部件相结合实现一体化无干预反应过程。芯片内预置的液体试剂和常温保存冻干试剂呈分离状态,互不干扰。本研究将微流控芯片平台和轻巧的实时荧光PCR仪相结合,建立了一体化实时荧光PCR检测猴痘病毒技术,实现“样品进—结果出”一体化全自动核酸检测,克服实时荧光PCR对实验场地和人员操作的限制,同时保持其高灵敏特异性和结果重复性。
猴痘病毒微流控芯片检测结果表明,该芯片可以特异性地检测猴痘病毒,以重组质粒为标准品确定的检测灵敏度达到100拷贝,当测试样本中为100拷贝时可得到稳定的扩增结果,不同时间和不同一体化实时荧光PCR仪器检测IPC基因和MPXV阳性对照的Ct值接近,变异系数低至1.30%,确定该微流控芯片具有良好的重复性和可靠性。应用微流控芯片检测携带MPVX和健康的咽拭子溶液,检测结果与行业标准检测结果一致,表明该方法可以应用于临床和口岸猴痘病毒的检测。
刘建礼等[22]研发的一体化全自动检测MERS微流控芯片,完成一次全流程检测仅需50 min左右,较常规实时荧光RT-PCR的2.5~3 h缩短了60%以上,检测样本中具有100拷贝可得到稳定的扩增结果,检测极限达到50拷贝,其检测灵敏度和稳定性与本研究结果一致。本研究应用升级版的一体化实时荧光PCR检测设备,全自动检测MPXV完成一次全流程检测仅需42 min,升级版的一体化实时荧光PCR检测设备个体轻巧,整机重量1 kg可以随手持有;配备锂电池,可以在无电源情况下连续工作5 h以上;其检测灵敏度和特异性与实验室传统实时荧光PCR检测结果一致,而其快速性、简便性和随地随时检测特点优于当前传统实时荧光PCR检测设备,因此该技术在野外现场和口岸一线检测领域中具有广阔的推广应用价值。
参考文献
[1] Shchelkunov S N, Totmenin A V, Babkin I V, et al. Human monkeypox and smallpox viruses: genomic comparison[J]. FEBS Letters, 2001, 509(1): 66-70.
[2] Arndt W D, Cotsmire S, Trainor K, et al. Evasion of the innate immune type I interferon system by monkeypox virus[J]. Journal of Virology, 2015, 89(20): 10489-10499.
[3] VON MAGNUSP, ANDERSENEK, PETERSEN K B et al. Apox-like disease in cynomolgus monkeys[J]. Acta Pathologica et Microbiologica Scandinavica, 1959, 46(2): 156-176.
[4] LANDNYJ ID, ZIEGLER P,KIMA E. A human infection caused by monkeypox virus in Basankusu Territory, Democtaic Republic of the Congo[J]. Bull World Health Organ,172, 46(5): 593-597.
[5] McCollum A M, Damon I K. Human monkeypox[J]. Clinical Infectious Diseases, 2014,58(2): 260-267.
[6]Petersen E, Kantele A, Koopmans M, et al. Human monkeypox: epidemiologic and clinical characteristics, diagnosis, and prevention[J]. Infectious Disease Clinics of North America, 2019,33(4): 1027-1043.
[7]任皎, 叶飞, 赵莉, 等. 猴痘病毒感染血清抗体ELISA检测方法的建立[J]. 中华实验和临床病毒学杂志, 2018, 32(6): 636-639.
[8]欧阳蕾, 吴佩璇, 师江龙, 等. 抗猴痘病毒A35R蛋白单克隆抗体的制备及双抗体夹心ELISA检测方法的建立[J]. 微生物学免疫学进展, 2024, 52(4): 1-8.
[9]Ye L, Lei X, Xu X, et al. Gold-based paper for antigen detection of monkeypox virus[J]. Analyst, 2023, 148(5): 985-994.
[10]赖祥德, 曹佩佩, 彭雅南, 等. 基于微波法快速合成胶体金建立猴痘病毒抗原免疫层析试纸条半定量方法[J]. 中国人兽共患病学报, 2023, 39(7): 617-621.
[11]WHO. Laboratory testing for the monkeypox virus: interim guidance[EB/OL]. (2022-05-23). https://www.who.int/publications/i/item/WHO-MPX laboratory-2022.1.
[12] MIAO Q, MA Y, WANG Q, et al. Microbiological diagnostic performance of metagenomic next-generation sequencing when applied to clinical practice[J]. Clinical Infectious Diseases, 2018, 67(Suppl2): 231-240.
[13]裴建新, 吴长城, 张银豪, 等. 宁夏首例猴痘病毒测序及全基因组序列特征分析[J]. 病毒学报, 2024, 40(4): 779-786.
[14]张睿 , 陈国强, 张敬友, 等. 猴痘病毒PCR检测方法的建立[J]. 中国动物检疫, 2011, 28(8): 51-53.
[15] 陈国强, 陈雷, 张敬友, 等. 猴痘病毒PCR检测试剂盒的研制及应用[J]. 畜牧与兽医, 2011, 43(10): 66-68.
[16] Ropp SL, Jin Q, Knight JC, et al. PCR strategy for identification and differentiation of small pox and other orthopoxviruses[J]. Journal of Clinical Microbiology, 1995, 33: 2069-2076.
[17]] LI Y, OLSON V A, LAUE T, et al. Detection of monkey-pox virus with real-time PCR assays[J]. Journal of Clinical Virology, 2006, 36(3): 194-203.
[18]冯俊霞, 陈锦, 崔晓虎, 等. 实时荧光定量PCR检测猴痘病毒的方法研究[J]. 遵义医科大学学报, 2024, 47(5): 508-512+521.
[19]杨国平, 周彪, 苏小建, 等. 猴痘病毒数字PCR 检测方法的建立[J]. 中国国境卫生检疫杂志, 2024, 47(4): 340-344.
[20] 许晓琳, 袁向芬, 孔玉方, 等. 猴痘病毒实时荧光LAMP 检测方法的建立[J]. 黑龙江畜牧兽医, 2024, 2: 72-78.
[21]杨宁, 马君妍, 孟子欣蓉,等. 重组酶介导等温扩增-CRISPR/ Cas13a 结合侧流层析技术快速检测猴痘病毒[J]. 中国口岸科学技术 2024, 14(3): 274-281.
[22]刘建礼, 高静, 蒋鹏翀, 等. 中东呼吸综合征冠状病毒微流控芯片自动检测方法的建立[J]. 中国公共卫生, 2023(1): 92-97.

图2 MPXV微流控芯片试剂盒
Fig.2 MPXV microfluidic chip kit

图3 3D打印拭子
Fig.3 3D printed swab

图4 搓揉管
Fig.4 Kneading tube
图1 手持式一体化实时荧光PCR仪
Fig.1 Portable integrated real-time fluorescence PCR instrument
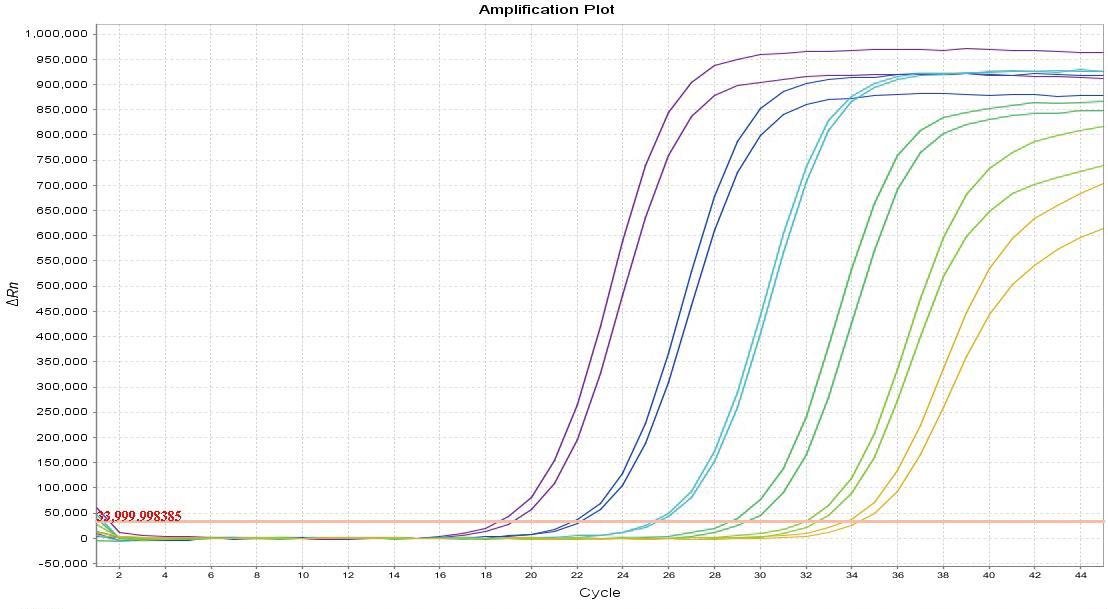
A
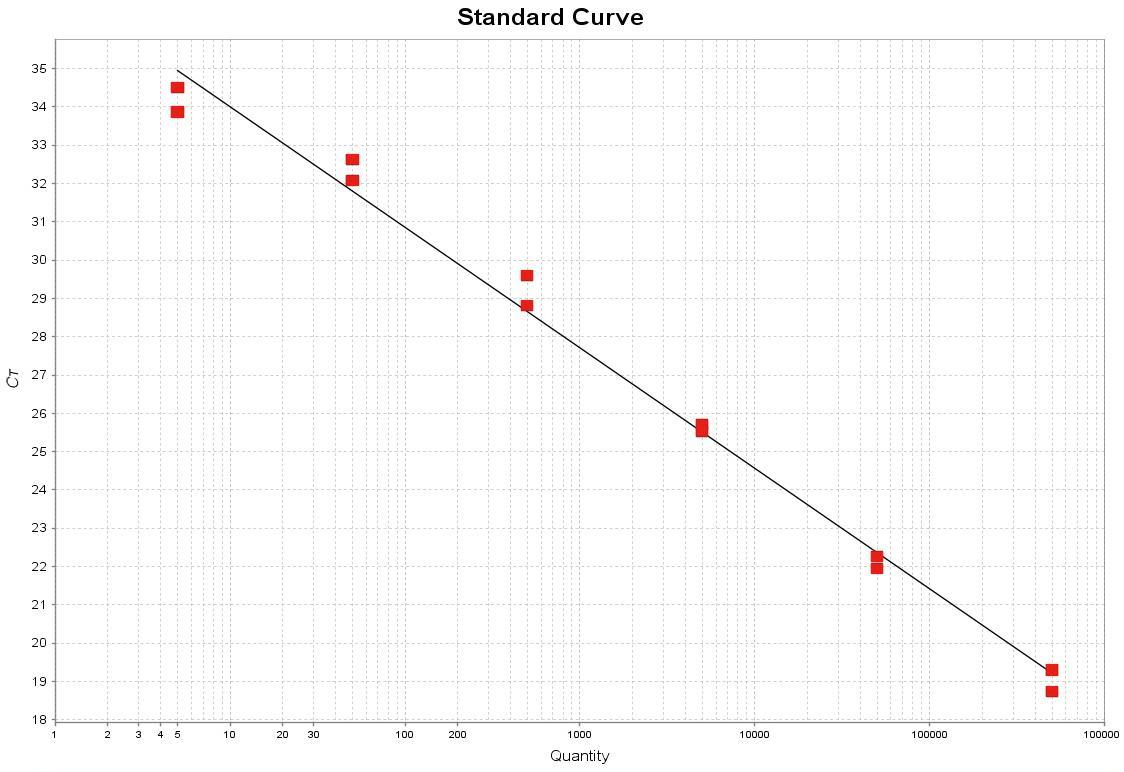
B
A: MPXV阳性质粒梯度扩增曲线; B: MPXV扩增标准曲线
图5 MPXV扩增效率
Fig.5 Amplification efficiency of MPXV
A: MPXV质粒梯度扩增曲线; B: 内标基因扩增结果
图6 MPXV质粒全流程标准曲线扩增结果
Fig.6 Full-process standard-curve amplification results of MPXV plasmid

B
A
C
D
E
F
G
H
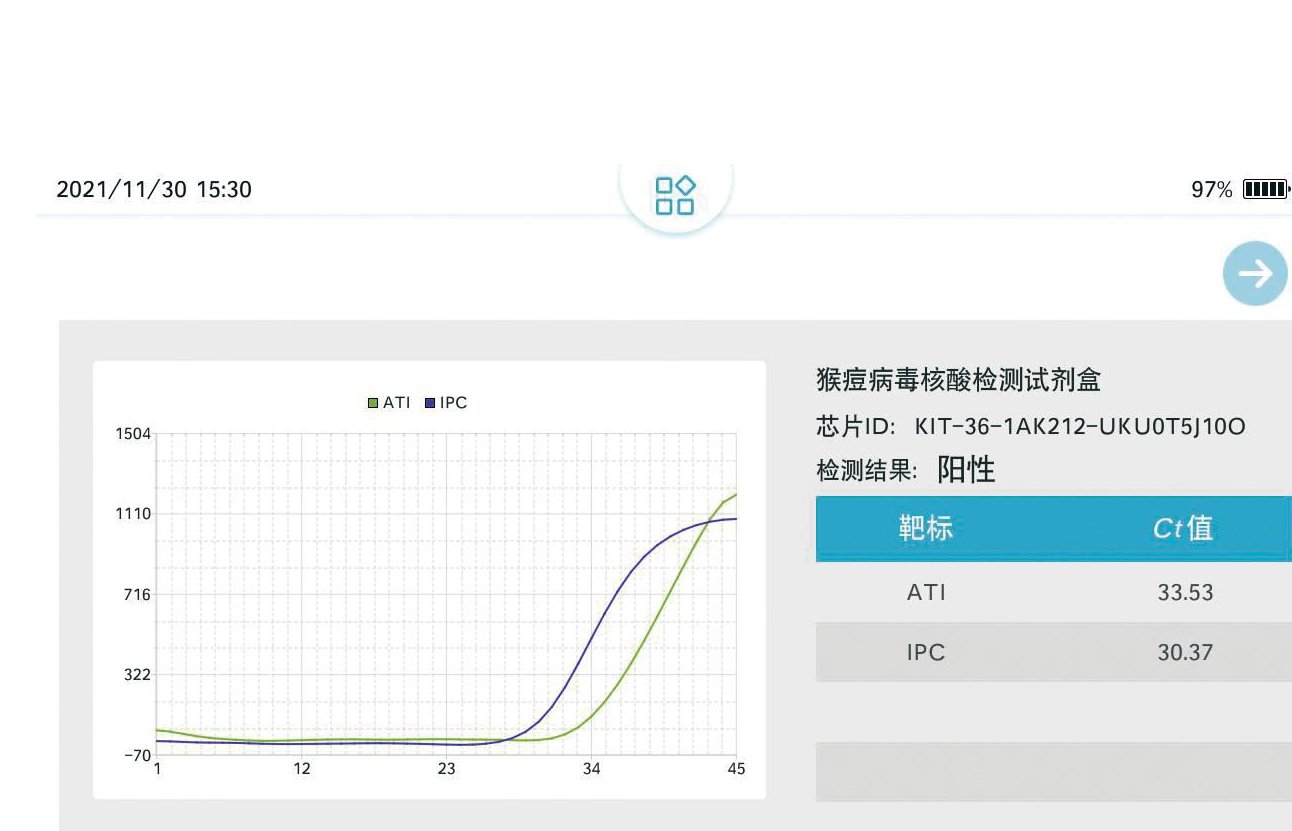
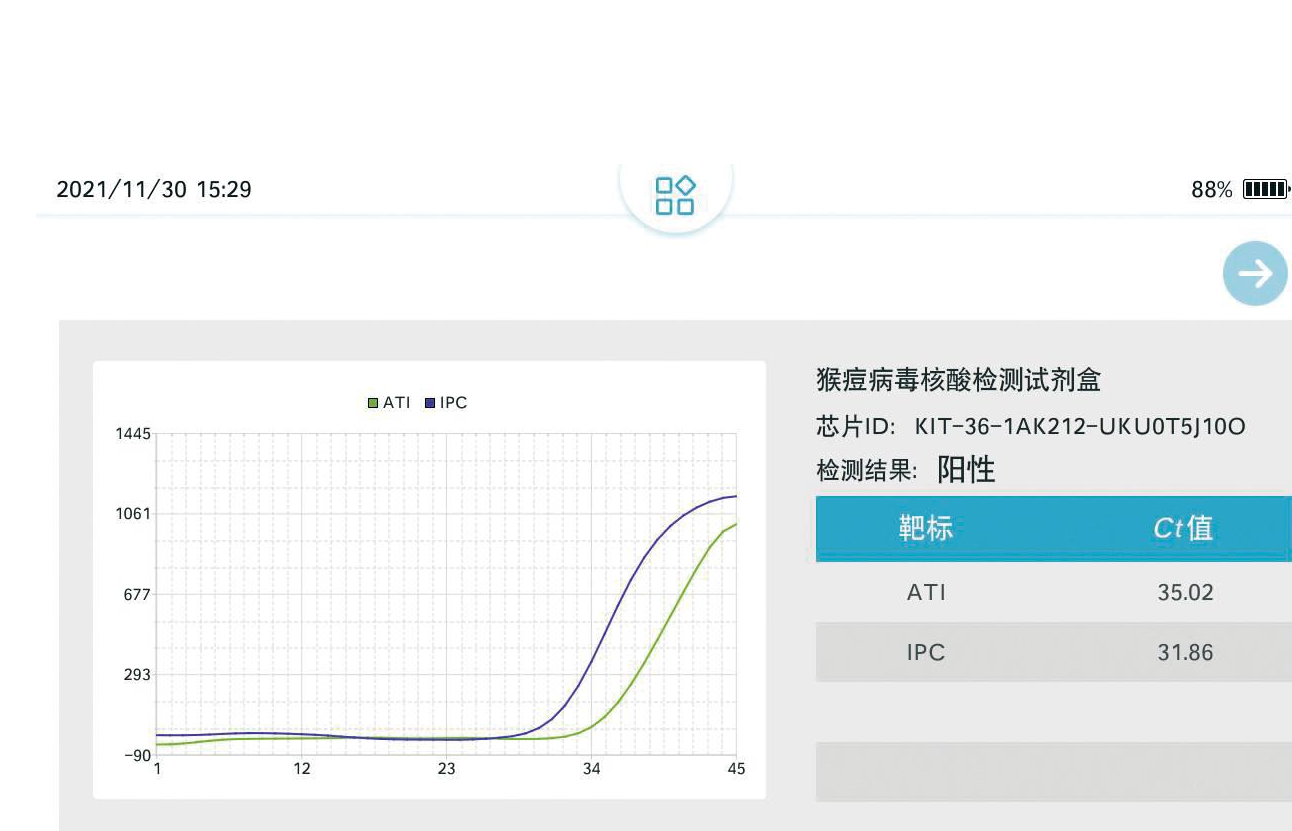
A, B, C, D, E, F, G, H: 微流控芯片重复检测MPXV结果
图8 MPXV微流控芯片检测的重复性
Fig.8 The repeatability of MPXV microfluidic chip detection
A
B
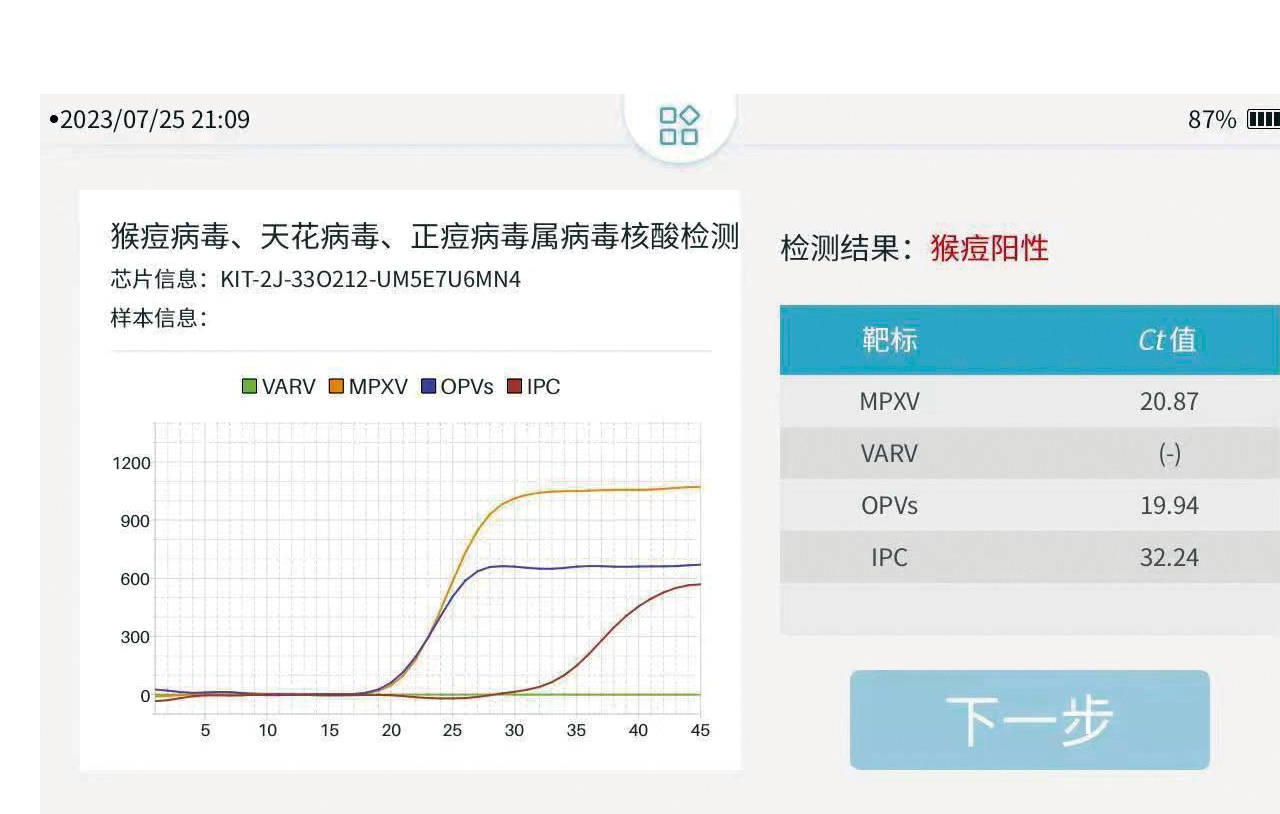
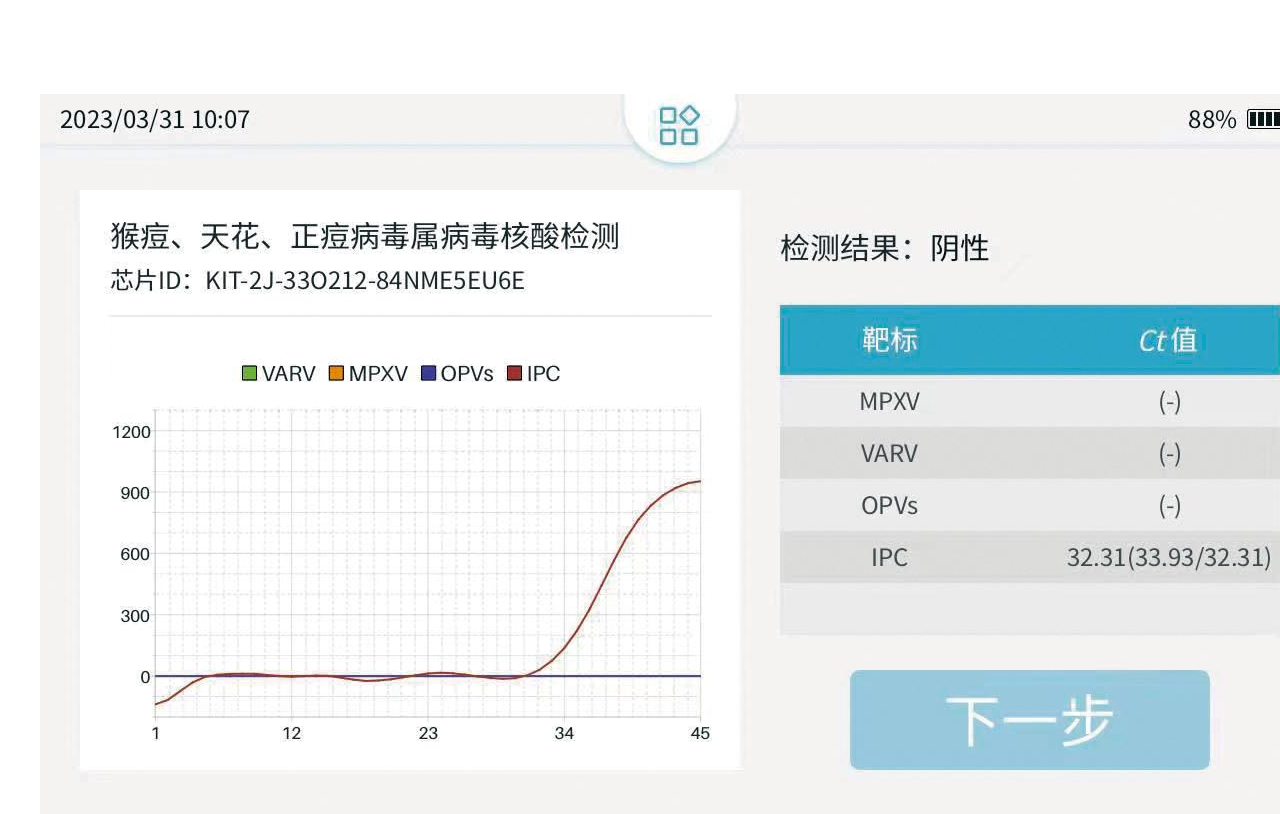
A: MPXV标准品咽拭子液; B: 健康咽拭子液
图9 微流控芯片检测患者结果
Fig.9 Detection results of patients via microfluidic chip
A: 健康咽拭子液; B: MPXV标准品咽拭子液
图10 普通实时荧光PCR检测结果
Fig.10 Detection results of conventional real-time fluorescence PCR detection







