CopyRight 2009-2020 © All Rights Reserved.版权所有: 中国海关未经授权禁止复制或建立镜像
Mediator Probe PCR检测技术的原理及其应用进展
作者:薛晓宁 张娟 徐翮飞 杜建森 王丽丽 张瑾
薛晓宁 张娟 徐翮飞 杜建森 王丽丽 张瑾
薛晓宁 1 张 娟 1 徐翮飞 1 杜建森 1 王丽丽 1 张 瑾 1 *
摘 要 中介探针聚合酶链式反应(Mediator Probe PCR,MP PCR)技术是一种基于信号生成与检测解耦设计的新型核酸检测技术。该技术通过引入一个独立的、可定制的“媒介子”寡核苷酸作为通用信号报告载体,有效克服了传统探针技术在多重检测、灵敏度与抗干扰能力方面的问题,实现了对多重靶标的高特异性、高灵敏度并行检测。本文系统阐述了MP PCR技术的技术原理、发展历程与关键技术演进,重点分析了其在病原体诊断,尤其是多重病原体与耐药基因检测、基因分型、肿瘤伴随诊断及核酸即时检测等领域的应用潜力。另外,本文还分析了该技术在引物与媒介子设计优化、成本控制及标准化方面所具有的技术优势和面临的挑战,为核酸检测技术的进一步研发、转化与应用提供理论与技术参考。
关键词 中介探针聚合酶链式反应;核酸检测;多重检测
A Review of the Principles and Application Progress of Mediator Probe PCR Detection Technology
XUE Xiao-Ning 1 ZHANG Juan 1 XU He-Fei 1 DU Jian-Sen 1 WANG Li-Li 1 ZHANG Jin 1*
Abstract Mediator Probe PCR (MP PCR) is a novel nucleic acid detection technology based on the design principle of signal generation-detection decoupling. By introducing an independent and customizable “mediator” oligonucleotide as a universal signal-reporting carrier, this technology effectively overcomes the limitations of traditional probe-based techniques in terms of multiplex detection, sensitivity, and anti-interference capability, thereby enabling the highly specific and sensitive parallel detection of multiple targets. This paper systematically reviews the core principles, development history and key technological advances of MP PCR, and elaborates on its wide application prospects in pathogen diagnosis, especially multi-pathogen and drug resistance gene detection, genotyping, tumor companion diagnosis, and nucleic acid point-of-care testing (POCT). In addition, it analyzes the advantages and challenges faced by this technology in primer/media design optimization, cost control and standardization, aiming to provide valuable theoretical and technical references for the further research and development, transformation and application of nucleic acid detection technologies.
Keywords Mediator Probe PCR; nucleic acid detection; multiplex detection
基金项目:海关总署科研项目(2023HK061)
第一作者:薛晓宁(1975—),男,汉族,山东青岛人,本科,副主任医师,主要从事分子生物学检测技术研究工作,E-mail: x_xiaoning@126.com
通信作者:张瑾(1977—),女,汉族,陕西安康人,博士,主任技师,主要从事传染病分子诊断技术研究工作,E-mail: zhjoohyn@hotmail.com
1. 青岛国际旅行卫生保健中心(青岛海关口岸门诊部) 青岛 266071
1. Qingdao International Travel Health Care Center (Port Clinic of Qingdao Customs District), Qingdao 266071
自1983年聚合酶链式反应(Polymerase Chain Reaction,PCR)技术出现以来,经历了从终点法(凝胶电泳)到实时荧光定量(Quantitative Real-Time PCR,qPCR),再到数字PCR(Digital PCR,dPCR)的不断迭代升级[1]。然而,传统探针技术,如TaqMan水解探针,逐渐暴露出两大问题:一方面,每条探针都需要单独标记荧光基团和淬灭剂,导致多重检测成本呈指数级增长;另一方面,由于荧光通道数量的限制,可同步检测的目标数通常不超过6种[2]。2012年,Faltin等[3]提出了一种创新的中介探针聚合酶链式反应(Mediator Probe PCR,MP PCR)技术,基于信号生成与检测解耦的设计理念,成功突破了上述限制。该技术通过无标记媒介子探针与靶标脱氧核糖核酸(Deoxyribonucleic Acid,DNA)特异性结合,并利用Taq酶的5'→3'核酸外切酶活性切割探针,释放中介序列(Mediator Sequence),进而与通用荧光报告基因(Universal Reporter,UR)杂交产生信号。MP PCR技术不仅显著降低了多重检测成本,还提高了检测的特异性和灵敏度。近年来,该技术在医学诊断、环境监测和食品安全等领域展现出广泛的应用前景,尤其在肿瘤液体活检和病原体检测方面取得了重要突破。
1 技术原理
Mediator Probe PCR的核心工作原理可以分为两个关键步骤:(1)探针结合与切割:媒介子探针与目标序列特异性结合,其结构包含5'端的目标互补区(Target-specific sequence)和3'端的媒介子标签(Mediator Tag)两个功能域,在PCR扩增过程中,Taq DNA聚合酶的5'→3'外切酶活性会切割与模板结合的媒介子探针,释放出游离的媒介子标签序列;(2)信号转换与激活:释放的媒介子序列随后与通用探针结合,并在Taq DNA聚合酶的催化下引导通用探针的延伸,导致通用探针的茎环结构展开,使荧光基团与淬灭基团分离,从而触发荧光信号的生成。荧光信号的强度与PCR循环中释放的媒介子标签量成正比,进而反映初始模板的浓度。由于信号生成依赖于探针切割的特异性,非特异性扩增产物(如引物二聚体)不会触发报告系统,因此显著降低了假阳性率。该技术通过解耦目标识别(媒介子探针)和信号报告(通用探针)实现了两大优势:成本效益高,单个通用报告系统可适配多种媒介子探针,大幅减少荧光标记试剂的消耗;灵活性强,仅需更换探针的目标互补区即可检测新靶标,而无需重新优化报告系统[4]。
根据图1所示,现将扩增与检测流程逐步描述如下:(a)核酸靶标准备:图中上方方框展示了扩增与检测所需的寡核苷酸组分,流程起始于核酸靶标,其可为RNA(a1)或DNA(a2)。若靶标为RNA,需先通过逆转录步骤将其转化为cDNA。(b)靶标变性:逆转录产物或原始DNA靶标在高温条件下发生变性,使双链核酸解离为单链。(c)探针与引物退火:介质探针引物分子与靶标序列退火结合。需注意,介质探针的5'端部分并不参与靶标退火。(d)延伸与切割:引物沿靶标序列延伸,同时介质探针被特异性切割。每完成一次靶标复制,即有一个介质分子被释放至溶液中。(e)介质与通用报告子结合:释放的介质分子在溶液中退火至通用报告子序列。(f)介质延伸:介质分子沿通用报告子进行延伸反应。(g)信号产生方式一:延伸反应引起荧光团去猝灭,其机制为:5′端被顺序降解,同时淬灭基团随之释放,从而产生荧光信号。(h)信号产生方式二:5′端发生位移,导致茎环结构展开,同样实现荧光去猝灭。以上所有反应步骤均在单一热循环内连续进行,实现扩增与检测的同步完成。
2 技术发展
Mediator Probe PCR技术的发展历程是从基础机制探索到临床应用优化的完整演进过程。该技术的理论根基可追溯至1991年Holland团队对Taq酶5'→3'核酸外切酶活性的发现[5],这一突破揭示了聚合酶切割探针的分子基础。随后,Lyamichev等[6]在1993年进一步阐明其切割机制属于结构特异性内切酶活性,为后续探针设计奠定了酶学基础。真正的技术革命始于2012年,Faltin团队首次提出Mediator Probe PCR概念并验证了单重检测的可行性,其核心创新在于将传统的标记探针解耦为无标记媒介子探针和通用报告系统,这一设计显著降低了检测成本并提高了信号特异性[3]。近年来,该技术在多重检测能力方面取得重大突破,2021年Borst团队开发的4重媒介子介导的微滴式数字聚合酶链式反应(Mediator Probe Droplet Digital Polymerase Chain Reaction,MP ddPCR)系统可同步检测KRAS/BRAF基因的7个高频突变(包括G12D、V600E等),其创新性在于无需调整引物浓度或退火温度即可实现稳定检测[7]。这一进展主要依赖于熔解曲线分析(Melting Curve Analysis,MCA)技术的优化,通过精确设计不同探针的Tm值差异(ΔTm≥5℃)实现多重靶标的特异性区分与定量[8-9]。
近年来,Mediator Probe PCR技术与数字PCR(Droplet Digital Polymerase Chain Reaction,ddPCR)的深度融合催生了新一代检测平台——MP ddPCR,该技术通过将介导探针系统的高特异性与数字PCR的绝对定量能力相结合,实现了检测性能的跨越式提升。研究表明,MP ddPCR可将检测灵敏度显著提升至0.004%等位基因频率(Limit of Detection,LoD),这一突破性进展使其在循环肿瘤DNA(Circulating Tumor DNA,ctDNA)低频突变检测等极具挑战性的应用场景中展现出独特优势[7-9]。在肿瘤液体活检领域,MP ddPCR技术已成功应用于EGFR T790M、KRAS G12D等关键驱动突变的超早期检测,其检测下限比常规qPCR方法降低1~2个数量级,为肿瘤微小残留病灶(Minimal Residual Disease,MRD)监测和靶向治疗疗效评估提供了强有力的技术支撑。
3 应用领域
Mediator Probe PCR技术凭借其高灵敏度、强特异性和显著的成本优势,已在医学诊断、环境监测和食品安全等多个领域展现出广泛的应用价值。
在医学诊断领域,Mediator Probe PCR技术最重要的突破体现在肿瘤液体活检方向。以结直肠癌(Colorectal Cancer,CRC)疗效监测为例,采用4重MP ddPCR技术可同步检测血浆中KRAS G12D/G13D和BRAF V600E等关键驱动突变,实现对治疗响应的动态追踪[7]。临床验证显示,该技术在18例患者随访中检测限低至1.5 拷贝/mL血浆,与单重qPCR检测结果的一致性高达98%,其超敏特性有效克服了传统组织活检的侵入性局限,为MRD的超早期预警提供了可靠工具[10]。
在病原体检测方面,针对SARS-CoV-2变异株的鉴别,Mediator Probe PCR技术可准确区分Omicron BA.2.86等高度相似亚型,其特异性设计有效减少了非特异性扩增导致的假阳性问题[11]。相较于传统荧光探针法qPCR,Mediator Probe PCR对超过10个突变靶点的检测能力具有明显优势,这一特性在结核分枝杆菌和HPV18等低载量病原体检测中也得到验证,其灵敏度可达10拷贝/反应[12-13]。
在环境监测领域[6],Mediator Probe PCR技术的高灵敏度和高抗干扰能力使其成为水质检测的理想选择。研究证实,该技术对水体中大肠杆菌O157:H7的检测限可达5 CFU/mL,这一性能显著优于传统培养方法。
食品安全检测是另一个重要应用方向,该技术已成功应用在食源性致病菌检测方面,Mediator Probe PCR可实现沙门氏菌和李斯特菌的同步快速检测,较传统方法缩短检测时间达50%,为食品安全事件应急响应争取了宝贵时间[14]。
4 技术优势与挑战
作为新一代核酸检测技术,Mediator Probe PCR展现出多方面的颠覆性优势,如表1所示,同时也面临着若干亟待解决的技术挑战。
与传统TaqMan探针相比,Mediator探针通过创新性的信号解耦设计展现出显著优势。在探针标记方面,TaqMan探针需为每条探针独立标记荧光基团和淬灭基团,而媒介子探针采用无标记设计,仅保留目标序列和媒介子标签,有效降低了检测成本[3]。信号生成机制上,TaqMan依赖探针自身的FRET效应,其淬灭效率受限于荧光—淬灭基团间距(通常为90%~95%),而媒介子系统通过媒介子标签与通用报告分子结合后,报告分子结构转换实现信号激活,淬灭效率可达99%以上[15],大幅降低了背景噪声。在多重检测能力方面,TaqMan需占用不同荧光通道(如FAM/HEX/Cy5),而Mediator仅需单一荧光通道,通过熔解温度差异(ΔTm≥5℃)区分媒介子标签即可实现4重检测[16]。此外,Mediator系统的通用报告分子可重复用于不同目标检测,避免了TaqMan平台更换靶标时需重新优化荧光标记的繁琐流程。这些特性使Mediator技术在成本敏感应用(如大规模筛查)和资源有限场景中展现出独特价值,但其非线性反应动力学和多重检测通量限制仍是当前优化的重点方向。
当然,这一方法也面临以下技术挑战。由于需要介导序列扩散至报告分子,每个循环需延长退火时间10~15 s,这也使得总检测时间增加约30%。目前最优解决方案是通过优化报告分子浓度(50~200 nm)及茎环结构稳定性来平衡反应效率与信号强度。当检测目标超过7重时,探针间交叉杂交风险显著升高[17]。最新研究采用人工智能探针设计算法(如Visual-OMP等)计算Tm值与二级结构冲突,可有效降低此类风险。随着这些问题的逐步解决,Mediator Probe PCR有望在保持成本优势的同时,进一步拓展其在精准医疗、环境监测等领域的应用深度和广度。
5 结论
Mediator Probe PCR技术通过创新的“探针切割—信号解耦”设计,在多重检测能力、成本效益和检测特异性等方面展现出显著优势,已成为突破传统核酸检测瓶颈的重要发展方向。尽管在反应动力学优化、超高多重检测稳定性等方面仍面临挑战,但随着探针设计算法、微流控整合等技术的持续发展,该技术有望进一步拓展其在精准医疗、现场快速筛查和大规模公共卫生监测中的应用边界。未来,与便携式设备、自动化系统的深度融合,将推动Mediator Probe PCR朝着更高效、更智能、更普惠的方向持续演进。
参考文献
[1] Kopylova K V, Kasparov E W, Marchenko I V, et al. Digital PCR as a Highly Sensitive Diagnostic Tool: A Review[J]. Molecular Biology, 2023, 57(5): 771-781.
[2] Marras S A. Interactive fluorophore and quencher pairs for labeling fluorescent nucleic acid hybridization probes[J]. Molecular Biotechnology, 2008, 38(3): 247-255.
[3] Faltin B, Wadle S, Roth G, et al. Mediator Probe PCR: A Novel Approach for Detection of Real-Time PCR Based on Label-Free Primary Probes and Standardized Secondary Universal Fluorogenic Reporters[J]. Clinical Chemistry, 2012, 58(11): 1546-1556.
[4] Wadle S, Lehnert M, Rubenwolf S, et al. Real-time PCR probe optimization using design of experiments approach[J]. Biomolecular detection and quantification, 2016, 7: 1-8.
[5] Holland P M, Abramson R D, Watson R, et al. Detection of specific polymerase chain reaction product by utilizing the 5'-3' exonuclease activity of Thermus aquaticus DNA polymerase[J]. Proceedings of the National Academy of Sciences of the United States of America, 1991, 88(16): 7276-7280.
[6] Lyamichev V, Brow M A, Dahlberg J E. Structure-specific endonucleolytic cleavage of nucleic acids by eubacterial DNA polymerases[J]. Science. 1993, 260(5109): 778-783.
[7] Schlenker F, Kipf E, Borst N, et al. Centrifugal Microfluidic Integration of 4-Plex ddPCR Demonstrated by the Quantification of Cancer-Associated Point Mutations[J]. Processes, 2021, 9: 97.
[8] Xu J, Wang J, Yuan B, et al. Multiprobe Amplification (MPA) with Melting Curve Analysis: A Highly Stable and Cost-Effective Platform for the Simultaneous Detection of Eight Potential Bacterial Bioterrorism Agents in Complex Samples[J]. Analytical Chemistry, 2024, 96(33): 13679-13689.
[9] Huang Q, Chen D, Du C, et al. Highly multiplex PCR assays by coupling the 5'-flap endonuclease activity of Taq DNA polymerase and molecular beacon reporters[J]. Proceedings of the National Academy of Sciences of the United States of America, 2022, 119(9): e2110672119. DOI: 10.1073/pnas.2110672119.
[10] Schlenker F, Kipf E, Deuter M, et al. Stringent Base Specific and Optimization-Free Multiplex Mediator Probe ddPCR for the Quantification of Point Mutations in Circulating Tumor DNA[J]. Cancers (Basel), 2021, 13(22): 5742. DOI: 10.3390/cancers13225742.
[11] Yan T, Zheng R, Li Y, et al. Epidemiological Insights into the Omicron Outbreak via MeltArray-Assisted Real-Time Tracking of SARS-CoV-2 Variants[J]. Viruses, 2023, 15(12): 2397. DOI: 10.3390/v15122397.
[12] Xu Y, Liang B, Du C, et al. Rapid Identification of Clinically Relevant Mycobacterium Species by Multicolor Melting Curve Analysis[J]. Journal of Clinical Microbiology, 2019, 57(1): e01096. DOI: 10.1128/JCM.01096-18.
[13] Tu C , Su B , Xiong Y, et al. Identification and quantification of gyrA variants in fluoroquinolone-resistant Mycobacterium tuberculosis in a MeltArray reaction[J].Journal of Clinical Microbiology, 2025, 63(7). DOI: 10.1128/jcm.00146-25.
[14] Wadle S, Lehnert M, Schuler F, et al. Simplified development of multiplex real-time PCR through master mix augmented by universal fluorogenic reporters[J]. Biotechniques, 2016, 61(3): 123-128.
[15] Azlinda Anwar, J Thomas August, Heng Phon Too. A stem-loop-mediated reverse transcription real-time PCR for the selective detection and quantification of the replicative strand of an RNA virus[J]. Analytical Biochemistry, 2006, 352(1): 120-128.
[16] Liao Y, Wang X, Sha C, et al. Combination of fluorescence color and melting temperature as a two-dimensional label for homogeneous multiplex PCR detection[J]. Nucleic Acids Research, 2013, 41(7): e76. DOI: 10.1093/nar/gkt004.
[17] Lehnert, Michael, Elena Kipf, Franziska Schlenker, et al. Fluorescence signal-to-noise optimisation for real-time PCR using universal reporter oligonucleotides[J]. Analytical Methods 2018, 10: 3444-3454.
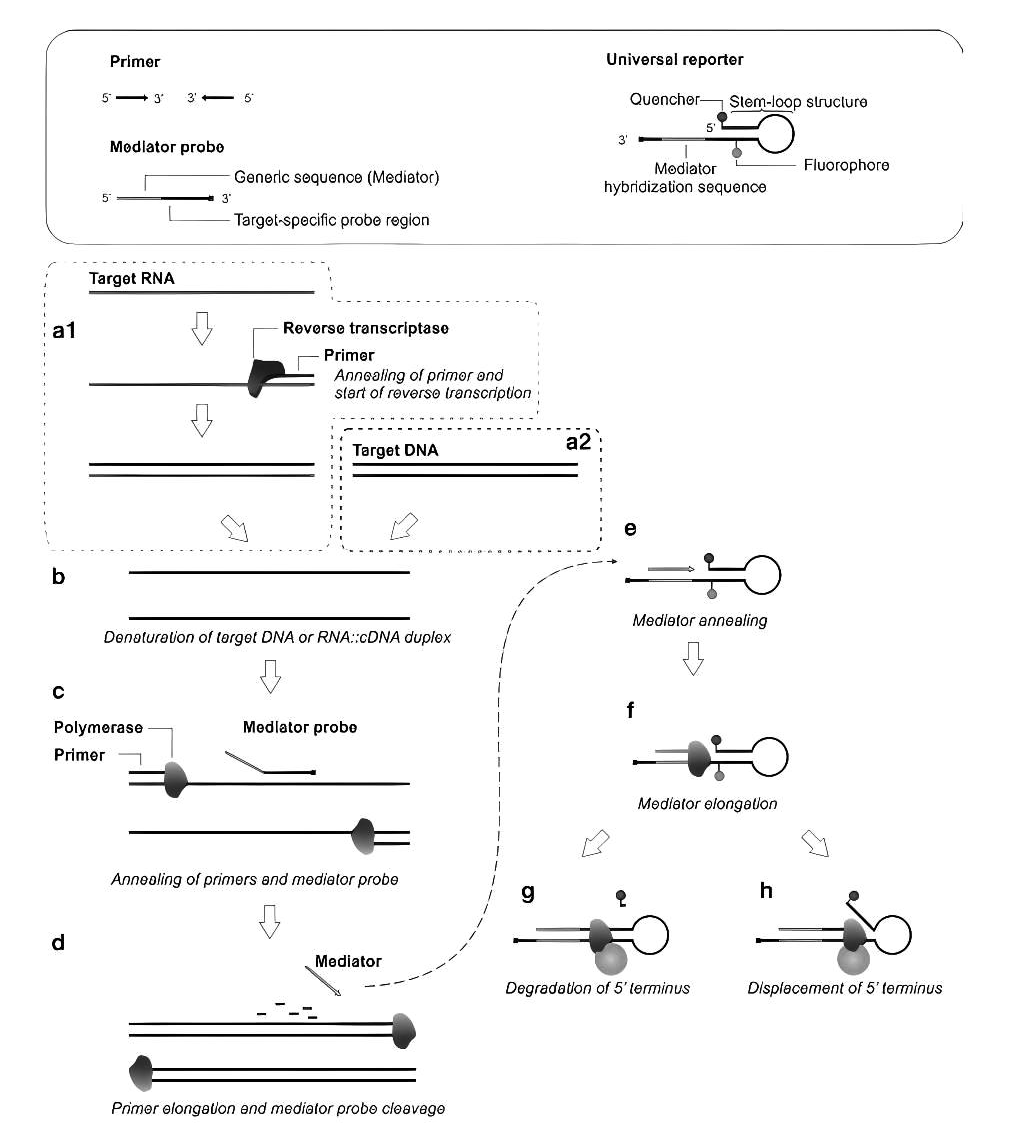
图1 Mediator Probe PCR反应机制示意图[4]
Fig.1 Schematic diagram of the reaction mechanism of Mediator Probe PCR[4]
表1 Mediator Probe PCR与qPCR比较的优势
Table 1 Advantages of Mediator Probe PCR compared with qPCR
技术特征 | 传统qPCR (荧光探针法) | Mediator Probe PCR | 优势 |
探针标记 | 每条探针独立标记荧光/淬灭剂 | 无标记 | 成本降低>60%[3] |
报告分子 | 无 | 通用设计, 可重复用于不同目标 | 多重检测无需新增荧光通道 |
信号特异性 | 依赖FRET效率 [3] | 通过结构转换实现去淬灭 | 淬灭效率>99%[5] |







