CopyRight 2009-2020 © All Rights Reserved.版权所有: 中国海关未经授权禁止复制或建立镜像
濒危植物桃儿七DNA条形码鉴定方法初探
作者:李春雷 王溪桥 解迎双 王 波 李亚平 赵晓丽
李春雷 王溪桥 解迎双 王 波 李亚平 赵晓丽
李春雷 1 王溪桥 1 * 解迎双 1 王 波 1 李亚平 1 赵晓丽 2
摘 要 本研究利用DNA条形码技术结合第三代测序技术对濒危植物桃儿七的鉴定方法进行探索性研究。通过靶向测序比较通用DNA条形码ITS2、matK、trnH-psbA、rbcL、rpoB、rpoC1、ycf1、23S rDNA等对桃儿七的鉴定效率及效果,并结合PCR扩增、测序与序列分析结果,筛选出ITS2(支持率100%)、psbA-trnH(支持率99%)、rbcL(支持率80%)适用于桃儿七的物种鉴定,其余5个条形码则不适于鉴定桃儿七。该研究结果为开发桃儿七及相关植物性资源的鉴定与保护方法提供了理论参考和实践材料。
关键词 第三代测序技术;桃儿七;DNA 条形码;物种鉴定
A Preliminary Study on DNA Barcoding Identification Method for the Endangered Plant Podophyllum hexandrum
LI Chun-Lei 1 WANG Xi-Qiao 1* XIE Ying-Shuang 1 WANG Bo 1 LI Ya-Ping 1 ZHAO Xiao-Li 2
Abstract This study explores DNA barcoding-based identification methods for the endangered plant Podophyllum hexandrum by integrating third-generation sequencing technology. Targeted sequencing was conducted to evaluate and compare the identification efficiency and performance of eight universal DNA barcodes, including ITS2, matK, trnH-psbA, rbcL, rpoB, rpoC1, ycf1, and 23S rDNA, for the species identification of P. hexandrum. Based on the results of PCR amplification, sequencing and sequence analysis, ITS2 (support rate 100%), psbA-trnH (support rate 99%), and rbcL (support rate 80%) were selected as suitable for the species identification of Podophyllum hexandrum, while the remaining five barcodes were not suitable for this purpose. These findings provide a theoretical reference and practical materials for the development of identification and conservation methods for P. hexandrum and related plant resources.
Keywords third-generation sequencing technology; Podophyllum hexandrum; DNA barcoding; species identification
桃儿七(Podophyllum hexandrum)作为小檗科(Berberidaceae)桃儿七属的珍稀多年生草本植物,是我国濒危药用植物资源。该物种主要分布于我国西部高海拔地区(陕西、甘肃、四川、云南、西藏等地),因其根茎所含鬼臼毒素具有显著的抗肿瘤活性,被列入《中国国家重点保护野生植物名录》[1]和《濒危野生动植物种国际贸易公约》(CITES)附录Ⅱ。桃儿七的抗癌药用价值催生了巨大的市场需求,一些不法商人为了谋利对桃儿七过度采挖,破坏其生境,又因其生长缓慢,导致其野生种群数量锐减,资源保护形势愈发严峻。海关对桃儿七实施严密监管,是依法阻断非法贸易链条、履行国际公约义务、维护国家生态安全与医药产业健康发展的重要举措。然而,由于桃儿七的药用形态具有多样性,包括根茎原材料、粗提取物、高纯度单体乃至含其成分的成药等,为不法分子试图通过伪报品名、夹藏携带方式逃避监管提供了可能,也给海关的鉴定工作带来挑战。
在濒危植物保护工作中,准确快速的物种鉴定技术是资源监管和执法行动的重要基础。传统形态学鉴定方法受限于标本完整性、发育阶段和专业人员经验等因素,而相比之下,分子生物学鉴定技术,特别是DNA条形码(DNA Barcoding)技术因其具有不受原材料形态、部位、生长阶段的限制,且具有取样量少、准确可靠的特点[2-6]而成为研究热点。目前,DNA 条形码技术已经实现对动物、植物和真菌物种的快速鉴定,线粒体COⅠ基因已广泛应用于动物及真菌的物种鉴定中,由于植物线粒体COⅠ基因组进化速率远慢于在动物中的进化速率,不适合作为大多数植物的编码基因,许多学者对植物中适合作为DNA条形码的基因进行了积极探索。国际生命条形码联盟建议选择叶绿体基因组片段作为条形码进行植物物种鉴定,包括rpoB、 rpoC1、matK、 rbcL、accD、nhdJ、ycf、trnH-psbA、atpF-atpH、psbK-psbⅠ等编码/非编码基因片段,此外还有核基因ITS。截至目前,采用上述条形码作为标准片段的研究很多,如Lahaye等[7-8]、Kress等[9]、Fazekas等[10]对matK进行了比对研究,其中Lahaye等的结果显示matK 390F/1326R对所研究的植物扩增率达100%,可以作为单个片段应用于植物条形码。另外,Kress等[11]应用rDNA ITS序列和质体trnH-psbA基因间序列对53个科88个属99个物种的进行研究,结果表明rDNA ITS序列和质体trnH-psbA基因间序列可以对植物物种进行DNA条形编码;Newmaster等[12]、Kress等[9]、Fazekas等[10]发现rbcL可以区分部分同属植物。
第三代测序技术的兴起为DNA条形码研究带来了新的机遇。该技术不需要经过PCR扩增,即可实现对每一条DNA分子的单独测序。这种对核酸直接进行测序的技术大大降低了因扩增引入的偏差和错误,此外,该技术的数据处理速度较快。第三代测序技术主要包括Helicoscope单分子测序技术、PacBio单分子实时测序技术(Single Molecule Real-Time Sequencing,SMRT)以及纳米孔测序技术3种。其中,纳米孔测序技术是借助电泳驱动单个分子逐一通过纳米孔来实现测序的,其无需荧光标记核苷酸、聚合酶合成,对单分子DNA链可进行实时测序,提高检测效率的同时节约了成本,可以快速、高通量地筛选到分子标记。李静等[13]利用第三代测序技术结合DNA条形码技术对当归补血方破壁饮片的物种进行了准确鉴定,也存在利用第三代测序技术未能鉴定出物种的相关研究[14],因此有建议将该技术作为探索用于组分较少的混合中草药物种鉴定研究。虽然该技术在中药材鉴定中已取得初步成功,但在濒危植物保护领域的应用仍较少。
鉴于上述研究结论,本研究运用第三代测序技术与DNA条形码相对濒危植物桃儿七的鉴定进行探索性研究。选择植物叶绿体的rpoB、 rpoC1、matK、rbcL、ycf、trnH-psbA基因序列及核基因ITS2、23S rDNA作为DNA条形码候选引物序列,通过PCR扩增、靶向测序等方式,比较并筛选适用于鉴定濒危植物桃儿七的DNA条形码。
1 材料与方法
1.1 供试样品
供试样品濒危植物桃儿七为未经加工的根原材料,不属于CITES公约第七条中关于“包装好备零售的制成品”。供试样品呈不规则圆柱形或结节状,表面棕褐色,断面类白色;未经提取、炮制或制成任何剂型,分别采购于甘肃省定西市漳县金钟镇、甘肃省定西市岷县、甘肃省定西市漳县、甘肃省陇南市宕昌县等4个不同地区。根据不同地区分别放入已编号的封口袋中以备后续实验。
1.2 主要试剂耗材
植物基因组DNA提取试剂盒 Ver.2(AG21011)、PCR扩增试剂盒(AG11009)、引物合成均购自湖南艾科瑞生物工程有限公司;直接连接建库试剂盒(C-006-0015)、直接条形码试剂盒Set A(C-006-0017)、测序试剂盒(QCell-384/6k)均购自成都奇碳泰科生物技术有限公司。
1.3 方法
1.3.1 DNA提取方法
分别取桃儿七样品的干燥根,用75%乙醇擦拭其表面以去除表面土等杂质,去除棕褐色外表皮部分,保留中间白色部分,然后分别称取50 mg,用液氮研磨至粉末状,水浴 8~12 h。利用植物基因组DNA提取试剂盒Ver.2提取总DNA。
1.3.2 PCR扩增
PCR扩增反应体系为25 μL,包含2×1 step PCR buffer,12.5 μL;上下游引物(10 μmol/L),各1.0 μL;1 step Enzyme Mix,1.0 μL;DNA 模板,2.0 μL;ddH2O,7.5 μL。扩增程序为:94℃ 5 min;94℃ 30 s, 56℃ 30 s, 72℃ 45 s, 40 个循环;72℃ 10 min;其中不同的条形码退火温度不同,具体的退火温度及DNA条形码引物信息见表1。扩增产物用1.5%琼脂糖凝胶电泳检测,并对扩增产物测序。
1.3.3 纳米孔测序
利用纳米孔测序技术对上述PCR产物进行测序,见表1。建库的具体步骤为:对PCR扩增产物进行末端修复,连接条形码接头,对连接产物进行纯化及定量,再连接测序接头,然后按照测序试剂盒说明要求进行芯片的加载及上机测序。
1.3.4 数据处理
将测序获得的序列进行拼接,然后将拼接好的序列在NCBI官网上进行序列比对,利用 MEGA 7.0软件构建进化树并分析。
2 结果与分析
2.1 PCR扩增结果及分析
从图1可知,应用ITS2、psbA-trnH、matK、23S rDNA、rbcL、rpoB、rpoC1、ycl等条形码序列设计的引物进行扩增,得到的产物除rpoC1、23S rDNA条形码存在非特异性扩增,其余的条形码条带清晰,亮度较高,稳定性好,PCR扩增效率均为100%。从片段长度上看,matK的长度最长为794 bp,ITS2的长度最短为226 bp,其余的psbA-trnH的长度为760 bp,23S rDNA的长度为363 bp,rbcL的长度为607 bp,rpoB的长度为590 bp,rpoC1的长度为487 bp,ycl的长度为600 bp。该反应体系稳定可靠,能满足DNA条形码鉴定的实验要求。
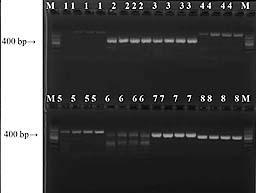
M: 1000 DNA Marker; 1-4: matk; 5-8: ITS2; 9-12: rpoB; 13-16: rpoC1; 17-20: psbA-trnH; 21-24: 23S rDNA; 25-28: rbcL; 29-32: ycl
图1 DNA条形码PCR扩增结果
Fig.1 PCR amplification results of DNA barcodes
2.2 测序结果分析
本研究同时进行了二代测序与三代测序,将两种测序方法拼接好的序列分别在 NCBI 官网上进行序列比对,得到了同样的结果。结果显示:这 8 种条形码的测序效率均达到了100%,其中ITS2、psbA-trnH、rbcL序列比对结果显示,与桃儿七的相似度高,均在99%~100%之间,与分布在我国的小檗科的其他物种,如山荷叶属(南方山荷叶)、鬼臼属(八角莲、小八角莲、川八角莲、云南八角莲、贵州八角莲、六角莲)之间的相似度均在98%以下;而matK、rpoC1序列比对结果显示,虽然与桃儿七的相似度在99%~100%之间,但与小檗科的其他物种,如南方山荷叶、日本山荷叶、八角莲、云南八角莲、贵州八角莲、川八角莲、小八角莲和六角莲的同源性也高达99%~100%;23S rDNA、rpoB、ycl序列比对后,未比对出与桃儿七及小檗科其他属的23S rDNA、rpoB、ycl基因同源性较高的序列。综上所述,ITS2、psbA-trnH、rbcL共3对引物可作为鉴别桃儿七的DNA条形码引物,而matK、rpoC1、23S rDNA、rpoB、ycl作为DNA条形码引物无法准确区分桃儿七与小檗科3个属的其他物种。
2.3 系统发育和物种鉴定
利用MEGA 7.0软件对所扩增序列进行聚类分析,分别对 8 种条形码所扩增序列及NCBI上下载的序列进行N-J系统邻接树构建。从系统邻接树可知:ITS2(图2-A)、psbA-trnH(图2-B)、rbcL(图2-C)的聚类图中,样品序列与桃儿七聚为一支,支持率分别为100%、99%、80%,可以很好地与其他小檗科植物分开。MatK(图2-D)、rpoC1(图2-E)邻接树图中,样品序列单独聚为一支,与桃儿七、小檗科其他物种均没有聚为一支。因此,ITS2、psbA-trnH、rbcL共3对引物可作为鉴别桃儿七的DNA条形码引物,在桃儿七物种分子鉴定中具有较大潜力。
3 讨论
从理论上分析,第三代高通量测序技术的测序过程无需PCR扩增,具有超长读长特征,可达二代测序的100 倍以上,因此测序速度更快、耗时更短、通量更大,可获得完整的DNA条形码序列。DNA条形码技术不同于一般的分子标记技术,它更侧重于物种识别和鉴定,通过建立鉴定数据库,可以一次性快速鉴定大量样本。本研究创新性使用第三代测序技术结合分子DNA条形码技术,为更快、更高通量地筛选到濒危植物桃儿七分子标记提供了一条新途径。另外,本研究采用靶向测序方案,目标性强,大大提高了筛选的效率以及测序的准确率,加快了方法的使用,使后期筛选的DNA条形码更为准确。
从操作过程分析,第三代测序技术操作相对简单,对实验室条件和人员要求不高,可便携移动和实现现场检测。此外,测序的整个流程最短的在几个小时内即可完成,时效性强,适用于应急疫情处理[15-16],能实现现场疫情的快速检测鉴定。操作过程需要注意DNA提取核酸的质量直接影响物种鉴定的结果。桃儿七属于根茎类药材,针对这种样品,应在前处理时通过去除外表皮,增加取样量,延长水浴时间[17-18]等步骤来提高所提取核酸的质量。
单分子测序技术在基因组、转录组、单细胞测序及蛋白质测序等领域均展现出了强大的应用潜力,其推动了临床医学的发展。桃儿七是我国重要的珍稀濒危药用植物,单分子测序技术在中药材鉴定中的应用可为本研究提供基础。同时,桃儿七作为我国濒危物种,研究开发关于它的物种鉴定技术,尝试利用第三代测序技术鉴别保护植物,不仅能为开发濒危植物及相关植物资源的保护策略与方法提供理论依据,也可为后续保护方法的开发与优化提供关键技术支撑。
参考文献
[1]国家环境保护局, 中国科学院植物研究所. 中国珍稀濒危保护植物名录[M]. 北京: 科学出版社, 1987: 28-30.
[2] Zhou X G, Ren L F, Li Y T, et al. The next-generation sequencing technology: a technology review and future perspective[J]. Science China Life Sciences, 2010, 53(1): 44-57.
[3] Ståhlberg A, Krzyzanowski P M, Egyud M, et al. Simple multiplexed PCR-based barcoding of DNA for ultrasensitive mutation detection by next-generation sequencing[J]. Nature Protocols, 2017, 12(4): 664-682.
[4] Sarwat M, M M Yamdagni. DNA barcoding, microarrays and next generation sequencing: recent tools for genetic diversity estimation and authentication of medicinal plants[J]. Critical Reviews in Biotechnology, 2016, 36(2): 191-203.
[5] Shokralla S, Gibson J F, Nikbakht H, et al. Next-generation DNA barcoding: using next- generation sequencing to enhance and accelerate DNA barcode capture from single specimens[J]. Molecular Ecology Resources, 2014, 14(5): 892-901.
[6] Ogden R, Linacre A. Wildlife forensic science: a review of genetic geographic origin assignment[J]. Forensic Science International: Genetics. 2015, 18: 152-159.
[7] Lahaye R, Savolainen V, Duthoit S, et al. A test of psbK-psbI and atpF-atpH as potential plant DNA barcodes using the flora of the Kruger National Park as a model system (South Africa)[J]. Nature Precedings, 2008, 1896: 1. DOI: hdl.handle.net/10210/8915.
[8] Lahaye R, van der Bank M, Bogarin D, et al. DNA barcoding the floras of biodiversity hotspots[J]. Proceedings of the National Academy of Sciences of the United States of America, 2008, 105(8): 2923-2928.
[9] Kress W J, Wurdack K J, Zimmer E A, et al. Use of DNA barcodes to identify flowering plants[J]. Proceedings of the National Academy of Sciences of the United States of America, 2005, 102(23): 8369-8374.
[10] Fazekas A J, Burgess K S, Kesanakurti P R, et al. Multiple multilocus DNA barcodes from the plastid genome discriminate plant species equally well[J]. Plos One, 2008,3(7): e2802. PMID: 18665273 PMCID: PMC2475660.
[11] Kress W J, Erickson D L. A two locus global DNA barcode for land plants: the coding rbcL gene complements the non-coding trnH-psbA spacer region[J]. Plos One, 2007, 2(6): e508. DOI: 10.1371/journal.pone.0000508.
[12] Newmaster S G, Fazekas A J, Ragupathy S. DNA barcoding in land plants:evaluation of rbcL in a multigene tiered approach[J]. Canadian Journal of Botany, 2006, 84(3): 335-341.
[13]李静, 王梦婷, 宋经元, 等. 基于高通量测序技术的当归补血方破壁饮片物种组成分析[J]. 中国中药杂志, 2022, 47(10): 2700-2707.
[14] Zheng X S, Zhang P, Liao B S, et al. A comprehensive quality evaluation system for complex herbal medicine using pacbio sequencing,PCR-denaturing gradient gel electrophoresis and several chemical approaches[J]. Frontiers in Plant Science, 2017, 8: 1578. DOI: 10.3389/fpls.2017.01578.
[15]甘明宇, 李刚, 俞惠, 等. 宏基因组Nanopore测序在儿童呼吸道病原微生物快速检测中的应用价值[J]. 中国循证儿科杂志, 2020, 15(5): 378-381.
[16]邓浩辉, 刘惠媛, 高洪波, 等. 纳米孔三代测序在HIV/AIDS合并肺部感染者快速病原学鉴定的应用价值探讨[J]. 转化医学杂志, 2021, 10(1): 45-47.
[17]段中岗, 黄琼林, 杨锦芬, 等. 适合中药材DNA条形码分析的DNA提取方法的研究[J].中药新药与临床药理, 2009, 20(5): 480-484.
[18]罗焜, 马培, 姚辉, 等. 中药DNA条形码鉴定中的DNA提取方法研究[J]. 世界科学技术(中医药现代化), 2012, 14(2): 1433-1439.
基金项目:海关总署科研项目(2023HK015)
第一作者:李春雷(1988—),女,汉族,辽宁锦州人,硕士,农艺师,主要从事植物检疫工作,E-mail: 936844930@qq.com
通信作者:王溪桥(1984—),男,汉族,甘肃兰州人,硕士,高级农艺师,主要从事植物检疫工作,E-mail: brooksu37@163.com
1. 兰州海关技术中心 兰州 730010
2. 中国海关科学技术研究中心 北京 100026
1. Lanzhou Customs Technology Center, Lanzhou 730010
2. Science and Technology Research Center of China Customs, Beijing 100026

表1 PCR反应引物序列
Table 1 The primer sequence of PCR amplification
序号 | 引物 | 序列 (5'-3' ) | 退火温度 (°C) |
1 | ITS2 F | ATGCGATACTTGGTGTGAAT | 56 |
ITS3 R | GACGCTTCTCCAGACTACAAT | ||
2 | trnH | CGCGCATGGTGGATTCACAATCC | 58 |
psbA | GTTATGCATGAACGTAATGCTC | ||
3 | rbcLa F | ATGTCACCACAAACAGAGACTAAAGC | |
rbcLa R | CTTCTGCTACAAATAAGAATCGATCTC | ||
4 | p23SrV F1 | GGACAGAAAGACCCTATGAAGCTT | |
p23SrV R1 | TCAGCCTGTTATCCCTAGAGTAAC | ||
5 | rpoB 1f | AAGTGCATTGTTGGAACTGG | |
rpoB 4r | GATCCCAGCATCACAATTCC | ||
6 | rpoC1 2f | GGCAAAGAGGGAAGATTTCG | |
rpoC1 4r | CCATAAGCATATCTTGAGTTGG | ||
7 | Matk 390F | CGATCTATTCATTCAATATTTC | 48 |
Matk 1326R | TCTAGCACACGAAAGTCGAAGT | ||
8 | Ycl 1bF | TCTCGACGAAAATCAGATTGTTGTGA | 57 |
Ycl 1bR | ATACATGTCAAAGTGATGGAAAA |
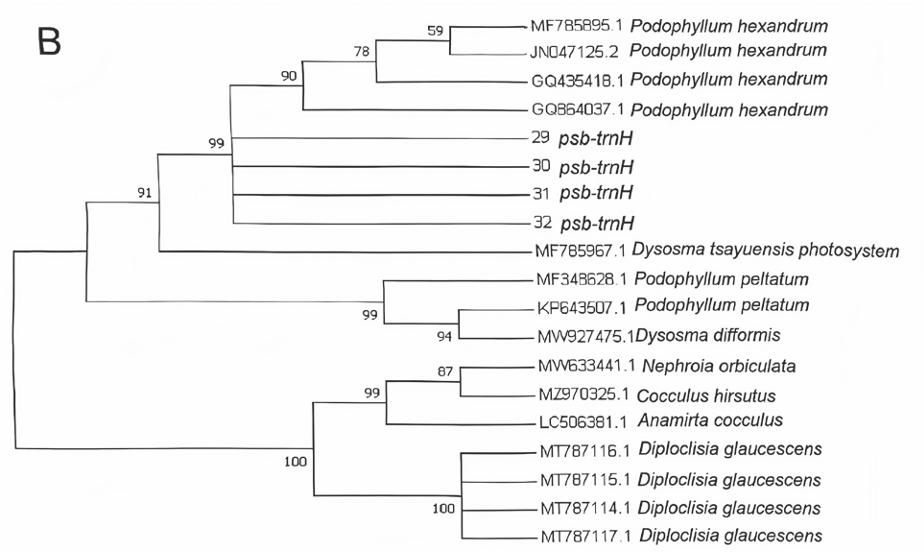
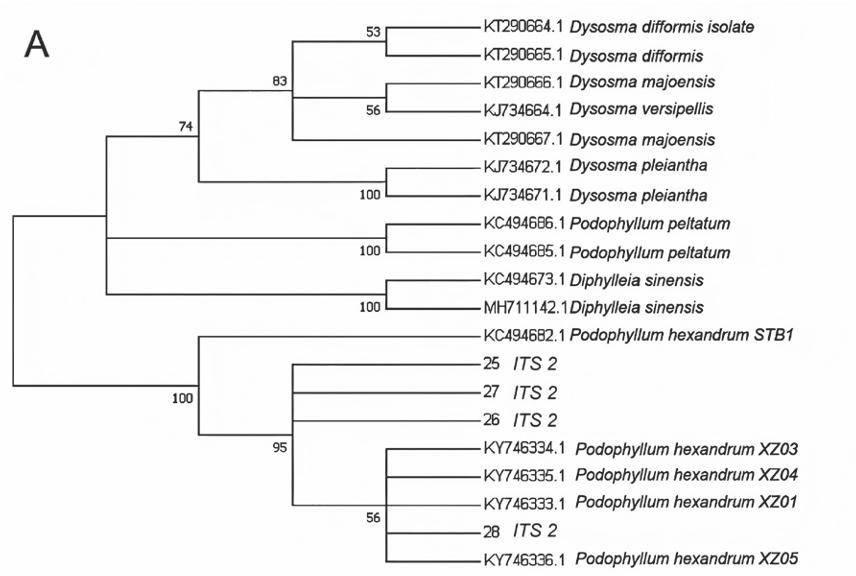
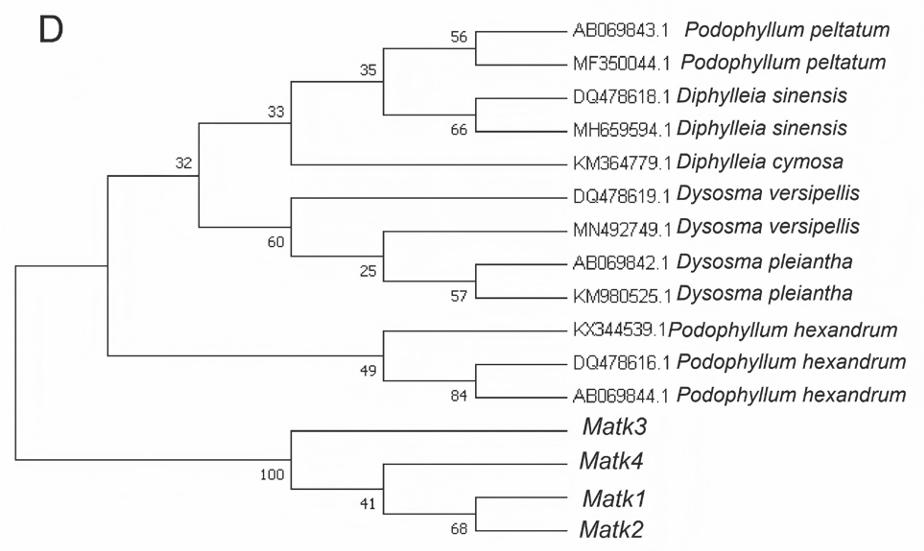
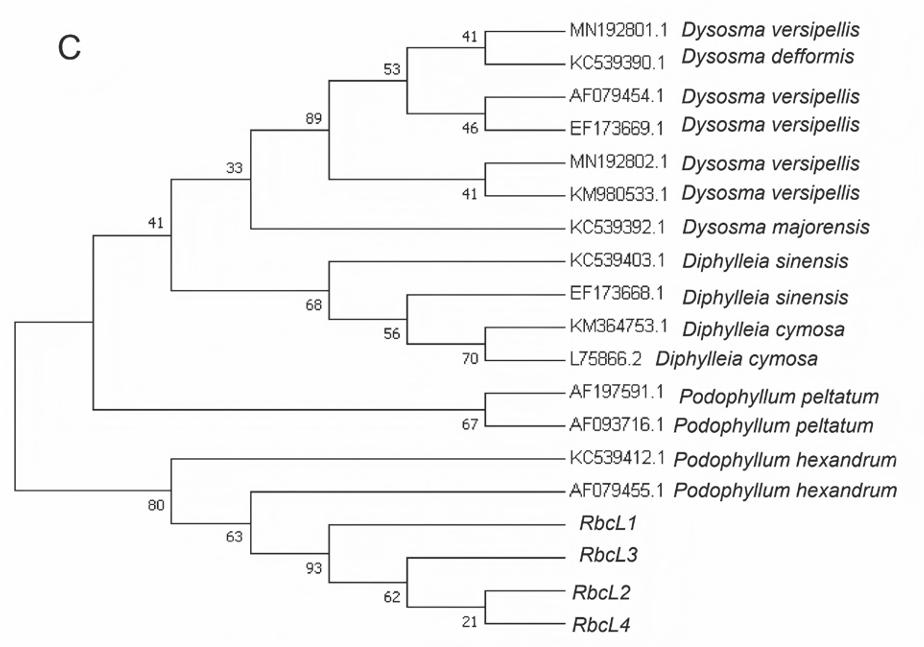
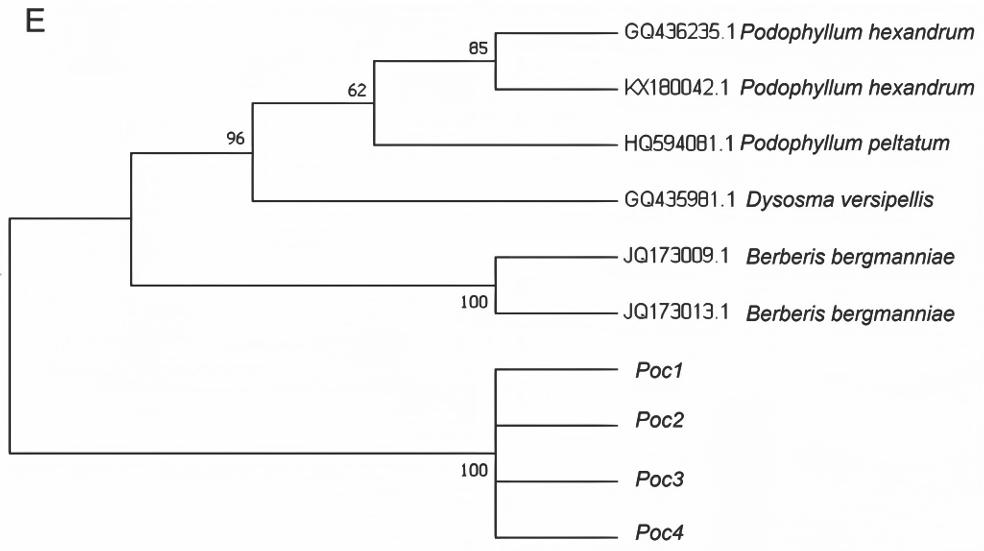
A: ITS 2; B: psbA-trnH ; C: rbcL ; D: MatK ; E: rpoC 1
图2 基于DNA条形码序列构建的系统发育树
Fig.2 Phylogenetic tree constructed based on DNA barcode sequences







